氮与氟、硫、镓三种元素之间可以形成具有特殊组成和性质的化合物。回答下列问题:
(1)基态镓原子电子排布式为___ ;硫原子核外有___ 种运动状态不同的电子。
(2)第一电离能符号为I1,I1(N)___ I1(S)(填“>”或“<”)。
(3)NSF(N=S-F)与SNF(S=N-F)互为同分异构体。
①关于NSF与SNF的说法正确的是___ (填标号)。
A.二者均含有极性键和非极性键
B.二者均含有σ键与π键
C.二者均为非极性分子
D.二者与SO2均互为等电子体
②NSF发生聚合生成三聚分子A(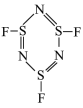 ),SNF发生聚合生成三聚分子B(
),SNF发生聚合生成三聚分子B( ),分子A中σ键与π键数目之比为
),分子A中σ键与π键数目之比为___ ,分子B中氮原子价电子空间构型为___ 。
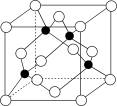
(4)氮化镓是直接隙半导体材料,具有易发光、电光转化效率高的特点。某种立方晶型氮化镓晶胞如图所示。(图中“O”与“●”大小比例关系符合二者原子实际大小比例关系)
①图中“●”表示的原子为___ (填元素符号)。
②已知NA为阿伏加 德罗常数的值,晶胞的密度为dg·cm-3。则晶胞的边长为___ nm。两个距离最近的氮原子之间的距离为___ nm。(均用含d和NA的式子表示)
(1)基态镓原子电子排布式为
(2)第一电离能符号为I1,I1(N)
(3)NSF(N=S-F)与SNF(S=N-F)互为同分异构体。
①关于NSF与SNF的说法正确的是
A.二者均含有极性键和非极性键
B.二者均含有σ键与π键
C.二者均为非极性分子
D.二者与SO2均互为等电子体
②NSF发生聚合生成三聚分子A(
 ),SNF发生聚合生成三聚分子B(
),SNF发生聚合生成三聚分子B( ),分子A中σ键与π键数目之比为
),分子A中σ键与π键数目之比为(4)氮化镓是直接隙半导体材料,具有易发光、电光转化效率高的特点。某种立方晶型氮化镓晶胞如图所示。(图中“O”与“●”大小比例关系符合二者原子实际大小比例关系)
①图中“●”表示的原子为
②已知NA为阿伏加 德罗常数的值,晶胞的密度为dg·cm-3。则晶胞的边长为

更新时间:2020-06-29 17:18:48
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】深井岩盐的主要配料为:精制盐、碘酸钾(KIO3)、亚铁氰化钾[K4Fe(CN)6·3H2O]。其中亚铁氰化钾的无水盐在高温下会发生分解:3K4[Fe(CN)6] 2(CN)2↑+12KCN+N2↑+Fe3C+C
2(CN)2↑+12KCN+N2↑+Fe3C+C
请回答下列问题:
(1)①Fe2+基态核外电子排布式为_____ 。
② 的空间构型为
的空间构型为______ (用文字描述)。
③(CN)2分子中碳原子杂化轨道类型为_______ ,一种与CN-互为等电子体的分子的电子式为_______ 。
④1molFe(CN)63−中含有σ键的数目为____ mol。
(2)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=___ 。Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于____ (填晶体类型)。
(3)如图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体,则该立方体是不是Fe3O4的晶胞______ (填“是”或“否”),立方体中三价铁离子处于氧离子围成的________ (填空间结构)空隙。

(4)Fe能形成多种氧化物,其中FeO晶胞结构为NaCl型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响。由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1),若测得某FexO晶体密度为5.71g•cm﹣3,晶胞边长为4.28×10﹣10 m,则FexO中x=____ 。(用代数式表示,不要求算出具体结果)。
 2(CN)2↑+12KCN+N2↑+Fe3C+C
2(CN)2↑+12KCN+N2↑+Fe3C+C请回答下列问题:
(1)①Fe2+基态核外电子排布式为
②
 的空间构型为
的空间构型为③(CN)2分子中碳原子杂化轨道类型为
④1molFe(CN)63−中含有σ键的数目为
(2)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=
(3)如图是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体,则该立方体是不是Fe3O4的晶胞

(4)Fe能形成多种氧化物,其中FeO晶胞结构为NaCl型。晶体中实际上存在空位、错位、杂质原子等缺陷,晶体缺陷对晶体的性质会产生重大影响。由于晶体缺陷,在晶体中Fe和O的个数比发生了变化,变为FexO(x<1),若测得某FexO晶体密度为5.71g•cm﹣3,晶胞边长为4.28×10﹣10 m,则FexO中x=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2,元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)基态X原子核外共有___________ 种运动状态不同的电子,其价电子排布式为___________ 。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是___________ 。
(3)写出一种由第三周期元素组成的与YZ 互为等电子体的分子的电子式:
互为等电子体的分子的电子式:___________ 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为___________ 。
(1)基态X原子核外共有
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
(3)写出一种由第三周期元素组成的与YZ
 互为等电子体的分子的电子式:
互为等电子体的分子的电子式:(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氟硼酸盐是化工生产中比较常见的一类物质,如 、
、 、
、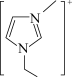
 等。
等。
(1)下列状态的氟中,失去最外层一个电子所需要的能量最大的为___________(填字母)。
(2) 是合成深紫色固体氟硼铍酸钾的原料。
是合成深紫色固体氟硼铍酸钾的原料。 能结合
能结合 形成
形成 ,在此过程中F—B—F键的键角将
,在此过程中F—B—F键的键角将___________ (填“减小”或“增大”)。
(3)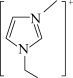
 是一种液体电解质,在有机合成中能提高氢化反应的选择性。
是一种液体电解质,在有机合成中能提高氢化反应的选择性。
①该物质的组成元素中属于p区元素的有___________ 种。
②该物质中C原子的杂化类型为___________ 。
③与 (熔点:530℃)相比,该物质熔点较低的可能原因为
(熔点:530℃)相比,该物质熔点较低的可能原因为______ 。
(4) 是合成新型材料氮化硼的原料之一、
是合成新型材料氮化硼的原料之一、
① 中对键合电子吸引能力最强的元素是
中对键合电子吸引能力最强的元素是____ (填元素符号),其中配位键与 键的数目之比为
键的数目之比为____ 。
②氮化硼的主要结构有六方氮化硼和立方氮化硼,其中立方氮化硼晶胞的截面图如图所示:

据此判断,每个晶胞中含有B的数目为____ ,B、N原子之间的最短距离为______ nm。
 、
、 、
、
 等。
等。(1)下列状态的氟中,失去最外层一个电子所需要的能量最大的为___________(填字母)。
A. | B. |
C. | D. |
 是合成深紫色固体氟硼铍酸钾的原料。
是合成深紫色固体氟硼铍酸钾的原料。 能结合
能结合 形成
形成 ,在此过程中F—B—F键的键角将
,在此过程中F—B—F键的键角将(3)

 是一种液体电解质,在有机合成中能提高氢化反应的选择性。
是一种液体电解质,在有机合成中能提高氢化反应的选择性。①该物质的组成元素中属于p区元素的有
②该物质中C原子的杂化类型为
③与
 (熔点:530℃)相比,该物质熔点较低的可能原因为
(熔点:530℃)相比,该物质熔点较低的可能原因为(4)
 是合成新型材料氮化硼的原料之一、
是合成新型材料氮化硼的原料之一、①
 中对键合电子吸引能力最强的元素是
中对键合电子吸引能力最强的元素是 键的数目之比为
键的数目之比为②氮化硼的主要结构有六方氮化硼和立方氮化硼,其中立方氮化硼晶胞的截面图如图所示:

据此判断,每个晶胞中含有B的数目为
您最近一年使用:0次
【推荐1】我国科学家在《National Science Review》上报道了具有特殊稳定性的类钙钛矿结构中性团簇Co13O8,理论研究表明该团簇具有独特的立方芳香性。这类新型的氧钝化金属团簇有望用作基因新材料,研究人员将其命名为“金属氧立方”。回答下列问题:
(1)钴元素的常见价态为+2和+3。写出+3价基态钴离子的价电子排布图_______ 。
(2)辉砷钴矿(主要成分为CoAsS)是一种常见的钴矿石。
①CoAsS中三种元素的电负性大小关系为_______ 。O、S、As的简单氢化物分子键角从大到小的顺序为_______ ,原因是_______ 。
②砷的硫化物有多种,有一种硫化砷的结构为 ,则该分子中发生sp3杂化的元素有
,则该分子中发生sp3杂化的元素有_______ 种;还有一种线型结构As2S2,该分子中各原子均达到8电子稳定结构,As2S2的电子式为_______ 。
(3)钴离子极易形成配合物,如[Co(NH3)6](NO3)3,与NH3互为等电子体的阳离子有_______ (任写一种), 中的大π键为
中的大π键为_______ 。
(4)Co13O8中性团簇分子的结构如图所示,该分子中每个氧原子周围距离最近且相等的钴原子有_______ 个。
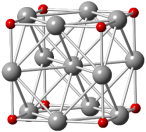
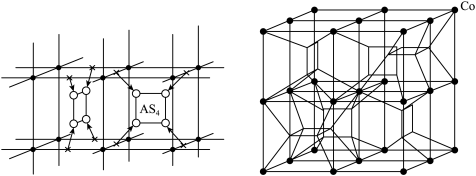
(5)方钴矿(钴的砷化合物)晶体的晶胞结构如下图所示,下图中的右图为一个完整的晶胞,图中黑球表示Co,正方形结构放大之后如下左图所示(白圈表示As,符号×不表示原子,只是表示该点为线段中点),该晶体的化学式为_______ 。设NA表示阿伏加德罗常数的值,最近两个Co原子之间的距离为a pm,则该晶体密度为_______ g·cm-3(列出表达式)。
(1)钴元素的常见价态为+2和+3。写出+3价基态钴离子的价电子排布图
(2)辉砷钴矿(主要成分为CoAsS)是一种常见的钴矿石。
①CoAsS中三种元素的电负性大小关系为
②砷的硫化物有多种,有一种硫化砷的结构为
 ,则该分子中发生sp3杂化的元素有
,则该分子中发生sp3杂化的元素有(3)钴离子极易形成配合物,如[Co(NH3)6](NO3)3,与NH3互为等电子体的阳离子有
 中的大π键为
中的大π键为(4)Co13O8中性团簇分子的结构如图所示,该分子中每个氧原子周围距离最近且相等的钴原子有

(5)方钴矿(钴的砷化合物)晶体的晶胞结构如下图所示,下图中的右图为一个完整的晶胞,图中黑球表示Co,正方形结构放大之后如下左图所示(白圈表示As,符号×不表示原子,只是表示该点为线段中点),该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铜、锌原子结构的特殊性,决定了它们的单质及其化合物在化工生产中发挥着重要的作用,回答下列问题。
(1)基态锌原子的价电子排布式为___________ ,基态 的核外电子存在
的核外电子存在___________ 种不同的空间运动状态。
(2)当黄铜受到氨腐蚀时,会出现“龟裂”现象,生成四氨合铜配合物。
① 中各非金属元素电负性由大到小的顺序为
中各非金属元素电负性由大到小的顺序为___________ ;阴离子中心原子的杂化轨道类型是___________ ,空间构型为___________ 。
② 中
中 的键角比独立
的键角比独立 的键角
的键角___________ (填“大”“小”或“相等”),原因是___________ 。
(3) 的熔点为872℃,
的熔点为872℃, 的熔点为275℃,
的熔点为275℃, 和
和 熔点差异大的原因为
熔点差异大的原因为___________ 。
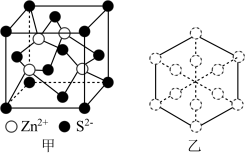
(4)立方ZnS晶体常用作半导体材料,其晶胞结构如图甲所示,密度为 。
。
①两个S原子之间的最短距离为___________ nm(已知 为阿伏加德罗常数的值,用含
为阿伏加德罗常数的值,用含 、d的代数式表示)。
、d的代数式表示)。
②若ZnS晶胞沿体对角线方向投影,所得的Zn原子投影外围图形为正六边形,如图乙所示,则S原子的投影外围图形为___________ 。
(1)基态锌原子的价电子排布式为
 的核外电子存在
的核外电子存在(2)当黄铜受到氨腐蚀时,会出现“龟裂”现象,生成四氨合铜配合物。
①
 中各非金属元素电负性由大到小的顺序为
中各非金属元素电负性由大到小的顺序为②
 中
中 的键角比独立
的键角比独立 的键角
的键角(3)
 的熔点为872℃,
的熔点为872℃, 的熔点为275℃,
的熔点为275℃, 和
和 熔点差异大的原因为
熔点差异大的原因为(4)立方ZnS晶体常用作半导体材料,其晶胞结构如图甲所示,密度为
 。
。
①两个S原子之间的最短距离为
 为阿伏加德罗常数的值,用含
为阿伏加德罗常数的值,用含 、d的代数式表示)。
、d的代数式表示)。②若ZnS晶胞沿体对角线方向投影,所得的Zn原子投影外围图形为正六边形,如图乙所示,则S原子的投影外围图形为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】由H、C、O、N、S、Al、Fe、Ti等元素能形成多种物质。这些物质有许多用途。请回答下列问题:
(1)某同学写出了铝原子的4种不同状态的电子排布图:
A. B.
B.
C. D.
D.
其中能量最低的是____ (填字母),状态D是铝原子的某种激发态,但该电子排布图有错误,主要是违背了____ 。
(2)C、O、N原子的第一电离能由大到小的顺序为____ ;H2S的键角(94°)比H2O的键角(105°)小的原因是____ 。
(3)铁能与三氮唑(结构见图甲)形成多种配合物。

①lmol三氮唑中所含σ键的数目为____ mol;碳原子杂化方式是____ 。
②三氮唑的沸点为260℃,与之结构相似且相对分子质量接近的环戊二烯(结构见图乙)的沸点为42.5℃,前者沸点较高的原因是____ 。
(4)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是____ 。
(5)近年来,钙钛矿太阳能电池是光电材料领域的研究热门,其晶胞结构如图所示,钙钛矿的化学式为____ ,该晶胞中Ca2+与O2-的最短距离是____ cm(已知晶胞参数为anm)。

(1)某同学写出了铝原子的4种不同状态的电子排布图:
A.
 B.
B.
C.
 D.
D.
其中能量最低的是
(2)C、O、N原子的第一电离能由大到小的顺序为
(3)铁能与三氮唑(结构见图甲)形成多种配合物。

①lmol三氮唑中所含σ键的数目为
②三氮唑的沸点为260℃,与之结构相似且相对分子质量接近的环戊二烯(结构见图乙)的沸点为42.5℃,前者沸点较高的原因是
(4)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是
(5)近年来,钙钛矿太阳能电池是光电材料领域的研究热门,其晶胞结构如图所示,钙钛矿的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中②和⑦两元素形成的五原子分子的结构式为_______________________ ;
(2)由③和⑤两元素形成的物质与NaOH溶液反应的离子方程式为_______________________ ;
(3)由元素①和②的原子构成的R离子空间构型为平面正三角形,则该离子符号为________ ;其中心原子的杂化类型为_______________________ ;
(4)下列说法正确的是_______________________ ;
a.电负性②>③ b.③⑥两元素能形成极性分子
c.④⑦两元素形成的化合物中只含离子键 d.⑧⑨⑩三元素最外层电子数均为2
(5)M元素与表中元素⑨既同族又同周期,是一种重要的金属元素,若人体内M元素的含量偏低,则会影响O2在体内的正常运输。已知M2+与CN-溶液反应得到M(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成六配位化合物。
上述沉淀溶解过程的化学方程式为_______________________ 。

请回答下列问题:
(1)表中②和⑦两元素形成的五原子分子的结构式为
(2)由③和⑤两元素形成的物质与NaOH溶液反应的离子方程式为
(3)由元素①和②的原子构成的R离子空间构型为平面正三角形,则该离子符号为
(4)下列说法正确的是
a.电负性②>③ b.③⑥两元素能形成极性分子
c.④⑦两元素形成的化合物中只含离子键 d.⑧⑨⑩三元素最外层电子数均为2
(5)M元素与表中元素⑨既同族又同周期,是一种重要的金属元素,若人体内M元素的含量偏低,则会影响O2在体内的正常运输。已知M2+与CN-溶液反应得到M(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成六配位化合物。
上述沉淀溶解过程的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D为原子序数依次增大的非金属短周期主族元素,其中A的某种单质是重要的半导体材料。请回答下列问题:
(1)A在元素周期表中的位置为___________ 。
(2)B元素的最高价氧化物的分子式为___________ 。高速通信离不开光导纤维,用于制造光导纤维的基本原料是___________ (填化学式)。
(3)从原子结构角度解释D的非金属性大于C的原因:___________ 。
(4)化合物C2D2在合成橡胶、硬水软化等方面有着重要应用。C2D2分子的结构式为___________ 该分子属于___________ 分子(填“极性”或“非极性”)。
(5)化合物M是制备晶体A的中间产物,它是由A、D和氢三种元素按原子个数比1:3:l组成的。M极易水解,其完全水解的产物除了A的最高价含氧酸外,还有两种气体,这两种气体是___________ (填化学式)。
(1)A在元素周期表中的位置为
(2)B元素的最高价氧化物的分子式为
(3)从原子结构角度解释D的非金属性大于C的原因:
(4)化合物C2D2在合成橡胶、硬水软化等方面有着重要应用。C2D2分子的结构式为
(5)化合物M是制备晶体A的中间产物,它是由A、D和氢三种元素按原子个数比1:3:l组成的。M极易水解,其完全水解的产物除了A的最高价含氧酸外,还有两种气体,这两种气体是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】前四周期元素A、B、C、D、E的原子序数依次增大,基态A原子核外电子占据3个轨道,基态B原子核外电子占据3个能级且每个能级上电子数相等,C的双原子单质分子中σ键和π键数目之比为1∶2,D的最高化合价和最低化合价代数和等于4;基态E原子核外有6个未成对电子。
(1)基态E原子的核外电子排布式为____ ,该元素位于周期表的____ 区,基态D原子核外电子所占据____ 个轨道。
(2)A元素的各级电离能数据如表:
分析表中数据可知,相邻两级的电离能中,I3和I4之间差异最大,其主要原因是____ 。
(3)A、B、C元素的最高价氧化物对应的水化物酸性依次增强,其原因是____ 。
(4)氯元素与元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp3杂化、空间结构为三角锥形的是____ (填分子式)。
(5)(DC)4为热色性固体,且有色温效应。其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。在淡黄色→橙黄色→深红色的转化中,破坏的作用力是___ ;在常压下,(DC)4高于130℃分解为相应的单质,这一变化中破坏的作用力是____ 。在B、C、D的简单气态氢化物中,属于非极性分子的是____ (填分子式)。
(1)基态E原子的核外电子排布式为
(2)A元素的各级电离能数据如表:
| 符号 | I1 | I2 | I3 | I4 | I5 |
| 电离能/(kJ·mol-1) | 800.6 | 2427 | 3660 | 25026 | 32827 |
(3)A、B、C元素的最高价氧化物对应的水化物酸性依次增强,其原因是
(4)氯元素与元素组成的共价分子ACl3、BCl4、CCl3中,中心原子采用sp3杂化、空间结构为三角锥形的是
(5)(DC)4为热色性固体,且有色温效应。其颜色在低于-30℃时为淡黄色,室温下为橙黄色,高于100℃时为深红色。在淡黄色→橙黄色→深红色的转化中,破坏的作用力是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铜碘杂化团簇具有优异的光学性能,可用于制备发光二极管、发光墨水、生物成像仪器等。一种铜碘杂化团簇的合成路线如图:

(1)已知SbCl3(三氯化锑)是挥发性显著的物质,由此判断SbCl3中主要含有的化学键类型是___ 。
(2)Sb为第四周期VA族元素,预测SbCl3的立体结构为___ 。
(3)Et2O(CH3CH2OCH2CH3,乙醚)中氧原子以及 中碳原子的杂化类型分别是
中碳原子的杂化类型分别是___ 、___ 。
(4)CuI中Cu+的核外电子排布式为___ 。
(5)SbCy3只能与一个Cu+配位的原因是___ 。
(6)已知上述铜碘杂化团簇属四方晶系,晶胞参数分别为anm、bnm、cnm,棱间夹角为α=β=γ=90°,平均一个晶胞含有一个铜碘杂化团簇,该团簇的化学式为___ 。设阿伏加 德罗常数的值为NA,已知SbCy的相对分子量是371,则该铜碘杂化团簇的密度是___ g·cm-3(列计算式)。

(1)已知SbCl3(三氯化锑)是挥发性显著的物质,由此判断SbCl3中主要含有的化学键类型是
(2)Sb为第四周期VA族元素,预测SbCl3的立体结构为
(3)Et2O(CH3CH2OCH2CH3,乙醚)中氧原子以及
 中碳原子的杂化类型分别是
中碳原子的杂化类型分别是(4)CuI中Cu+的核外电子排布式为
(5)SbCy3只能与一个Cu+配位的原因是
(6)已知上述铜碘杂化团簇属四方晶系,晶胞参数分别为anm、bnm、cnm,棱间夹角为α=β=γ=90°,平均一个晶胞含有一个铜碘杂化团簇,该团簇的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】锌及其化合物在工农业生产及科学研究中具有广泛的用途。回答下列问题:
(1)Zn位于元素周期表的___________ 区,基态Zn2+的核外电子排布式为___________ 。
(2)氨基酸锌是研究最早和使用最广泛的第三代锌添加剂,该添加剂具有优良的营养功能。如图1是氨基酸锌的结构简式。
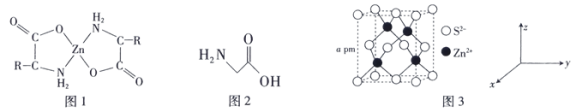
①组成氨基酸锌的C、N、O的电负性由大到小的顺序是___________ 。
②氨基酸锌的Zn2+形成配位键,其中提供空轨道的原子是___________ 。
③最简单的氨基酸是甘氨酸(结构简式如图2),其结构中π键与σ键的数量比为___________ 。
(3)ZnS可用于制白色颜料、玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS的晶胞如图3所示。
①上图中 的坐标有
的坐标有 、
、 ,与
,与 距离最近的
距离最近的 还有
还有___________ (填坐标)。
②Zn2+占据___________ (填“八面体”或“四面体”)空隙,空隙利用率为___________ %。
③ZnS的密度为___________  。
。
(1)Zn位于元素周期表的
(2)氨基酸锌是研究最早和使用最广泛的第三代锌添加剂,该添加剂具有优良的营养功能。如图1是氨基酸锌的结构简式。

①组成氨基酸锌的C、N、O的电负性由大到小的顺序是
②氨基酸锌的Zn2+形成配位键,其中提供空轨道的原子是
③最简单的氨基酸是甘氨酸(结构简式如图2),其结构中π键与σ键的数量比为
(3)ZnS可用于制白色颜料、玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS的晶胞如图3所示。
①上图中
 的坐标有
的坐标有 、
、 ,与
,与 距离最近的
距离最近的 还有
还有②Zn2+占据
③ZnS的密度为
 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】钽(Ta)和铌(Nb)为高新技术产业的关键元素,其单质的性质相似。一种以花岗伟晶岩型铌钽矿(主要成分为 、
、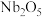 、
、 和少量的FeO、CaO、MgO等)为原料制取钽和铌的流程如图一:
和少量的FeO、CaO、MgO等)为原料制取钽和铌的流程如图一: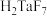 、
、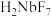 两种二元强酸。
两种二元强酸。
已知:①MIBK为甲基异丁基酮:
② ,
,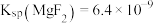 ,
,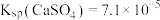 。
。
(1)加快“浸取”速率可采取的措施是______ 。
(2)“浸取”时得到的“浸渣”主要成分为______ (填化学式),“浸取”时还会产生“废气”,“废气”中除了挥发出的HF还可能有______ (填化学式)。 与氢氟酸反应的离子方程式为
与氢氟酸反应的离子方程式为______ 。
(3)“萃取”时,若萃取剂MIBK的量一定,______ (填“一次萃取”或“少量多次萃取”)的萃取效率更高。
(4)用金属钠还原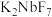 制取金属铌的化学方程式为
制取金属铌的化学方程式为______ 。
(5)钽形成的晶体TaAs在室温下拥有超高的空穴迁移率和较低的电子迁移率。TaAs的晶胞结构如图二所示。诗写出As的配位数:______ 。晶体的密度为______  (列出计算式,阿伏伽德罗常数的值为
(列出计算式,阿伏伽德罗常数的值为 )。
)。
 、
、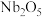 、
、 和少量的FeO、CaO、MgO等)为原料制取钽和铌的流程如图一:
和少量的FeO、CaO、MgO等)为原料制取钽和铌的流程如图一: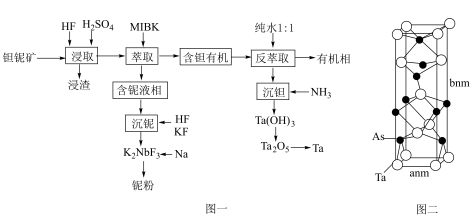
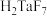 、
、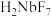 两种二元强酸。
两种二元强酸。已知:①MIBK为甲基异丁基酮:
②
 ,
,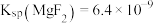 ,
,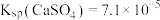 。
。(1)加快“浸取”速率可采取的措施是
(2)“浸取”时得到的“浸渣”主要成分为
 与氢氟酸反应的离子方程式为
与氢氟酸反应的离子方程式为(3)“萃取”时,若萃取剂MIBK的量一定,
(4)用金属钠还原
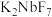 制取金属铌的化学方程式为
制取金属铌的化学方程式为(5)钽形成的晶体TaAs在室温下拥有超高的空穴迁移率和较低的电子迁移率。TaAs的晶胞结构如图二所示。诗写出As的配位数:
 (列出计算式,阿伏伽德罗常数的值为
(列出计算式,阿伏伽德罗常数的值为 )。
)。
您最近一年使用:0次



