元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2,元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)基态X原子核外共有___________ 种运动状态不同的电子,其价电子排布式为___________ 。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是___________ 。
(3)写出一种由第三周期元素组成的与YZ 互为等电子体的分子的电子式:
互为等电子体的分子的电子式:___________ 。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为___________ 。
(1)基态X原子核外共有
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
(3)写出一种由第三周期元素组成的与YZ
 互为等电子体的分子的电子式:
互为等电子体的分子的电子式:(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
更新时间:2022-10-19 10:54:09
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】已知A、B、C、D、E是五种短周期主族元素,C与E同主族,其原子半径与原子序数的关系如图,且A、B、C、D可形成化合物X。回答下列问题:
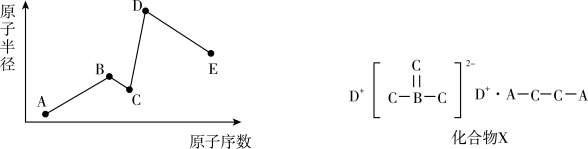
(1)元素E在周期表的位置为第_______ 周期_______ 族,A、B、C、D、E五种元素原子的最外层电子数之和为_______ 。
(2)B、C、E分别形成的最简单氢化物的沸点由高到低的顺序为_______ ;能比较得出B、E的最高价氧化物的水化物酸性强弱的化学反应离子方程式为_______ 。
(3)A、B、C、D、E五种元素中能形成的简单离子中,半径最大的是_______ (填离子符号,下同),半径最小的是_______ 。
(4)C、D形成的一种离子化合物M能与水反应生成C的单质和产物N。M的电子式为_______ ,N中所含有的化学键类型为_______ 。
(5)下列关于化合物X的说法正确的是_______。

(1)元素E在周期表的位置为第
(2)B、C、E分别形成的最简单氢化物的沸点由高到低的顺序为
(3)A、B、C、D、E五种元素中能形成的简单离子中,半径最大的是
(4)C、D形成的一种离子化合物M能与水反应生成C的单质和产物N。M的电子式为
(5)下列关于化合物X的说法正确的是_______。
| A.具有强氧化性 | B.溶于水呈碱性,能促进油污水解 |
C.能使酸性 溶液褪色 溶液褪色 | D.能用于净水,原理与明矾净水相同 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用 Cs2CO3、XO2(X=Si、Ge)和 H3BO3首次合成了组成为 CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si 三种元素电负性由大到小的顺序为_______ ;第一电离能I1(Si) ___ I1(Ge)(填>或<)。
(2)基态Ge 原子简化核外电子排布式为_________ ;SiO2、 GeO2 具有类似的晶体结构, 其中熔点较高的是 __________ , 原因是 _________ 。
(3)如图为硼酸晶体的片层结构,其中硼的杂化方式为____________ 。

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形)。晶胞参数为 apm、b pm、c pm。如图为沿 y 轴投影的晶胞中所有 Cs 原子的分布图和原子分数坐标。CsSiB3O7的摩尔质量为 M g•mol-1,设 NA为阿伏加 德罗常数的值,则CsSiB3O7晶体的密度为_________ g•cm-3(用代数式表示)。

(1)C、O、Si 三种元素电负性由大到小的顺序为
(2)基态Ge 原子简化核外电子排布式为
(3)如图为硼酸晶体的片层结构,其中硼的杂化方式为

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形)。晶胞参数为 apm、b pm、c pm。如图为沿 y 轴投影的晶胞中所有 Cs 原子的分布图和原子分数坐标。CsSiB3O7的摩尔质量为 M g•mol-1,设 NA为阿伏加 德罗常数的值,则CsSiB3O7晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D是四种短周期元素,E是过渡元素,A、B、C同周期,C、D同主族,A原子M层电子数是L层的一半,B是同周期第一电离能最小的元素,C在同周期中未成对电子数最多,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的名称:A__ B___ C ___ D ___
(2)上述五种元素中最高价氧化物对应水化物酸性最强的是(用化学式表示,下同)____ ,碱性最强的是______ 。
(3)D所在周期第一电离能最小的元素是_____ ,电负性最大的元素是_____ 。(填元素符号)
(4)D的氢化物比C的氢化物的沸点__ (填“高”或“低”),原因是 ___________ 。
(5)E元素原子的核电荷数是____ ,E元素在周期表的位置是 _____ ,E元素处于周期表分区中的____ 区。
(6)画出D的核外电子排布图________ ,E的外围电子排布图_________ 。
(7)用电子式表示B的硫化物的形成过程:________________ 。
(1)写出下列元素的名称:A
(2)上述五种元素中最高价氧化物对应水化物酸性最强的是(用化学式表示,下同)
(3)D所在周期第一电离能最小的元素是
(4)D的氢化物比C的氢化物的沸点
(5)E元素原子的核电荷数是
(6)画出D的核外电子排布图
(7)用电子式表示B的硫化物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E、F、G代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素名称为________ 。此元素简单氢化物的空间构型为________ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为________ ,C的基态原子的电子式为_____________________ 。
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为________ ,其基态原子的价电子排布图为_____________________ 。
(4)E为元素周期表前四周期基态原子未成对电子最多的元素,E元素的价电子排布式为_____________ 。
(5)F为33号元素,其基态原子的电子排布式为[Ar]__________________ 。
(6)G元素为第四周期与O同主族的元素,其最高价氧化物对应水化物的化学式为________ ,此物质中G原子的杂化类型为_____________ 。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素名称为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,B的元素符号为
(3)D元素的正三价离子的3d能级为半充满,D的元素符号为
(4)E为元素周期表前四周期基态原子未成对电子最多的元素,E元素的价电子排布式为
(5)F为33号元素,其基态原子的电子排布式为[Ar]
(6)G元素为第四周期与O同主族的元素,其最高价氧化物对应水化物的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题:
(1)A的元素符号为_______ ,D的元素名称为_______ 。
(2)基态B原子中能量最高的电子所在的原子轨道的电子云在空间有_______ 个伸展方向,原子轨道呈_______ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子轨道表示式为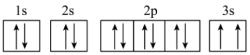 。该同学所写的轨道表示式违反了
。该同学所写的轨道表示式违反了_______ 。
(4)E元素原子核外有_______ 种运动状态不同的电子。
(5)G原子外围电子排布式为_______ 。
(6)检验F元素的方法是_______ 。
| A | 元素原子半径在周期表中最小,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p轨道总电子数比s轨道总电子数少1 |
| C | 元素的第一至第四电离能分别是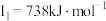 、 、 、 、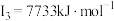 、 、 |
| D | 原子核外所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为4,原子半径在同周期中最小 |
| F | 是前四周期中电负性最小的元素 |
| G | 在周期表的第七列 |
(2)基态B原子中能量最高的电子所在的原子轨道的电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子轨道表示式为
 。该同学所写的轨道表示式违反了
。该同学所写的轨道表示式违反了(4)E元素原子核外有
(5)G原子外围电子排布式为
(6)检验F元素的方法是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】CuO、Cu2S等含铜化合物可以催化合成HCOOH。回答下列问题:
(1)基态铜原子的价电子排布式为___________ ,其核外电子占据的原子轨道共有___________ 个。
(2)HCOOH中元素电负性从大到小的顺序为___________ ;催化过程中可能产生 ,
, 的空间构型为
的空间构型为___________ ,碳氧键的平均键长 比CH3OH要
比CH3OH要___________ (填“长”或“短”);在有机溶剂中,H2SO4的电离平衡常数Ka1(H2SO4)比H2CO3的电离平衡常数Ka1(H2CO3)大,除S的非金属性比C强外,在分子结构上还存在的原因是___________ 。
(3)已知Cu2S晶胞中S2-的位置如图所示,Cu+位于S2-所构成的正四面体中心。
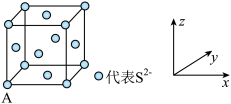
S2-配位数为___________ ;已知图中A处(S2-)的原子分数坐标为(0,0,0),则晶胞中与A距离最近的Cu+的原子分数坐标为___________ ;若晶胞参数anm,晶体的密度为dg·cm-3,则阿伏加德罗常数的值为___________ (用含a和d的式子表示)。
(1)基态铜原子的价电子排布式为
(2)HCOOH中元素电负性从大到小的顺序为
 ,
, 的空间构型为
的空间构型为 比CH3OH要
比CH3OH要(3)已知Cu2S晶胞中S2-的位置如图所示,Cu+位于S2-所构成的正四面体中心。

S2-配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】钛酸钙是最典型的钙钛矿型化合物,该类化合物具有特殊的理化性质。
(1)基态 的核外电子排布式为
的核外电子排布式为_______________ 。
(2)氧原子核外电子有__________ 种空间运动状态。比较离子半径大小
___________ 
(3)关于钛元素下列说法不正确的是________
(4)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
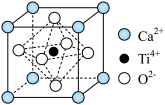
①钛酸钙的晶胞如图所示,1个晶胞中含有 的个数是
的个数是____________
1个 周围等距且最近的
周围等距且最近的 有
有_________ 个。
②已知,钛酸钙晶体的晶胞形状为立方体,其棱长为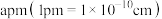 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
__________  (列出计算式)。
(列出计算式)。
(5)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。
① 中
中 的杂化方式为
的杂化方式为________________ 。
②请从化学键的角度解释由甲胺形成 的过程:
的过程:_______________ 。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氧原子核外电子有


(3)关于钛元素下列说法不正确的是________
A.钛原子的原子轨道能量: |
| B.在钛的电子云图中,用小黑点表示绕核做高速圆周运动的电子 |
C.钛原子中,电子从 的状态跃迁到 的状态跃迁到 的状态时,将释放能量 的状态时,将释放能量 |
| D.钛在周期表中的位置是第四周期第IB族 |
(4)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①钛酸钙的晶胞如图所示,1个晶胞中含有
 的个数是
的个数是1个
 周围等距且最近的
周围等距且最近的 有
有
②已知,钛酸钙晶体的晶胞形状为立方体,其棱长为
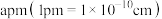 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
 (列出计算式)。
(列出计算式)。(5)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物
 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。①
 中
中 的杂化方式为
的杂化方式为②请从化学键的角度解释由甲胺形成
 的过程:
的过程:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】2015年10月中国药学家屠呦呦因发现青蒿素(一种用于治疗疟疾的药物)而获得诺贝尔生理医学奖。青蒿素(C15H22O5)的结构如图所示。请回答下列问题:
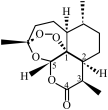
(1)组成青蒿素的三种元素电负性由小到大排序是_____ ,在基态O原子中,核外存在_____ 对自旋相反的电子。
(2)下列关于青蒿素的说法正确的是_____ (填序号)。
a.青蒿素中既存在极性键又存在非极性键
b.在青蒿素分子中,所有碳原子均采取sp3杂化
c.图中数字标识的五个碳原子均只以σ键与其它原子成键
(3)在确定青蒿素结构的过程中,可采用NaBH4作为还原剂,其制备方法为:4NaH+B(OCH3)→3NaBH4+3CH3ONa
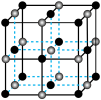
①NaH为_____ 晶体,如图是NaH晶胞结构,则NaH晶体的配位数是_____ ,若晶胞棱长为a,则Na原子最小核间距为_____ 。
②B(OCH3)3中B采用的杂化类型是_____ 。写出两个与B(OCH3)3具有相同空间构型的分子或离子_____ 。
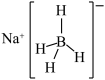
③NaBH4结构如图所示,结构中存在的化学键类型有_____ 。

(1)组成青蒿素的三种元素电负性由小到大排序是
(2)下列关于青蒿素的说法正确的是
a.青蒿素中既存在极性键又存在非极性键
b.在青蒿素分子中,所有碳原子均采取sp3杂化
c.图中数字标识的五个碳原子均只以σ键与其它原子成键
(3)在确定青蒿素结构的过程中,可采用NaBH4作为还原剂,其制备方法为:4NaH+B(OCH3)→3NaBH4+3CH3ONa
①NaH为

②B(OCH3)3中B采用的杂化类型是
③NaBH4结构如图所示,结构中存在的化学键类型有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】I.工业中可利用生产钛白的副产物FeSO4·7H2O和硫铁矿(FeS2)联合制备铁精粉(FexOy)和硫酸,实现能源及资源的有效利用。
(1)FeSO4·7H2O结构示意图如图:
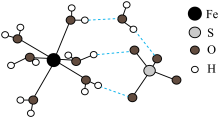
①Fe2+的价层电子排布式为_____ 。
②H2O中O和SO 中S均为sp3杂化,比较H2O中H-O-H键角和SO
中S均为sp3杂化,比较H2O中H-O-H键角和SO 中O-S-O键角的大小并解释原因
中O-S-O键角的大小并解释原因____ 。
③FeSO4·7H2O中H2O与Fe2+、H2O与SO 的作用力类型分别是
的作用力类型分别是_____ 。
(2)FeS2晶体的晶胞形状为立方体,边长为anm,结构如图:
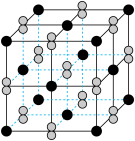
①Fe2+的配位数_____ 个。
②FeS2的摩尔质量为120g·mol-1,阿伏加德罗常数为NA,晶体的密度为_____ g•cm-3。(1nm=10—9m)
Ⅱ.四氟肼(N2F4)可作高能燃料的氧化剂,可用Fe3+与二氟胺(HNF2)反应制得,发生的反应是2HNF2+2Fe3+=N2F4↑+2Fe2++2H+,请回答有关问题:
(3)F原子最外层电子排布式_____ ;N原子核外不同运动状态的电子有_____ 种;N2的电子式_____ ;F元素的非金属性比N强,用原子结构的知识说明理由:_____ 。
(4)HNF2中N元素的化合价是_____ ;反应中氧化剂与还原剂的物质的量之比为_____ ;若生成0.1molN2F4,电子转移数是____ 。
(1)FeSO4·7H2O结构示意图如图:

①Fe2+的价层电子排布式为
②H2O中O和SO
 中S均为sp3杂化,比较H2O中H-O-H键角和SO
中S均为sp3杂化,比较H2O中H-O-H键角和SO 中O-S-O键角的大小并解释原因
中O-S-O键角的大小并解释原因③FeSO4·7H2O中H2O与Fe2+、H2O与SO
 的作用力类型分别是
的作用力类型分别是(2)FeS2晶体的晶胞形状为立方体,边长为anm,结构如图:

①Fe2+的配位数
②FeS2的摩尔质量为120g·mol-1,阿伏加德罗常数为NA,晶体的密度为
Ⅱ.四氟肼(N2F4)可作高能燃料的氧化剂,可用Fe3+与二氟胺(HNF2)反应制得,发生的反应是2HNF2+2Fe3+=N2F4↑+2Fe2++2H+,请回答有关问题:
(3)F原子最外层电子排布式
(4)HNF2中N元素的化合价是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铜、银、金与社会生活联系密切。
(1) 在周期表中, 铜、银、金位于同一族,它们基态原子的外围电子排布式的通式为__________________ (用n表示电子层数),它们位于元素周期表的________ 区。
(2)化学上,银氨溶液可以检验醛基的存在,例如:CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag↓+3NH3
CH3COONH4+2Ag↓+3NH3
+H2O。1个CH3CHO分子中所含π键的数目为________ ,碳原子的杂化轨道类型为________ ;CH3CH2OH、CH3CHO的相对分子质量仅相差2,但沸点相差很大(分别为78.5℃,20.8℃),其主要原因是________________________ ;NH3的VSEPR模型为________ 。
(3)金不溶于硝酸,但溶于“王水”,发生反应:Au+4HCl+HNO3=H[AuCl4]+NO↑+2H2O。金溶于王水的主要原因是形成了[AuCl4],提高了金的活动性。在[AuCl4]-中,金离子的配位数为________ ,画出该配离子的结构式:________ 。
(4)金、银、铜都有良好的延展性,解释其原因:________________________________ 。
(5)金、银的一种合金具有较强的储氢能力。该合金的晶胞为面心立方结构,银原子位于面心,金原子位于顶点。若该晶胞边长为anm,金、银原子的半径分别为bnm、cnm。则该晶胞的空间利用率(φ)
为________ (用含a、b、c和圆周率π的式子表示 )。
(1) 在周期表中, 铜、银、金位于同一族,它们基态原子的外围电子排布式的通式为
(2)化学上,银氨溶液可以检验醛基的存在,例如:CH3CHO+2Ag(NH3)2OH
 CH3COONH4+2Ag↓+3NH3
CH3COONH4+2Ag↓+3NH3+H2O。1个CH3CHO分子中所含π键的数目为
(3)金不溶于硝酸,但溶于“王水”,发生反应:Au+4HCl+HNO3=H[AuCl4]+NO↑+2H2O。金溶于王水的主要原因是形成了[AuCl4],提高了金的活动性。在[AuCl4]-中,金离子的配位数为
(4)金、银、铜都有良好的延展性,解释其原因:
(5)金、银的一种合金具有较强的储氢能力。该合金的晶胞为面心立方结构,银原子位于面心,金原子位于顶点。若该晶胞边长为anm,金、银原子的半径分别为bnm、cnm。则该晶胞的空间利用率(φ)
为
您最近一年使用:0次
【推荐2】回答下列问题:
Ⅰ.(1)基态氮原子最外层有___________ 种能量不同的电子。
(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是___________ (填编号)。
a.NH3比PH3稳定性强
b.Na3PO4溶液与HNO3反应生成H3PO4
c.硝酸显强氧化性,磷酸不显强氧化性
d.氮气常温是气体,磷单质是固体
II.镁、钙和锶(Sr)都属于碱土金属,具有相似的化学性质。
(3)颗粒状的单质锶与稀硫酸反应,反应现象不如钠和水反应剧烈,原因是___________ 。
(4)锶在一定条件下分别与N2、H2发生反应,生成Y、Z两种锶的固态化合物,Y、Z与水反应均可放出气体。0.01 mol Y溶于100 mL盐酸恰好完全反应生成氯化物混合溶液, 则盐酸的物质的量浓度为___________ ,Z的电子式为___________ 。
III.Fe、Ni是两种重要的过渡金属元素
(5)基态Ni原子中,电子占据的最高能层符号为___________ ,同周期元素中基态原子未成对电子数与Ni相同的元素名称为___________ 。
(6)Fe3+与酚类物质的显色反应常用于其离子检验,已知 Fe3+遇邻苯二酚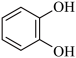 )和对苯二酚
)和对苯二酚 )均显绿色。邻苯二酚的熔沸点比对苯二酚
)均显绿色。邻苯二酚的熔沸点比对苯二酚___________ (填“高”或“低”), 原因是___________ 。
Ⅰ.(1)基态氮原子最外层有
(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是
a.NH3比PH3稳定性强
b.Na3PO4溶液与HNO3反应生成H3PO4
c.硝酸显强氧化性,磷酸不显强氧化性
d.氮气常温是气体,磷单质是固体
II.镁、钙和锶(Sr)都属于碱土金属,具有相似的化学性质。
(3)颗粒状的单质锶与稀硫酸反应,反应现象不如钠和水反应剧烈,原因是
(4)锶在一定条件下分别与N2、H2发生反应,生成Y、Z两种锶的固态化合物,Y、Z与水反应均可放出气体。0.01 mol Y溶于100 mL盐酸恰好完全反应生成氯化物混合溶液, 则盐酸的物质的量浓度为
III.Fe、Ni是两种重要的过渡金属元素
(5)基态Ni原子中,电子占据的最高能层符号为
(6)Fe3+与酚类物质的显色反应常用于其离子检验,已知 Fe3+遇邻苯二酚
 )和对苯二酚
)和对苯二酚 )均显绿色。邻苯二酚的熔沸点比对苯二酚
)均显绿色。邻苯二酚的熔沸点比对苯二酚
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+比B-少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为 40%,且其核内质子数等于中子数。化合物R是由A、D两元素形成的离子化合物,其中A+阳离子与Dn-阴离子数之比为2∶1。请回答下列问题:
(1)B-的电子排布式为______________ ,在CB3分子中C元素原子的原子轨道发生的是______ 杂化。
(2)C的氢化物的空间构型为________________ ,其氢化物在同族元素所形成的氢化物中沸点最高的原因是__________________________________________________________ 。
(3)B元素的电负性____ D元素的电负性(填“>”、“<”或“=”),用一个 化学方程式说明B、D两元素形成的单质的氧化性强弱:________________________________ 。
(4)如图所示是R形成的晶体的晶胞,设晶胞的棱长为a cm。 试计算R晶体的密度为_________________ 。(阿伏伽德罗常数用NA表示)

(1)B-的电子排布式为
(2)C的氢化物的空间构型为
(3)B元素的电负性
(4)如图所示是R形成的晶体的晶胞,设晶胞的棱长为a cm。 试计算R晶体的密度为

您最近一年使用:0次



