为比较Fe3+和Cu2+对H2O2分解的催化效果,某体学研究小组的同学分别设计了图甲、乙所示的实验。请回答相关问题:

(1)定性比较:图甲可通过观察_____ ,定性比较得出结论。有同学提出将CuSO4改为CuCl2更合理一些,其理由是______ 。
(2)定量比较:如图乙所示,实验时均以生成40 mL气体为标准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是________ ,实验中需要测量的数据是_______ 。
(3)将0.10 mol MnO2粉末加入到50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。

①写出H2O2在MnO2作用下发生反应的化学方程式:_______ 。
②H2O2的初始物质的量浓度为________ 。(保留两位有效数字)

(1)定性比较:图甲可通过观察
(2)定量比较:如图乙所示,实验时均以生成40 mL气体为标准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是
(3)将0.10 mol MnO2粉末加入到50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。

①写出H2O2在MnO2作用下发生反应的化学方程式:
②H2O2的初始物质的量浓度为
更新时间:2020-07-03 21:52:35
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】(l)在下列事实中,什么因素影响了化学反应的速率?
①熔融的KClO3放出气泡很慢,撒入少量MnO2很快产生气体______ ;
②同浓度、同体积的盐酸中放入同样大小的锌粒和镁粒,产生气体有快有慢______ ;
③KI晶体和HgCl2晶体混合后无明显现象,若一起投入水中,很快生成红色HgI2______ ;
(2)某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。限选试剂:1.00 mol/LHNO3、2.00 mol/LHNO3,细颗粒大理石、粗颗粒大理石,35℃水浴。
①请根据能进行的探究内容,填写以下实验设计表,完成探究实验:
②整个实验中应控制的不变量是硝酸溶液体积和______ 。
③该实验小组用如右图实验装置进行实验。

a.除电子天平、干燥管、锥形瓶、药匙、胶塞等仪器外,必需的实验仪器还有______ 。
b.若反应开始时电子天平读数为100.00g,经2分钟反应结束时的读数为95.60g,则这两分钟内用CaCO3来表示的速率为_____ g/min。
c.若撤除干燥管装置,所测速率______ (填“偏大”、“偏小”或“不变”)。
①熔融的KClO3放出气泡很慢,撒入少量MnO2很快产生气体
②同浓度、同体积的盐酸中放入同样大小的锌粒和镁粒,产生气体有快有慢
③KI晶体和HgCl2晶体混合后无明显现象,若一起投入水中,很快生成红色HgI2
(2)某探究小组用测量HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。限选试剂:1.00 mol/LHNO3、2.00 mol/LHNO3,细颗粒大理石、粗颗粒大理石,35℃水浴。
①请根据能进行的探究内容,填写以下实验设计表,完成探究实验:
| 实验编号 | T℃ | 大理石规格 | HNO3浓度(mol/L) |
| A | 常温 | 2.00 | |
| B | 粗颗粒 | 1.00 | |
| C | 粗颗粒 | 2.00 | |
| D | 细颗粒 | 2.00 |
③该实验小组用如右图实验装置进行实验。

a.除电子天平、干燥管、锥形瓶、药匙、胶塞等仪器外,必需的实验仪器还有
b.若反应开始时电子天平读数为100.00g,经2分钟反应结束时的读数为95.60g,则这两分钟内用CaCO3来表示的速率为
c.若撤除干燥管装置,所测速率
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】H2O2作为氧化剂在反应时不产生污染物被称为绿色氧化剂,因而受到人们越来越多的关注。为比较Fe3+和Cu2+对H2O2(2%和5%两种浓度)分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答下列问题:
(1)定性分析:图甲可通过观察_______ 定性比较得出结论。有同学提出将FeCl3溶液改为Fe2(SO4)3溶液更合理,其理由是_______ 。

(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为______ ,检查该装置气密性的方法是:关闭A的活塞,将注射器活塞向外拉出一段后松手,过一段时间后看______ ,实验中需要测量的数据是______ 。
(3)加入MnO2粉末于H2O2溶液中,在标准状况下放出气体的体积和时间的关系如丙图所示。由D到A过程中,随着反应的进行反应速率逐渐______ (填“加快”或“减慢”),其变化的原因是______ 。(选填字母编号)

A.改变了反应的活化能
B.改变活化分子百分比
C.改变了反应途径
D.改变单位体积内的分子总数
(4)另一小组同学为了研究浓度对反应速率的影响,设计了如下实验设计方案,请帮助完成(所有空均需填满)。
可得到的结论是浓度越大,H2O2分解速率越快。
(1)定性分析:图甲可通过观察

(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为
(3)加入MnO2粉末于H2O2溶液中,在标准状况下放出气体的体积和时间的关系如丙图所示。由D到A过程中,随着反应的进行反应速率逐渐

A.改变了反应的活化能
B.改变活化分子百分比
C.改变了反应途径
D.改变单位体积内的分子总数
(4)另一小组同学为了研究浓度对反应速率的影响,设计了如下实验设计方案,请帮助完成(所有空均需填满)。
| 实验编号 | T/K | 催化剂 | 浓度 |
| 实验1 | 298 | 3滴FeCl3溶液 | 10mL2%H2O2 |
| 实验2 | 298 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。实验药品:铜、铁、镁、0.5 mol • L-1H2SO4溶液、2 mol • L-1 H2SO4溶液。甲同学研究的实验报告如下表∶
(1) 甲同学表中实验步骤②为______________________ 。
(2) 甲同学的实验目的是__________________________ 。
要得出正确的实验结论,还需要控制的实验条件是_____________ 。
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行实验∶
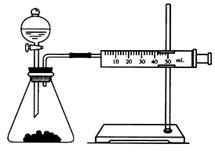
(3)乙同学在实验中应该测定的数据是_________________ 。
(4)乙同学完成该实验应选用的实验药品是________________ 。
| 实验步骤 | 现象 | 结论 |
| 分别取等体积的2 mol • L-1 的硫酸溶液于三支试管中 ②______________________ | 反应速率∶ 镁>铁,铜不反应 | 金属的性质越活泼,反应速率越快 |
(2) 甲同学的实验目的是
要得出正确的实验结论,还需要控制的实验条件是
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行实验∶

(3)乙同学在实验中应该测定的数据是
(4)乙同学完成该实验应选用的实验药品是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】在绿色低碳技术的研发体系中,实现 的减排和利用技术日益受到重视。回答下列问题:
的减排和利用技术日益受到重视。回答下列问题:
(1)RWGS反应 △H可实现
△H可实现 的减排。已知:部分化学键的键能如表所示:
的减排。已知:部分化学键的键能如表所示:
则
_________  ,该反应的正活化能和逆活化能中较大的是
,该反应的正活化能和逆活化能中较大的是_________ (填“正活化能”或“逆活化能”)。
(2)甲烷化反应:
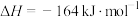 可有效降低空气中的含量。已知
可有效降低空气中的含量。已知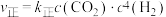 ,
, (
( 、
、 分别为正逆反应的速率常数)。
分别为正逆反应的速率常数)。
①加入催化剂,该反应 的将
的将_________ (填“增大”“减小”或“不变”)。
②实验测得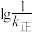 、
、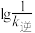 随温度变化的曲线如图所示,则表示
随温度变化的曲线如图所示,则表示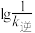 随温度变化的曲线为
随温度变化的曲线为_________ (填“L1或L2”),原因为_________ 。

(3)科学家将甲烷化反应设计成如图的原电池装置来实现 的减排和利用。
的减排和利用。

电极A为原电池的_________ (填“正极”或“负极”),该电极的反应式为_________ 。
 的减排和利用技术日益受到重视。回答下列问题:
的减排和利用技术日益受到重视。回答下列问题:(1)RWGS反应
 △H可实现
△H可实现 的减排。已知:部分化学键的键能如表所示:
的减排。已知:部分化学键的键能如表所示:| 化学键 |  | C=O | C-H | H-H | O-H |
| 键能(kJ/mol) | 997 | 800 | 414 | 436 | 499 |

 ,该反应的正活化能和逆活化能中较大的是
,该反应的正活化能和逆活化能中较大的是(2)甲烷化反应:

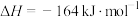 可有效降低空气中的含量。已知
可有效降低空气中的含量。已知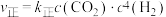 ,
, (
( 、
、 分别为正逆反应的速率常数)。
分别为正逆反应的速率常数)。①加入催化剂,该反应
 的将
的将②实验测得
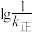 、
、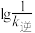 随温度变化的曲线如图所示,则表示
随温度变化的曲线如图所示,则表示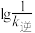 随温度变化的曲线为
随温度变化的曲线为
(3)科学家将甲烷化反应设计成如图的原电池装置来实现
 的减排和利用。
的减排和利用。
电极A为原电池的
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】设计实验测定锌与硫酸反应的速率,按下列实验步骤完成实验:

①按图示安装装置,加入锌粒,然后快速加入40mL1mol/L的硫酸溶液,测量收集10mLH2所用的时间。
②按图示再安装一套装置,加入与前一套装置相同的锌粒,然后再快速加入40mL4mol/L的硫酸溶液,测量收集10mLH2所用的时间。
回答下列问题:
(1)实验所用仪器有:锥形瓶、双孔塞、分液漏斗、直角导气管、50mL注射器、铁架台、________ 。
(2)观察到的现象是:____________________________________ ;
收集10mL气体②所用时间比①所用时间________ 。
(3)所能得出的实验结论是:_________________________________ 。
(4)若在①实验中加入适量MnO2,则:________
A.如果①比②速率慢,则证明MnO2无催化作用
B.如果①比②速率快,则不能证明MnO2有无催化作用
C.如果①比②速率慢,则不能证明MnO2有无催化作用
D.如果①比②速率快,则证明MnO2有催化作用

①按图示安装装置,加入锌粒,然后快速加入40mL1mol/L的硫酸溶液,测量收集10mLH2所用的时间。
②按图示再安装一套装置,加入与前一套装置相同的锌粒,然后再快速加入40mL4mol/L的硫酸溶液,测量收集10mLH2所用的时间。
回答下列问题:
(1)实验所用仪器有:锥形瓶、双孔塞、分液漏斗、直角导气管、50mL注射器、铁架台、
(2)观察到的现象是:
收集10mL气体②所用时间比①所用时间
(3)所能得出的实验结论是:
(4)若在①实验中加入适量MnO2,则:
A.如果①比②速率慢,则证明MnO2无催化作用
B.如果①比②速率快,则不能证明MnO2有无催化作用
C.如果①比②速率慢,则不能证明MnO2有无催化作用
D.如果①比②速率快,则证明MnO2有催化作用
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】氮是自然界各种生物体生命活动不可缺少的重要元素。
(1)下列说法中,不正确的是___________ (填字母序号)。
a.氮原子的最外层有5个电子,氮气分子中存在氮氮三键,常温下化学性质稳定
b.氮元素位于元素周期表的第二周期,第VA族
c.氮元素的最低化合价为-3价,最高化合价为+5价
d.根据元素周期律推测,氮化硅的化学式为SiN
(2)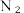 分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是
分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是 (铵根离子),将
(铵根离子),将 转化为
转化为  需与
需与___________ (填“酸”或“碱”)反应。写出该反应离子方程式:___________ 和 的电子式
的电子式___________ 。
(3)大自然通过闪电可将空气中的氮气转化为含氮化合物,从而实现自然固氮。该过程中生成的含氮化合物是___________ 。
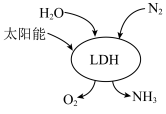
(4)我国科研团队借助一种固体催化剂(LDH),在常温常压和可见光作用下实现了人工固氮。其过程如图所示。写出该过程中反应的化学方程式:___________ 。___________ 。
(6)上述流程中,需要使用催化剂的反应是___________ (填“Ⅰ”、“Ⅱ”或“Ⅲ”),使用催化剂的目的是___________ 。
(7)工业合成氨反应为: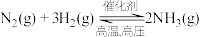 对其描述正确的是___________(填序号)。
对其描述正确的是___________(填序号)。
(8)采用上述工业制硝酸的流程,若 (已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
(已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为___________ g。
(1)下列说法中,不正确的是
a.氮原子的最外层有5个电子,氮气分子中存在氮氮三键,常温下化学性质稳定
b.氮元素位于元素周期表的第二周期,第VA族
c.氮元素的最低化合价为-3价,最高化合价为+5价
d.根据元素周期律推测,氮化硅的化学式为SiN
(2)
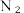 分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是
分子不能被大多数动植物直接吸收。植物吸收和利用效果最好的是 (铵根离子),将
(铵根离子),将 转化为
转化为  需与
需与 的电子式
的电子式(3)大自然通过闪电可将空气中的氮气转化为含氮化合物,从而实现自然固氮。该过程中生成的含氮化合物是
(4)我国科研团队借助一种固体催化剂(LDH),在常温常压和可见光作用下实现了人工固氮。其过程如图所示。写出该过程中反应的化学方程式:
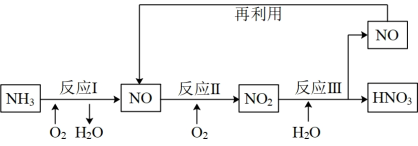
(6)上述流程中,需要使用催化剂的反应是
(7)工业合成氨反应为:
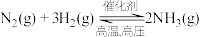 对其描述正确的是___________(填序号)。
对其描述正确的是___________(填序号)。A.在上述条件下,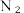 能全部转化为 能全部转化为 |
| B.若其他条件一定时,增大氮气的浓度,可增大反应速率 |
| C.达到平衡时,体系中各物质的浓度一定相等 |
| D.当正反应速率等于逆反应速率且不为零时,该反应达到平衡状态 |
(8)采用上述工业制硝酸的流程,若
 (已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
(已折算成标准状况的气体体积)完全反应生成硝酸,理论上生成硝酸的质量为
您最近一年使用:0次
【推荐1】某废旧金属材料中主要含  和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收
和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收 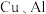 并制取绿矾等。回答下列问题:
并制取绿矾等。回答下列问题:___________ 。
(2)碱浸时 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(3)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是___________ 。
(4)加入试剂 后可能发生的反应有
后可能发生的反应有___________ 个,这些反应中属于化合反应的离子方程式为___________ 。
(5)滤液Ⅱ经过结晶法制取绿矾晶体,绿矾在空气中容易被部分氧化。现取被部分氧化的绿矾晶体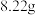 溶于蒸馏水后,加入足量的
溶于蒸馏水后,加入足量的  溶液,过滤得沉淀
溶液,过滤得沉淀 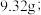 再通入
再通入  (标准状况)氯气恰好将其中的
(标准状况)氯气恰好将其中的  完全氧化。
完全氧化。
①为确定绿矾未被全部氧化,可选择的最佳试剂是___________ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液
②操作Ⅱ为___________ 。
③通过计算推测晶体中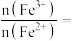
___________ 。
 和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收
和可燃性有机物,为节约和充分利用资源,通过如下工艺流程回收 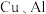 并制取绿矾等。回答下列问题:
并制取绿矾等。回答下列问题: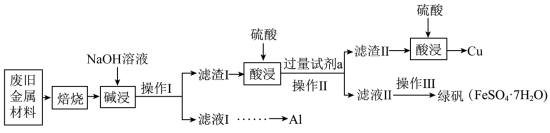
(2)碱浸时
 发生反应的化学方程式为
发生反应的化学方程式为(3)操作Ⅰ、Ⅱ中使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是
(4)加入试剂
 后可能发生的反应有
后可能发生的反应有(5)滤液Ⅱ经过结晶法制取绿矾晶体,绿矾在空气中容易被部分氧化。现取被部分氧化的绿矾晶体
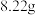 溶于蒸馏水后,加入足量的
溶于蒸馏水后,加入足量的  溶液,过滤得沉淀
溶液,过滤得沉淀 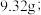 再通入
再通入  (标准状况)氯气恰好将其中的
(标准状况)氯气恰好将其中的  完全氧化。
完全氧化。①为确定绿矾未被全部氧化,可选择的最佳试剂是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液 D.
溶液 D. 溶液
溶液②操作Ⅱ为
③通过计算推测晶体中
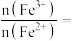
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】七水合硫酸亚铁(FeSO4•7H2O)在医学上常用作补血剂,某课外小组通过以下实验方法测定某补血剂中亚铁离子的含量。
步骤1:取10片补血剂样品除去糖衣,研磨,溶解,过滤。将滤液配成250mL溶液。
步骤2:取上述溶液25.00mL于锥形瓶中,逐滴加入0.0100mol•L-1酸性KMnO4溶液至恰好完全反应,消耗KMnO4溶液20.00mL。(假定药品中其他成分不与KMnO4反应)
已知:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O
请回答:
(1)步骤1中配制溶液时需要的玻璃仪器除250mL容量瓶,烧杯、玻璃棒外,还需要____ 。
(2)配制溶液操作中,若定容、摇匀后发现溶液体积低于刻度线,则测得的补血剂中亚铁离子的含量____ (“偏高”、“偏低”“无影响”);若定容时俯视,则测得的补血剂中亚铁离子的含量____ (“偏高”、“偏低”“无影响”)。
(3)该补血剂中亚铁离子的含量为____ mg/片。
步骤1:取10片补血剂样品除去糖衣,研磨,溶解,过滤。将滤液配成250mL溶液。
步骤2:取上述溶液25.00mL于锥形瓶中,逐滴加入0.0100mol•L-1酸性KMnO4溶液至恰好完全反应,消耗KMnO4溶液20.00mL。(假定药品中其他成分不与KMnO4反应)
已知:MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O
请回答:
(1)步骤1中配制溶液时需要的玻璃仪器除250mL容量瓶,烧杯、玻璃棒外,还需要
(2)配制溶液操作中,若定容、摇匀后发现溶液体积低于刻度线,则测得的补血剂中亚铁离子的含量
(3)该补血剂中亚铁离子的含量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】氨基甲酸铵(NH2COONH4)为白色粉末,易溶于水,难溶于CCl4,水解生成NH4HCO3,受热分解生成CO(NH2)2,是一种优良的氨化剂,其工业制取原理为2NH3(g) +CO2(g) NH2COONH4 (s) ΔH<0。某化学小组模拟工业原理制备少量NH2COONH4,实验装置(夹持仪器及冷却装置已省略)如图所示。
NH2COONH4 (s) ΔH<0。某化学小组模拟工业原理制备少量NH2COONH4,实验装置(夹持仪器及冷却装置已省略)如图所示。

回答下列问题:
(1)装置Ⅰ中胶皮管a的作用为___________ ,仪器 b中发生反应的离子方程式为___________ 。
(2)装置Ⅱ中盛放的试剂为___________ ,若某同学实验时忘记安装装置V,其导致的后果是___________ 。
(3)装置Ⅳ可采取的冷却方式为___________ ,若没有冷却装置会导致氨基甲酸铵的产量降低,其原因是___________ 。
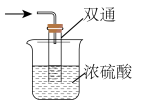
(4)尾气处理装置如图所示,浓硫酸的作用是___________ 。
(5)测量氨基甲酸铵样品的纯度:称取含有NH4HCO3的NH2COONH4样品0.782g,用足量石灰水充分处理后,使碳元素完全转化为CaCO3,过滤、洗涤、干燥,所得固体的质量为1. 000 g。则样品中NH2COONH4的纯度为___________ (保留三位有效数字)。
 NH2COONH4 (s) ΔH<0。某化学小组模拟工业原理制备少量NH2COONH4,实验装置(夹持仪器及冷却装置已省略)如图所示。
NH2COONH4 (s) ΔH<0。某化学小组模拟工业原理制备少量NH2COONH4,实验装置(夹持仪器及冷却装置已省略)如图所示。
回答下列问题:
(1)装置Ⅰ中胶皮管a的作用为
(2)装置Ⅱ中盛放的试剂为
(3)装置Ⅳ可采取的冷却方式为
(4)尾气处理装置如图所示,浓硫酸的作用是

(5)测量氨基甲酸铵样品的纯度:称取含有NH4HCO3的NH2COONH4样品0.782g,用足量石灰水充分处理后,使碳元素完全转化为CaCO3,过滤、洗涤、干燥,所得固体的质量为1. 000 g。则样品中NH2COONH4的纯度为
您最近一年使用:0次



