影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。实验药品:铜、铁、镁、0.5 mol • L-1H2SO4溶液、2 mol • L-1 H2SO4溶液。甲同学研究的实验报告如下表∶
(1) 甲同学表中实验步骤②为______________________ 。
(2) 甲同学的实验目的是__________________________ 。
要得出正确的实验结论,还需要控制的实验条件是_____________ 。
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行实验∶
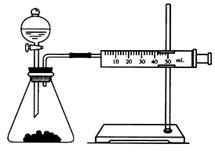
(3)乙同学在实验中应该测定的数据是_________________ 。
(4)乙同学完成该实验应选用的实验药品是________________ 。
| 实验步骤 | 现象 | 结论 |
| 分别取等体积的2 mol • L-1 的硫酸溶液于三支试管中 ②______________________ | 反应速率∶ 镁>铁,铜不反应 | 金属的性质越活泼,反应速率越快 |
(2) 甲同学的实验目的是
要得出正确的实验结论,还需要控制的实验条件是
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行实验∶

(3)乙同学在实验中应该测定的数据是
(4)乙同学完成该实验应选用的实验药品是
更新时间:2016-12-09 00:30:02
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
【推荐1】在一定条件下发生反应: 可以缓解大气中CO、NO污染问题。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如下表所示。
可以缓解大气中CO、NO污染问题。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如下表所示。
回答下列问题:
(1)控制变量是科学研究的重要方法,因此表中数据:
_______ ,
_______ 。
(2)对比实验Ⅰ、Ⅲ的目的是_______ 。
(3)实验Ⅰ和实验Ⅱ中,NO的物质的量浓度 随时间
随时间 的变化曲线如图所示。
的变化曲线如图所示。

①根据图像可以得出的结论是_______ 。
②实验Ⅱ中,NO的平衡转化率为_______ %。
(4)瑞典ASES公司设计的常用于驱动潜艇的液氨-液氧环保燃料电池如图所示。该燃料电池工作时,正极为电极_______ (填“1”或“2”,下同), 向电极
向电极_______ 移动。

 可以缓解大气中CO、NO污染问题。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如下表所示。
可以缓解大气中CO、NO污染问题。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,如下表所示。| 实验编号 |  |  初始浓度 初始浓度 |  初始浓度 初始浓度 | 催化剂的比表面积 |
| Ⅰ | 280 |  | 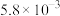 | 82 |
| Ⅱ | 280 |  |  | 124 |
| Ⅲ | 350 |  | 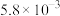 | 82 |
(1)控制变量是科学研究的重要方法,因此表中数据:


(2)对比实验Ⅰ、Ⅲ的目的是
(3)实验Ⅰ和实验Ⅱ中,NO的物质的量浓度
 随时间
随时间 的变化曲线如图所示。
的变化曲线如图所示。
①根据图像可以得出的结论是
②实验Ⅱ中,NO的平衡转化率为
(4)瑞典ASES公司设计的常用于驱动潜艇的液氨-液氧环保燃料电池如图所示。该燃料电池工作时,正极为电极
 向电极
向电极
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】已知NO2和N2O4之间发生可逆反应:2NO2(g)(红棕色) N2O4(g)(无色)
N2O4(g)(无色)
(1)在烧瓶A和B中盛有相同浓度的NO2与N2O4的混合气体,中间用止水夹夹紧,浸入到盛有水的烧杯中,如图所示。分别向两个烧杯中加入浓硫酸和NH4NO3 固体,观察到的现象是:A中颜色加深,说明该反应的正反应为__________ 反应(填吸热、放热);B中现象为:________________________ 。

(2)下图1是在一定温度下,某固定容积的密闭容器中充入一定量的NO2气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确 的是_____________
a.t1时,反应未达到平衡,NO2浓度在减小
b.t2时,反应达到平衡,反应不再进行
c.t2~t3,各物质浓度不再变化
d.t2~t3,各物质的浓度相等

(3)某容积2L的密闭容器中充入一定量的NO2和N2O4的混合气体,在一定温度压强下,两者物质的量随时间变化如图2所示。
① 表示NO2变化的曲线是_______________________ (填“X”或“Y”)。
② 在0到1 min内用Y的浓度变化表示的该反应的反应速率是_________ mol·L-1·min-1
 N2O4(g)(无色)
N2O4(g)(无色)(1)在烧瓶A和B中盛有相同浓度的NO2与N2O4的混合气体,中间用止水夹夹紧,浸入到盛有水的烧杯中,如图所示。分别向两个烧杯中加入浓硫酸和NH4NO3 固体,观察到的现象是:A中颜色加深,说明该反应的正反应为

(2)下图1是在一定温度下,某固定容积的密闭容器中充入一定量的NO2气体后,反应速率(v)与时间(t)的关系曲线。下列叙述
a.t1时,反应未达到平衡,NO2浓度在减小
b.t2时,反应达到平衡,反应不再进行
c.t2~t3,各物质浓度不再变化
d.t2~t3,各物质的浓度相等

(3)某容积2L的密闭容器中充入一定量的NO2和N2O4的混合气体,在一定温度压强下,两者物质的量随时间变化如图2所示。
① 表示NO2变化的曲线是
② 在0到1 min内用Y的浓度变化表示的该反应的反应速率是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)⇌2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________ 。
(2)反应前A的物质的量浓度是________ 。
(3)10 s末,生成物D的浓度为________ 。
(4)A与B的平衡转化率之比为________ 。
(5)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度____________ ;②增大A的浓度____________ 。
(1)用C表示10 s内反应的平均反应速率为
(2)反应前A的物质的量浓度是
(3)10 s末,生成物D的浓度为
(4)A与B的平衡转化率之比为
(5)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某校化学活动社团为测定1mol/L的H2SO4溶液与锌粒和锌粉反应的速率,设计如图1装置。
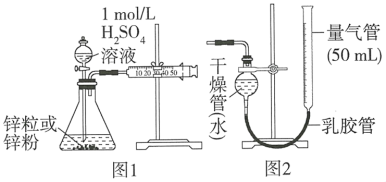
(1)图1中盛有H2SO4溶液的仪器名称是_______ 。
(2)按照图1装置实验时,限定了两次实验时间均为10min,还需要测定的另一个数据是_______ 。
(3)若将图1装置中的气体收集装置改为图2装置,实验完毕待冷却后,该学生准备读取量气管上液面所在处的刻度,发现量气管中液面高于干燥管中液面,应首先采取的操作是_______ 。

(1)图1中盛有H2SO4溶液的仪器名称是
(2)按照图1装置实验时,限定了两次实验时间均为10min,还需要测定的另一个数据是
(3)若将图1装置中的气体收集装置改为图2装置,实验完毕待冷却后,该学生准备读取量气管上液面所在处的刻度,发现量气管中液面高于干燥管中液面,应首先采取的操作是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)①通过实验A、B,可探究出_________ (填外部因素)的改变对化学反应速率的影响,其中V1=______ 、T1=________ ;
②通过实验__________ (填实验序号),可探究出_______ (填外部因素)的变化对化学反应速率的影响,其中V2=______ 。
(2)若t1<8,则由此实验可以得出的结论是__________ ;忽略溶液体积的变化,利用实验B中数据计算,0~8 s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=________ (保留2位有效数字)。
(3)该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊作用,则该作用是_____________ ,相应的粒子最可能是________ (填粒子符号)。

| 实验序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
②通过实验
(2)若t1<8,则由此实验可以得出的结论是
(3)该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊作用,则该作用是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】为比较Fe3+和Cu2+对H2O2分解的催化效果,甲乙两组同学分别设计了如图一、图二所示的实验。
(1)可通过观察图一的现象:_______________ ,而定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是_____________ ,你认为还可以作何改进?____________________ 。
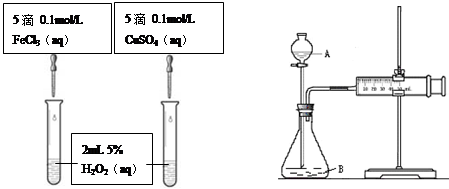
图一 图二
(2)检查图二装置气密性的方法是_______________________ 。图二所示实验中需测量的数据是________________________ 。
(1)可通过观察图一的现象:

图一 图二
(2)检查图二装置气密性的方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】草酸与高锰酸钾在酸性条件下能够发生如下反应: +H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
+H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
(1)该反应中氧化剂和还原剂的物质的量之比为______ 。
(2)我们可以通过观察_____ ,来判断反应速率的大小
(3)如果研究催化剂对化学反应速率的影响,使用实验______ 和_____ (用Ⅰ~Ⅳ表示,下同),如果研究温度对化学反应速率的影响,使用实验_______ 和______ (用Ⅰ~Ⅳ表示,下同)。
(4)实验Ⅰ和Ⅳ研究浓度对反应速率的影响,Ⅳ中加入1mL蒸馏水的目的是_____ 。
(5)反应I、III、IV中都可观察到反应速率先慢后快的现象,引起这种现象的原因是_____ 。
 +H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:
+H2C2O4+H+=Mn2++CO2↑+H2O(未配平),用4mL 0.001mol•L﹣1KMnO4溶液与2mL 0.01mol•L﹣1 H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:回答下列问题:组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 2 | 20 | |
Ⅱ | 2 | 20 | 5滴饱和MnSO4溶液 |
Ⅲ | 2 | 30 | |
Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(2)我们可以通过观察
(3)如果研究催化剂对化学反应速率的影响,使用实验
(4)实验Ⅰ和Ⅳ研究浓度对反应速率的影响,Ⅳ中加入1mL蒸馏水的目的是
(5)反应I、III、IV中都可观察到反应速率先慢后快的现象,引起这种现象的原因是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】乙烯(CH2=CH2)是非常重要的化工基础原料,由乙烯可以制备很多有机物。
I.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol水,发生CH2=CH2(g)+H2O(g) CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:
CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:
(1)计算在0-6min内的反应速率v(H2O)=___________ mol·L-1·min-1。
(2)8min时反应达到化学平衡状态,其理由是:___________ 。
Ⅱ.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g) CH3CH3(g),容器内气体的压强与反应时间的关系如下图:
CH3CH3(g),容器内气体的压强与反应时间的关系如下图:
(3)下列措施能增大反应速率的是___________(填字母)。
(4)达到化学平衡状态时,下列数值与开始时相同的是___________(填序号)
(5)反应进行到10min时,乙烯(CH2=CH2)的转化率a%=___________ 。
I.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol水,发生CH2=CH2(g)+H2O(g)
 CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:
CH3-CH2-OH(g)。乙醇的物质的量与反应时间的关系如下图:| 时间(min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 乙醇的物质的量(mol) | 0 | 0.3 | 0.5 | 0.6 | 0.65 | 0.65 |
(2)8min时反应达到化学平衡状态,其理由是:
Ⅱ.在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)
 CH3CH3(g),容器内气体的压强与反应时间的关系如下图:
CH3CH3(g),容器内气体的压强与反应时间的关系如下图:| 时间(min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 气体压强(MPa) | 100 | 80 | 70 | 65 | 60 | 60 |
| A.升高温度 |
| B.降低压强 |
| C.减小CH3CH3的浓度 |
| D.加入合适的催化剂 |
| A.容器内气体的压强 |
| B.容器内n(H2) |
| C.容器内c(CH2=CH2) |
| D.容器内气体的总质量 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】二氧化碳的捕捉、封存与再利用是实现温室气体减排的重要途径之一。
(1)二氧化碳的电子式为___________ 。
(2)下列利用二氧化碳的反应中原子利用率达100%的是_________ (填序号)。
a.CO2+2NH3 CO(NH2)2+H2O
CO(NH2)2+H2O
b.CO2+CH4 CH3COOH
CH3COOH
c.CO2+3H2 CH3OH+H2O
CH3OH+H2O
d.
(3)一种正在开发的利用二氧化碳制取甲醇的流程如下:
①反应(Ⅰ)将CO2和H2O转化为甲酸常用途径有两种,如下图(a)和(b)。
图(a)中能量主要转化方式为___________ ,图(b)中发生反应的化学方程式为___________ 。
②在5L的恒温恒容密闭容器中充入1moLCO和4molH2,加入催化剂发生反应,测得CO及CH3OH的物质的量随时间变化如下图所示。
图中第___________ min(填数字)反应达到平衡,CO在0~4min内的平均反应速率比在4~8min内的快,其原因是___________ ;达到平衡时氢气的浓度为___________ 。
(1)二氧化碳的电子式为
(2)下列利用二氧化碳的反应中原子利用率达100%的是
a.CO2+2NH3
 CO(NH2)2+H2O
CO(NH2)2+H2O b.CO2+CH4
 CH3COOH
CH3COOHc.CO2+3H2
 CH3OH+H2O
CH3OH+H2Od.

(3)一种正在开发的利用二氧化碳制取甲醇的流程如下:

①反应(Ⅰ)将CO2和H2O转化为甲酸常用途径有两种,如下图(a)和(b)。

图(a)中能量主要转化方式为
②在5L的恒温恒容密闭容器中充入1moLCO和4molH2,加入催化剂发生反应,测得CO及CH3OH的物质的量随时间变化如下图所示。

图中第
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用,为探究氯气的性质,某同学设计了如图所示的实验装置。
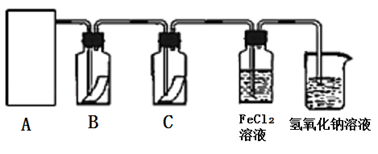
(1)实验中制取氯气的反应原理为(用化学方程式表示):______ 。
(2)利用以上制气原理,从图中选择合适的制气装置(A处)___ (填写序号) 。

(3)装置B、C依次放的是干燥的红色布条和湿润的红色布条,理论上装置______ 中的红色布条褪色,但实验过程中该同学发现装置B、C中的布条均褪色,其原因可能是______ ,说明该装置存在明显的缺陷,请提出合理的改进方法_____ 。
(4)为了验证氯气的氧化性, 将氯气通入FeCl2溶液中,写出氯气 与FeCl2溶液反应的离子方程式_ 。
(5)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是____ (填化学式)

(1)实验中制取氯气的反应原理为(用化学方程式表示):
(2)利用以上制气原理,从图中选择合适的制气装置(A处)

(3)装置B、C依次放的是干燥的红色布条和湿润的红色布条,理论上装置
(4)为了验证氯气的氧化性, 将氯气通入FeCl2溶液中,写出氯气 与FeCl2溶液反应的离子方程式
(5)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时,还需要加入稀硫酸和_______ ,原因是_______ ,对应的离子方程式_______ 。
(2)除去蒸馏水中溶解的O2常采用_______ 的方法。
(3)向FeSO4溶液中滴入氢氧化钠溶液后,沉淀颜色变化顺序为_______
A.红褐色、灰绿色、白色 B.白色、红褐色、黑色
C.白色、灰绿色、红褐色 D.蓝色、灰绿色、绿色
反应的化学方程式是_______ 。
(4)生成Fe(OH)2白色沉淀的操作是:用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是_______ 。

(1)用硫酸亚铁晶体配制上述FeSO4溶液时,还需要加入稀硫酸和
(2)除去蒸馏水中溶解的O2常采用
(3)向FeSO4溶液中滴入氢氧化钠溶液后,沉淀颜色变化顺序为
A.红褐色、灰绿色、白色 B.白色、红褐色、黑色
C.白色、灰绿色、红褐色 D.蓝色、灰绿色、绿色
反应的化学方程式是
(4)生成Fe(OH)2白色沉淀的操作是:用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用做供氧剂。

(1)A是制取CO2的装置。写出A中发生反应的化学方程式:______ 。
(2)填写表中空格:
(3)写出Na2O2与CO2反应的化学方程式:______ 。
(4)试管中收集满气体后,下一步实验操作及现象、结论是___ 。

(1)A是制取CO2的装置。写出A中发生反应的化学方程式:
(2)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | 除去CO2中混有的HCl |
| C | Na2O2 | |
| D | NaOH溶液 |
(4)试管中收集满气体后,下一步实验操作及现象、结论是
您最近一年使用:0次



