我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸的反应为:S+2KNO3+3C=K2S+N2↑+3CO2↑。下列说法正确的是
| A.N2是还原剂 | B.KNO3在反应中得到电子 |
| C.S在反应中被氧化 | D.1mol C参加反应有2 mol电子转移 |
更新时间:2020-07-07 17:05:18
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列变化中需加入还原剂才能实现的是
| A.Cl2→Cl- | B.Fe2O3→Fe | C.SO2→SO3 | D.C→CO2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列粒子不具有氧化性的是
| A.HCl | B.Fe2+ | C.Mg | D.KMnO4 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】用NA表示阿伏德罗常数,下列叙述正确的是
| A.标准状况下,11.2LH2O含有的分子数为0.5NA |
| B.通常状况下,NA个CO2分子占有的体积为22.4L |
| C.5.6g铁与足量氯气充分反应,转移电子数为0.2NA |
| D.常温常压下,1.4g氮气含有的氮原子数为0.1NA |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】火药是中国的“四大发明”之一。黑火药在发生爆炸时,发生的反应为2KNO3+3C+S=K2S+N2↑+3CO2↑,下列有关说法正确的是
| A.C是还原剂,KNO3与S是氧化剂 | B.当转移l mol e-时,有2.24 L N2生成 |
C.N2的电子式为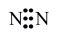 | D.K2S为共价化合物 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐3】阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A.1L0.1mol· NH4Cl溶液中, NH4Cl溶液中, 的数量为0.1 的数量为0.1 |
B.2.3gNa与O2完全反应,转移的电子数为0.1 |
C.标准状况下,2.24LN2和O2的混合气体中分子数为0.2 |
D.0.1mol NO和0.05mol O2于密闭容器中充分反应后,其分子总数为0.1 |
您最近一年使用:0次



