某学生为探究钠与二氧化碳的反应,利用如图装置进行实验。
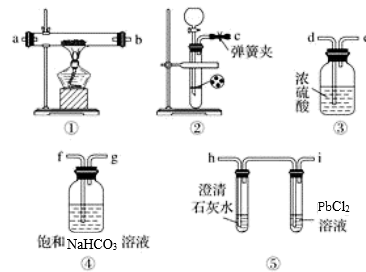
已知PdCl2能被一氧化碳还原得到黑色的Pd.请回答下列问题:
(1)请将如图各装置连接完整:c接f,_____ 接_____ ,_____ 接_____ ,_____ 接_____ 。
(2)若用稀盐酸与碳酸钙反应制备二氧化碳,在加稀盐酸时,发现碳酸钙与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是_____ (填字母)。
A.硝酸钠溶液 B.四氯化碳 C.苯 D.稀硝酸
(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让二氧化碳充满整个装置,当观察到_____ 时,再点燃酒精灯。此步操作的目的是_____________________ 。
(4)反应过程中二氧化碳足量,假如装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体。写出钠与二氧化碳反应的化学方程式_______________________________ 。

已知PdCl2能被一氧化碳还原得到黑色的Pd.请回答下列问题:
(1)请将如图各装置连接完整:c接f,
(2)若用稀盐酸与碳酸钙反应制备二氧化碳,在加稀盐酸时,发现碳酸钙与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是
A.硝酸钠溶液 B.四氯化碳 C.苯 D.稀硝酸
(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让二氧化碳充满整个装置,当观察到
(4)反应过程中二氧化碳足量,假如装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体。写出钠与二氧化碳反应的化学方程式
19-20高一下·山东德州·阶段练习 查看更多[7]
作业(七) 活泼的金属单质——钠甘肃省张掖市、陇南2地联考2022-2023学年高一上学期12月期中考试化学试题辽宁省沈阳市一二〇中学2021-2022学年高一上学期第一次月考化学试题(已下线)3.1.1 金属与非金属的反应(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版)(已下线)2.1.1活泼的金属单质——钠(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)2.1.1 活泼的金属单质——钠-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)山东省德州市夏津第一中学2019-2020学年高一下学期7月月考化学试题
更新时间:2020-07-20 21:19:50
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】 如图,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物。已知A在空气中燃烧生成淡黄色固体(部分产物已略去)。
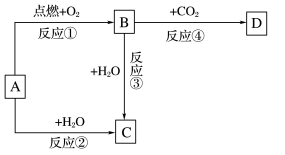
请填写下列空白:
(1)写出化学式:
A____ 、B____ 、C____ 、D____ 。
(2)以上反应中属于置换反应的有_____ (填写编号)。
(3)写出下列转化的化学方程式:
A C
C_____
B C
C________ 。

请填写下列空白:
(1)写出化学式:
A
(2)以上反应中属于置换反应的有
(3)写出下列转化的化学方程式:
A
 C
CB
 C
C
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某同学为测定一定质量的钠与水反应产生的氢气的体积,设计了图装置进行实验。
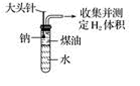
(1)实验开始,欲使钠与水接触反应,应如何操作?______________________________ ;反应开始后,试管中能观察到的现象是__________________________________________ 。
(2)已知有关物质的密度ρ(K):0.86 g·cm-3,ρ(Na):0.97 g·cm-3,ρ(煤油):0.8 g·cm-3。如果将钠换成相同大小的钾进行上述实验,结果钾反应完所用时间比钠反应完所用的时间________ (填“长”或“短”),其原因是________________________________ 。
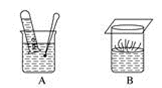
(3)从实验的安全考虑,比较金属钠、钾与水反应的实验操作图A、图B,请指出图B表示哪种金属与水反应____________________________ 。

(1)实验开始,欲使钠与水接触反应,应如何操作?
(2)已知有关物质的密度ρ(K):0.86 g·cm-3,ρ(Na):0.97 g·cm-3,ρ(煤油):0.8 g·cm-3。如果将钠换成相同大小的钾进行上述实验,结果钾反应完所用时间比钠反应完所用的时间
(3)从实验的安全考虑,比较金属钠、钾与水反应的实验操作图A、图B,请指出图B表示哪种金属与水反应

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】如图所示,下列各项变化的未知物焰色反应均呈黄色,E为淡黄色粉末。
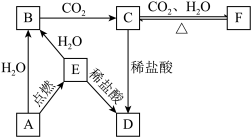
回答下列问题。
(1)写出A→B的化学方程式,_____________________ 。
(2)写出C→D的离子方程式,_____________ 。
(3)当C溶液中含有杂质F,如何除杂:____________________ ,反应涉及的离子方程式_____________ 。
(4)E与CO2反应气体体积减小了11.2L(标准状况下),反应中转移电子的数目是___________ 。
(5)在一密闭容器中有CO、H2、O2共16.5 g和足量的E,用电火花引燃,使其完全反应,固体增重7.5 g,则原混合气体中O2的质量是__________ g。

回答下列问题。
(1)写出A→B的化学方程式,
(2)写出C→D的离子方程式,
(3)当C溶液中含有杂质F,如何除杂:
(4)E与CO2反应气体体积减小了11.2L(标准状况下),反应中转移电子的数目是
(5)在一密闭容器中有CO、H2、O2共16.5 g和足量的E,用电火花引燃,使其完全反应,固体增重7.5 g,则原混合气体中O2的质量是
您最近一年使用:0次
【推荐1】某研究性学习小组设计用如图所示实验装置(夹持仪器省略)制取干燥的氨气并验证NH3具有还原性,请回答下列问题:
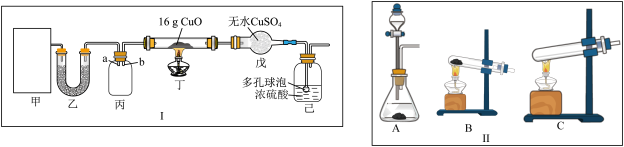
(1)实验室制备氨气有多种方法,现欲用NH4C1与Ca(OH)2反应制取NH3,则甲中的气体发生装置___________ (从Ⅱ中选用);用浓氨水与生石灰反应也可制取NH3,反应的化学方程式为__________
(2)装置丙用于收集NH3,应将导管__________ (填“a”或“b”)延长至集气瓶底部,装置乙中盛放的试剂为__________ ,装置己的作用为____________ (答两点)。
(3)若装置丁中黑色固体变红,则装置戊中现象为_________
(4)研究小组的同学通过讨论、分析后认为充分反应后生成的红色固体可能是Cu或Cu2O或二者的混合物,通过查阅资料知:Cu2O+2H+=Cu+Cu2++H2O。为探究固体的成分,提出了如下两种方案。
I. 甲同学取少量红色固体与稀硝酸混合,最终得到蓝色溶液,由此推测红色产物中有Cu2O。
①你对甲同学实验设计的评价是__________ (请给出必要的文字解释)。
②Cu2O与稀硝酸反应的离子方程式为_____________
Ⅱ.乙同学认为不需要借助任何化学试剂,只需要称量生成的红色固体的质量(设为xg)就能确定产物成分,当x取值范围为_____ 时,表明产物中既有Cu,又有Cu2O。

(1)实验室制备氨气有多种方法,现欲用NH4C1与Ca(OH)2反应制取NH3,则甲中的气体发生装置
(2)装置丙用于收集NH3,应将导管
(3)若装置丁中黑色固体变红,则装置戊中现象为
(4)研究小组的同学通过讨论、分析后认为充分反应后生成的红色固体可能是Cu或Cu2O或二者的混合物,通过查阅资料知:Cu2O+2H+=Cu+Cu2++H2O。为探究固体的成分,提出了如下两种方案。
I. 甲同学取少量红色固体与稀硝酸混合,最终得到蓝色溶液,由此推测红色产物中有Cu2O。
①你对甲同学实验设计的评价是
②Cu2O与稀硝酸反应的离子方程式为
Ⅱ.乙同学认为不需要借助任何化学试剂,只需要称量生成的红色固体的质量(设为xg)就能确定产物成分,当x取值范围为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某研究性学习小组利用如图所示装置完成有关实验。
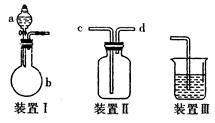
【实验一】快速制氨气
(1)用装置I快速制氨气,则装置I的a仪器中可加入浓氨水,b仪器中加入 。装置Ⅱ从 管口进气可作为氨气的收集装置。
【实验二】收集NO
(2)利用装置Ⅱ可收集NO,试简述操作方法: 。
【实验三】比较硫、碳、硅三种元素的非金属性强弱
(3)设计实验,完成下列表格(可以不填满,也可以再加行)

【实验一】快速制氨气
(1)用装置I快速制氨气,则装置I的a仪器中可加入浓氨水,b仪器中加入 。装置Ⅱ从 管口进气可作为氨气的收集装置。
【实验二】收集NO
(2)利用装置Ⅱ可收集NO,试简述操作方法: 。
【实验三】比较硫、碳、硅三种元素的非金属性强弱
(3)设计实验,完成下列表格(可以不填满,也可以再加行)
| 装置序号 | 仪器中所加物质名称 | 现象 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。

(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是__________________ 。
(2)实验室用装置E制备Cl2,其反应的化学方程式为__________________________ ;若有8mol的HCl参加反应,则转移的电子总数为________ 。
(3)该装置中氢氧化钠溶液的作用是___________________ 。
(4)通气后B、D两个试管中的现象______________ 。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:________ ,D:________ 。
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)____________________ 。

(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是
(2)实验室用装置E制备Cl2,其反应的化学方程式为
(3)该装置中氢氧化钠溶液的作用是
(4)通气后B、D两个试管中的现象
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某研究小组将纯净的 气体通入
气体通入 的
的 溶液中,得到了
溶液中,得到了 沉淀。为探究上述溶液中何种微粒能氧化通入的
沉淀。为探究上述溶液中何种微粒能氧化通入的 ,该小组提出了如下假设:
,该小组提出了如下假设:
假设一:溶液中的
假设二:溶液中溶解的
(1)验证假设一
该小组设计实验验证了假设一。请在下表空白处填写相关实验现象。
(2)验证假设二
请设计实验验证假设二,写出实验步骤、预期现象和结论。
 气体通入
气体通入 的
的 溶液中,得到了
溶液中,得到了 沉淀。为探究上述溶液中何种微粒能氧化通入的
沉淀。为探究上述溶液中何种微粒能氧化通入的 ,该小组提出了如下假设:
,该小组提出了如下假设:假设一:溶液中的

假设二:溶液中溶解的

(1)验证假设一
该小组设计实验验证了假设一。请在下表空白处填写相关实验现象。
| 实验步骤 | 实验现象 | 结论 |
实验1:在盛有不含 的25mL 的25mL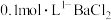 溶液的烧杯中,缓慢通入纯净的 溶液的烧杯中,缓慢通入纯净的 气体 气体 | 假设一成立 | |
实验2:在盛有不含 的 的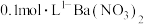 溶液的烧杯中,缓慢通入纯净的 溶液的烧杯中,缓慢通入纯净的 气体 气体 |
请设计实验验证假设二,写出实验步骤、预期现象和结论。
| 实验步骤、预期现象和结论(不要求写具体操作过程): |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时,还需要加入稀硫酸和_______ ,原因是_______ ,对应的离子方程式_______ 。
(2)除去蒸馏水中溶解的O2常采用_______ 的方法。
(3)向FeSO4溶液中滴入氢氧化钠溶液后,沉淀颜色变化顺序为_______
A.红褐色、灰绿色、白色 B.白色、红褐色、黑色
C.白色、灰绿色、红褐色 D.蓝色、灰绿色、绿色
反应的化学方程式是_______ 。
(4)生成Fe(OH)2白色沉淀的操作是:用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是_______ 。

(1)用硫酸亚铁晶体配制上述FeSO4溶液时,还需要加入稀硫酸和
(2)除去蒸馏水中溶解的O2常采用
(3)向FeSO4溶液中滴入氢氧化钠溶液后,沉淀颜色变化顺序为
A.红褐色、灰绿色、白色 B.白色、红褐色、黑色
C.白色、灰绿色、红褐色 D.蓝色、灰绿色、绿色
反应的化学方程式是
(4)生成Fe(OH)2白色沉淀的操作是:用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是

您最近一年使用:0次




