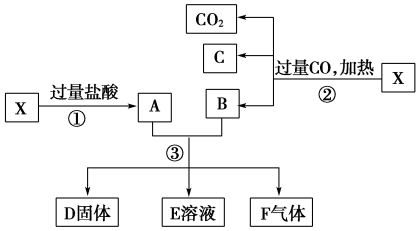
利用硫酸渣(主要含Fe2O3、FeO,杂质为Al2O3和SiO2等)生产铁基颜料铁黄(FeOOH)的制备流程如下:
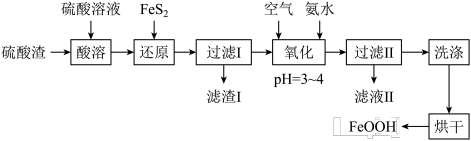
(1)“酸溶”时,Fe2O3与硫酸反应的离子方程式为___________________ 。
(2)滤渣I的主要成分是FeS2、S和___________ (填化学式);Fe3+被FeS2还原的离子方程式为_______________ 。
(3)“氧化”中,生成FeOOH的离子方程式为_______________ 。

(1)“酸溶”时,Fe2O3与硫酸反应的离子方程式为
(2)滤渣I的主要成分是FeS2、S和
(3)“氧化”中,生成FeOOH的离子方程式为
19-20高二下·辽宁大连·阶段练习 查看更多[2]
更新时间:2020-07-21 13:12:26
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】为响应党的二十大重要精神,将经济建设与环境保护的工作合二为一,黄铁矿(主要成分是 ,还有少量
,还有少量 等杂质)冶铁时产生的大量
等杂质)冶铁时产生的大量 废气在工业上进一步回收利用的工艺流程如下图:
废气在工业上进一步回收利用的工艺流程如下图:
(1)“煅烧”时,将空气从黄铁矿底部通入的目的是___________ ;写出该反应生成 的化学方程式:
的化学方程式:___________ 。
(2)“高炉炼铁”时,加入石灰石的作用是与 反应生成硅酸盐从而形成炉渣,
反应生成硅酸盐从而形成炉渣,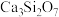 用氧化物的形式(
用氧化物的形式(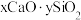 )可以表示为
)可以表示为___________ 。
(3)“氧化1”得到的气体中仍然混有 、
、 ,且延长反应时间气体中
,且延长反应时间气体中 、
、 的含量不变,原因是
的含量不变,原因是___________ ;“吸收”时,要用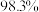 浓硫酸吸收
浓硫酸吸收 而不是用
而不是用 ,主要原因是
,主要原因是___________ 。
(4)在“吸收塔”中, 和
和 吸收
吸收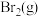 发生反应的离子方程式为
发生反应的离子方程式为___________ ;“氧化2”得到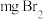 理论上需要通入
理论上需要通入___________ 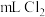 (假设该状态下的摩尔体积为
(假设该状态下的摩尔体积为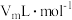 ,用含
,用含 的式子表示)。
的式子表示)。
 ,还有少量
,还有少量 等杂质)冶铁时产生的大量
等杂质)冶铁时产生的大量 废气在工业上进一步回收利用的工艺流程如下图:
废气在工业上进一步回收利用的工艺流程如下图: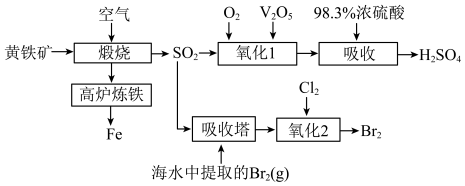
(1)“煅烧”时,将空气从黄铁矿底部通入的目的是
 的化学方程式:
的化学方程式:(2)“高炉炼铁”时,加入石灰石的作用是与
 反应生成硅酸盐从而形成炉渣,
反应生成硅酸盐从而形成炉渣,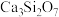 用氧化物的形式(
用氧化物的形式(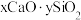 )可以表示为
)可以表示为(3)“氧化1”得到的气体中仍然混有
 、
、 ,且延长反应时间气体中
,且延长反应时间气体中 、
、 的含量不变,原因是
的含量不变,原因是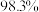 浓硫酸吸收
浓硫酸吸收 而不是用
而不是用 ,主要原因是
,主要原因是(4)在“吸收塔”中,
 和
和 吸收
吸收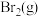 发生反应的离子方程式为
发生反应的离子方程式为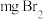 理论上需要通入
理论上需要通入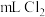 (假设该状态下的摩尔体积为
(假设该状态下的摩尔体积为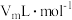 ,用含
,用含 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】利用下图,可以从不同角度研究含硫物质的性质及其转化关系,图中物质甲~己中均含有硫元素.回答下列问题:
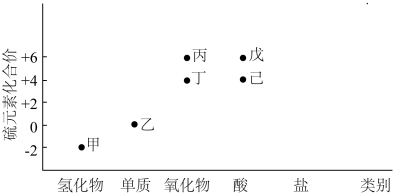
(1)写出甲的电子式:_______ ,该物质中的硫元素可表现出___________ (填“氧化性”或“还原性”);利用高温热分解甲可以获得乙,该方法的优点是______________ ,缺点是_____________ .
(2)黄铁矿(主要成分为 )在沸腾炉中与氧气反应,主要生成的含硫元素的物质是
)在沸腾炉中与氧气反应,主要生成的含硫元素的物质是__________ (填“丙”或“丁”),该物质与水化合生成___________ (填化学名称).
(3)① 溶液与戊溶液反应的离子方程式为
溶液与戊溶液反应的离子方程式为_______________________________ .
②同位素示踪实验可证实 中两个S原子的化学环境不同,实验过程为
中两个S原子的化学环境不同,实验过程为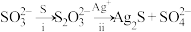 .过程ii中,
.过程ii中, 断裂的只有硫硫键,若过程i所用试剂为
断裂的只有硫硫键,若过程i所用试剂为 和
和 ,过程ii含硫产物是
,过程ii含硫产物是_____________ (标记出同位素原子).

(1)写出甲的电子式:
(2)黄铁矿(主要成分为
 )在沸腾炉中与氧气反应,主要生成的含硫元素的物质是
)在沸腾炉中与氧气反应,主要生成的含硫元素的物质是(3)①
 溶液与戊溶液反应的离子方程式为
溶液与戊溶液反应的离子方程式为②同位素示踪实验可证实
 中两个S原子的化学环境不同,实验过程为
中两个S原子的化学环境不同,实验过程为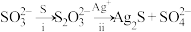 .过程ii中,
.过程ii中, 断裂的只有硫硫键,若过程i所用试剂为
断裂的只有硫硫键,若过程i所用试剂为 和
和 ,过程ii含硫产物是
,过程ii含硫产物是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】利用“价类二维图”研究物质的性质是化学研究的重要手段。下图是氯元素的化合价与部分物质类别的对应关系。
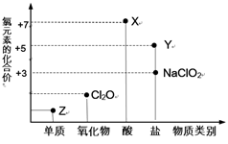
回答下列问题:
(1)X的电离方程式为______ 。
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为71:48,则m:n=______ 。
(3)Y可用于实验室制O2,其焰色试验为紫色,则Y含有的化学键类型为______ 。
(4)Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为______ 。

回答下列问题:
(1)X的电离方程式为
(2)氯的某种氧化物(ClmOn)中氯、氧元素质量比为71:48,则m:n=
(3)Y可用于实验室制O2,其焰色试验为紫色,则Y含有的化学键类型为
(4)Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】碳、硅及其化合物的开发由来已久,在现代生活中有广泛应用。

(1)SiO2是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是____ (用化学方程式表示)。
(2)某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,…,关闭活塞a。
请回答:
①B中反应的离子方程式是____ 。
②C装置的作用是____ ,X是____ 。
③为了验证碳的非金属性强于硅,步骤Ⅱ中未写的操作和现象是____ ,装置D中反应的化学方程是____ 。

(1)SiO2是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
(2)某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,…,关闭活塞a。
请回答:
①B中反应的离子方程式是
②C装置的作用是
③为了验证碳的非金属性强于硅,步骤Ⅱ中未写的操作和现象是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】冰晶石(Na3AlF6)是工业上冶炼金属铝的熔剂,以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:
(1)气体B易溶于水,画出其水溶液中可能存在的氢键形式:___________ 。解释工业上利用萤石(CaF2)制取气体B而不用氢气与其单质发生化合反应的原因:___________ 。
(2)下列说法正确的是___________。
(3)写出由气体B制备冰晶石的化学方程式:___________ 。
(4)将固体A(仅含一种化合物 )加入水中,设计实验检验所得澄清溶液中阴离子___________ 。

(1)气体B易溶于水,画出其水溶液中可能存在的氢键形式:
(2)下列说法正确的是___________。
| A.为防止空气进入,须在玻璃容器中进行 | B.固体A中可能存在少量氟化钙 |
| C.冰晶石是由NaF和AlF3组成的混合物 | D.酸性:Al(OH)3<HClO |
(4)将固体A(
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的操作方法为:____ 。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___________ (填选项编号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、___________ (填操作名称)、过滤、洗涤。
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___________(填选项编号)。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的操作方法为:
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___________(填选项编号)。
A.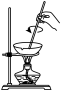 | B. | C. | D.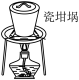 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某化学兴趣小组利用下列试剂:铁粉、锌粉、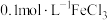 溶液,
溶液,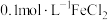 溶液,
溶液, 溶液;淀粉溶液,
溶液;淀粉溶液, 溶液,新制氯水,探究
溶液,新制氯水,探究 的氧化性、还原性,并利用实验结论解决一些问题。
的氧化性、还原性,并利用实验结论解决一些问题。
(1) 原子在周期表中的位置是
原子在周期表中的位置是___________ 。
(2)用所给试剂写出体现 具有还原性的反应的化学方程式
具有还原性的反应的化学方程式___________ 。
(3)设计实验方案,完成下列表格。
(4)该兴趣小组为说明“ 具有氧化性”,提出了向
具有氧化性”,提出了向 溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为
溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为___________ 。
(5) 溶液中加入
溶液中加入 溶液,是为了检验
溶液,是为了检验 的
的___________ (填“氧化性”或“还原性”),在溶液中 与
与
___________ (填“能”或“不能”)大量共存,如果不能大量共存,请写出该反应的离子方程式___________ 。
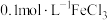 溶液,
溶液,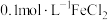 溶液,
溶液, 溶液;淀粉溶液,
溶液;淀粉溶液, 溶液,新制氯水,探究
溶液,新制氯水,探究 的氧化性、还原性,并利用实验结论解决一些问题。
的氧化性、还原性,并利用实验结论解决一些问题。(1)
 原子在周期表中的位置是
原子在周期表中的位置是(2)用所给试剂写出体现
 具有还原性的反应的化学方程式
具有还原性的反应的化学方程式(3)设计实验方案,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 |
探究 具有氧化性 具有氧化性 | ①取少量 溶液,往溶液中加入足量铁粉,再加入少量 溶液,往溶液中加入足量铁粉,再加入少量 溶液 溶液 | 加入铁粉后,溶液颜色变为 |
②取少量 溶液,往溶液中滴入3滴 溶液,往溶液中滴入3滴 溶液,然后再滴加2滴淀粉溶液 溶液,然后再滴加2滴淀粉溶液 | 加入淀粉溶液可观察到 |
(4)该兴趣小组为说明“
 具有氧化性”,提出了向
具有氧化性”,提出了向 溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为
溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为(5)
 溶液中加入
溶液中加入 溶液,是为了检验
溶液,是为了检验 的
的 与
与
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】长期放置的 溶液易被氧化而变质,某兴趣小组进行了如下实验:
溶液易被氧化而变质,某兴趣小组进行了如下实验:
(1)设计实验检验 ,溶液的变质程度。
,溶液的变质程度。
①补充上述实验方案中的实验现象_______ 、_______ 。
②若要使部分变质的 复原,方法是
复原,方法是_______ (用离子方程式表示)。
③步骤2加入酸性高锰酸钾溶液离子方程式是_______ 。
(2)利用部分变质的 溶液制备
溶液制备 。
。
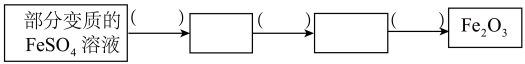
①图中所填是所需试剂或条件,分别为_______ 、_______ 、_______ 、“ ”中所填是含铁物质的化学式,分别是
”中所填是含铁物质的化学式,分别是_______ 、_______ (以离子形式存在的可写离子符号)。
②若100 mL该变质溶液能制得1.6g (实验过程误差忽略),则变质前
(实验过程误差忽略),则变质前 溶液物质的量浓度为
溶液物质的量浓度为_______ 。
(3) 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:
由上述实验_______ (填能或不能)得出“维生素C可将 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:_______ 。
 溶液易被氧化而变质,某兴趣小组进行了如下实验:
溶液易被氧化而变质,某兴趣小组进行了如下实验:(1)设计实验检验
 ,溶液的变质程度。
,溶液的变质程度。| 实验方案 | 步骤1 | 步骤2 |
| 取待检测液于试管中,向其中滴加KSCN溶液 | 取待检测液于试管中,向其中滴加少量酸性高锰酸钾溶液 | |
| 实验现象 | _______ | _______ |
| 实验结论 |  溶液部分变质 溶液部分变质 | |
②若要使部分变质的
 复原,方法是
复原,方法是③步骤2加入酸性高锰酸钾溶液离子方程式是
(2)利用部分变质的
 溶液制备
溶液制备 。
。
①图中所填是所需试剂或条件,分别为
 ”中所填是含铁物质的化学式,分别是
”中所填是含铁物质的化学式,分别是②若100 mL该变质溶液能制得1.6g
 (实验过程误差忽略),则变质前
(实验过程误差忽略),则变质前 溶液物质的量浓度为
溶液物质的量浓度为(3)
 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将
可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将 转化为
转化为 ,以利于人体吸收。为了验证这一猜想,设计了如下实验:
,以利于人体吸收。为了验证这一猜想,设计了如下实验:| 实验方案 | 实验现象 |
取适量 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液 | 紫色褪去 |
 转化为
转化为 ”的结论?请说明理由:
”的结论?请说明理由:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】硫酸铁铵[化学式可表示为NH4Fe(SO4)2]可用作分析试剂等。某兴趣小组利用铁矿石(主要成分为Fe3O4、Fe2O3)制硫酸铁铵的流程如下:
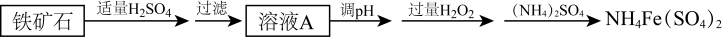
回答下列问题:
(1)写出Fe3O4与稀硫酸反应的离子方程式:___________ 。
(2)加入H2O2的作用是___________ 。
(3)若想探究NH4Fe(SO4)2与Ba(OH)2反应生成最大质量沉淀的条件,某同学向含amolNH4Fe(SO4)2的溶液中滴加含bmolBa(OH)2的溶液,与OH—反应的顺序:先是___________ (填离子符号,下同)后是___________ ,当a=b时,发生的离子反应为___________ ,当___________ 时,沉淀的质量达到最大。
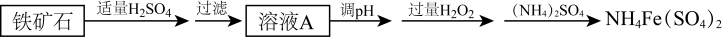
回答下列问题:
(1)写出Fe3O4与稀硫酸反应的离子方程式:
(2)加入H2O2的作用是
(3)若想探究NH4Fe(SO4)2与Ba(OH)2反应生成最大质量沉淀的条件,某同学向含amolNH4Fe(SO4)2的溶液中滴加含bmolBa(OH)2的溶液,与OH—反应的顺序:先是
您最近一年使用:0次
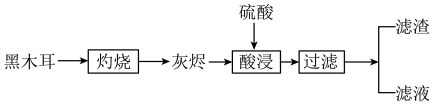
【推荐1】黑木耳是常见食品,可以补充人体所必需的微量元素铁。某兴趣小组设计实验,检验黑木耳中的铁元素,实验流程如图:
(1)灼烧黑木耳必须用到下列仪器中的___ (填字母)。
A. B.
B.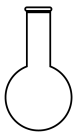 C.
C.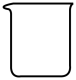 D.
D.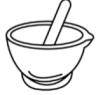
(2)灰烬中含有铁的氧化物以及钾、钙、硅等元素的化合物,酸浸的目的是___ 。
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有___ ;另取滤液检验,滤液能使KMnO4溶液紫色褪去,说明滤液中存在具有___ (填“氧化性”或“还原性”)的粒子。
(4)为进一步探究Fe3+和Fe2+的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
(5)实验结束,离开实验室之前,下列做法正确的是___ (填字母)。
A.废弃药品直接倒入水池冲走 B.药品仪器归放
C.清洁实验仪器,打扫实验室卫生 D.关闭水电、门窗

(1)灼烧黑木耳必须用到下列仪器中的
A.
 B.
B. C.
C. D.
D.
(2)灰烬中含有铁的氧化物以及钾、钙、硅等元素的化合物,酸浸的目的是
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有
(4)为进一步探究Fe3+和Fe2+的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
| 实验操作 | 实验现象 | 离子方程式 | 实验结论 |
| 向FeCl2溶液中添加新制氯水 | 溶液由浅绿色变为棕黄色 | 2Fe2++Cl2=2Fe3++2Cl- | ① |
| 向FeCl3溶液加入足量的铁粉 | 铁粉逐渐溶解,溶液由棕黄色变为浅绿色 | ② | Fe3+具有氧化性 |
A.废弃药品直接倒入水池冲走 B.药品仪器归放
C.清洁实验仪器,打扫实验室卫生 D.关闭水电、门窗
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:

已知E是形成酸雨的主要气体,请回答:
(1)A的组成元素为______ (用化学符号表示);
(2)C溶液可溶解铜片,写出该反应的离子方程式______________________________ ;
(3)写出F→G反应的化学方程式_________________________________ ,设计实验证明溶液G中含有
____________________________________________________________________ 。

已知E是形成酸雨的主要气体,请回答:
(1)A的组成元素为
(2)C溶液可溶解铜片,写出该反应的离子方程式
(3)写出F→G反应的化学方程式

您最近一年使用:0次

 和CuO的混合物,且知氧化性顺序:
和CuO的混合物,且知氧化性顺序: 。取等质量的两份X样品进行如下实验:
。取等质量的两份X样品进行如下实验: