实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:2KMnO4+16HCl(浓)=2KCl+MnCl2+5Cl2↑+8H2O
①该反应中浓盐酸体现出来的性质为______
②氧化剂与还原剂之比是______
③如反应中转移了0.6mol电子,则产生的气体在标准状况下体积为______ .
①该反应中浓盐酸体现出来的性质为
②氧化剂与还原剂之比是
③如反应中转移了0.6mol电子,则产生的气体在标准状况下体积为
更新时间:2020-07-25 21:47:27
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)医学上常用酸性高锰酸钾溶液与草酸溶液的反应来测定血钙的含量,配平以下离子方程式,并填上合适的微粒:___ H++___ MnO +
+___ H2C2O4 =___ CO2↑+___ Mn2++______
(2)请将5种物质N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
①________ +________ →________ +________ +__________ +H2O
②反应中1 mol氧化剂得到_________ mol 电子。
 +
+(2)请将5种物质N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
①
②反应中1 mol氧化剂得到
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】(1)实验室用MnO2跟浓盐酸共热反应制取Cl2,化学方程式是4HCl(浓)+MnO2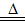 Cl2↑+MnCl2+2H2O,HCl所起的作用有
Cl2↑+MnCl2+2H2O,HCl所起的作用有___ 。
(2)KMnO4是常用的氧化剂。用KMnO4跟浓盐酸在室温下制氯气的化学方程式是2KMnO4+16HCl(浓)=2KCl+MnCl2+5Cl2↑+8H2O,用双线桥法表示该反应的电子得失情况:___ 。
(3)历史上曾用“地康法”制Cl2。这一方法是用CuCl2作催化剂,在450℃下利用空气中的O2跟HCl反应制Cl2。这一反应的化学方程式为___ 。
(4)若要制得71gCl2,则(1)(2)(3)中三种方法被氧化的HCl的质量之比是___ ,参与反应的HCl的质量之比是__ 。
(5)可知第(1)(2)(3)问中涉及的反应的氧化剂的氧化性从强到弱的顺序为KMnO4>MnO2>O2,你认为得到这个顺序的依据是__ 。
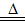 Cl2↑+MnCl2+2H2O,HCl所起的作用有
Cl2↑+MnCl2+2H2O,HCl所起的作用有(2)KMnO4是常用的氧化剂。用KMnO4跟浓盐酸在室温下制氯气的化学方程式是2KMnO4+16HCl(浓)=2KCl+MnCl2+5Cl2↑+8H2O,用双线桥法表示该反应的电子得失情况:
(3)历史上曾用“地康法”制Cl2。这一方法是用CuCl2作催化剂,在450℃下利用空气中的O2跟HCl反应制Cl2。这一反应的化学方程式为
(4)若要制得71gCl2,则(1)(2)(3)中三种方法被氧化的HCl的质量之比是
(5)可知第(1)(2)(3)问中涉及的反应的氧化剂的氧化性从强到弱的顺序为KMnO4>MnO2>O2,你认为得到这个顺序的依据是
您最近一年使用:0次
【推荐3】在工业上,次磷酸(H3PO2)常用于化学镀银,发生的反应如下:Ag++H3PO2+H2O→Ag↓+H3PO4+H+.
请回答下列问题:
(1)H3PO2中,P元素的化合价为________ ;该反应中,H3PO2被________ (填“氧化”或“还原”)。
②配平该离子方程式:________________________________________
(3)H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程式:_____________ ;
(4)若该反应有5a个电子转移,则镀件镀上银的质量为________ g(已知每个银原子质量为b g)。
请回答下列问题:
(1)H3PO2中,P元素的化合价为
②配平该离子方程式:
(3)H3PO2是一元弱酸,写出其与足量NaOH溶液反应的离子方程式:
(4)若该反应有5a个电子转移,则镀件镀上银的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中。
(1)________ 元素被氧化,________ 是氧化剂。
(2)________ 是氧化产物,________ 发生氧化反应。
(3)在参加反应的盐酸中,起还原剂(被氧化)作用的HCl与起酸性作用的HCl的质量比为_______ 。
(4)用双线桥法标明电子转移的方向和数目。____________________
(1)
(2)
(3)在参加反应的盐酸中,起还原剂(被氧化)作用的HCl与起酸性作用的HCl的质量比为
(4)用双线桥法标明电子转移的方向和数目。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】当Cl2遇到NH3时,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用“双线桥法”表示反应的电子转移方向和数目:___________ ;
(2)参加反应的NH3中,被氧化的N原子与未被氧化的N原子之比:___________ ;
(3)写出NH4Cl在溶液中的电离方程式___________ ,在其溶液中分散质粒子的直径范围为___________ ;
(4)若反应中有6.8g氨发生氧化反应,则反应中有生成氮气的质量为___________ g;请写出N2的一种用途___________ 。
(1)用“双线桥法”表示反应的电子转移方向和数目:
(2)参加反应的NH3中,被氧化的N原子与未被氧化的N原子之比:
(3)写出NH4Cl在溶液中的电离方程式
(4)若反应中有6.8g氨发生氧化反应,则反应中有生成氮气的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求写出下列方程式。
(1)实验室(舍勒法)制氯气的离子方程式:___________ 。
(2)碳酸钙溶于醋酸的离子方程式:___________ 。
(3) 胶体制备的离子方程式:
胶体制备的离子方程式:___________ 。
(4)工业制漂白粉的化学方程式:___________ 。
(5)向 溶液滴加
溶液滴加 溶液至
溶液至 时的离子方程式:
时的离子方程式:___________ 。
(1)实验室(舍勒法)制氯气的离子方程式:
(2)碳酸钙溶于醋酸的离子方程式:
(3)
 胶体制备的离子方程式:
胶体制备的离子方程式:(4)工业制漂白粉的化学方程式:
(5)向
 溶液滴加
溶液滴加 溶液至
溶液至 时的离子方程式:
时的离子方程式:
您最近一年使用:0次
【推荐2】氯元素是中学化学中常见的重要非金属元素之一,氯元素的单质及其化合物在生产与生活中有着重要的用途,依据所学知识完成下列问题:
Ⅰ.实验室制备氯气的化学方程式是_____________________ ;多余的氯气用氢氧化钠溶液吸收,其离子方程式为_________________
Ⅱ.常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,还有 NaCl与C12生成。
(1)写出并配平该反应的化学方程式____________________ 。
(2)如果反应中生成标准状况下11.2L 氯气,则被氧化的 HCl的物质的量为_______ ,转移电子数为_________ 。
(3)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为负一价),以除去水中硫化物产生的臭味。取适量ClO2,通入到含有H2S(二元弱酸)的水中,再向共中加入少量氯化钡溶液,发现有白色沉淀生成。写出ClO2与H2S水溶液反应的离子方程式____________ 。
Ⅰ.实验室制备氯气的化学方程式是
Ⅱ.常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,已被联合国世界卫生组织(WHO)列为高效安全消毒剂。常温下,它可用氯酸钠固体与浓盐酸反应制备得到,还有 NaCl与C12生成。
(1)写出并配平该反应的化学方程式
(2)如果反应中生成标准状况下11.2L 氯气,则被氧化的 HCl的物质的量为
(3)二氧化氯可迅速氧化硫化物(其中还原产物中氯元素为负一价),以除去水中硫化物产生的臭味。取适量ClO2,通入到含有H2S(二元弱酸)的水中,再向共中加入少量氯化钡溶液,发现有白色沉淀生成。写出ClO2与H2S水溶液反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题:
(1)关于甲、乙、丙、丁四套装置的说法正确的是_______ 。

(2)以下物质(或粒子)与其用途之间关联正确的是_______ 。
(3)实验室制取Cl2的化学方程式:_______ 。浓盐酸表现的性质是_______ 。
(4)已知:在稀硫酸中,MnO 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。_______
(1)关于甲、乙、丙、丁四套装置的说法正确的是

| A.用装置甲制取氯气 | B.用丙装置可以较长时间看到白色Fe(OH)2白色沉淀 |
| C.用丁装置证明碳酸氢钠受热易分解 | D.用装置乙除去氢气中的少量氯化氢 |
| A.硬铝——制导线 | B.14C——测定文物年代 |
| C.锗——作半导体材料 | D.Ti-Fe合金——作不锈钢材料 |
(4)已知:在稀硫酸中,MnO
 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
您最近一年使用:0次



