溴化钙是一种溴化物,用于石油钻井,也用于制造溴化铵及光敏纸、灭火剂、制冷剂等。制备CaBr2·2H2O的主要流程如图:
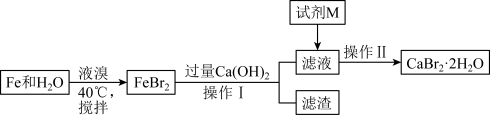
(1)与液溴的反应温度不能超过40℃的原因是____ 。
(2)滤渣的成分可能是____ 。
(3)试剂M是____ ,加入M的目的是____ 。
(4)操作Ⅱ的步骤为蒸发浓缩、____ 、洗涤、干燥
(5)将氨气通入石灰乳,加入溴,于65℃进行反应也可制得溴化钙,此反应中还会生成一种无色无味气体,写出反应的化学方程式____ 。
(6)制得的CaBr2·2H2O可以通过以下方法测定纯度:称取10.00g样品溶于水,滴入足量Na2CO3溶液,充分反应后过滤,将滤渣洗涤、烘干、冷却,称量。得到3.50g固体,则CaBr2·2H2O的质量分数为____ 。

(1)与液溴的反应温度不能超过40℃的原因是
(2)滤渣的成分可能是
(3)试剂M是
(4)操作Ⅱ的步骤为蒸发浓缩、
(5)将氨气通入石灰乳,加入溴,于65℃进行反应也可制得溴化钙,此反应中还会生成一种无色无味气体,写出反应的化学方程式
(6)制得的CaBr2·2H2O可以通过以下方法测定纯度:称取10.00g样品溶于水,滴入足量Na2CO3溶液,充分反应后过滤,将滤渣洗涤、烘干、冷却,称量。得到3.50g固体,则CaBr2·2H2O的质量分数为
更新时间:2020-08-02 08:46:50
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】现将氯气和空气(不参与反应)以体积比约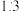 混合通入含水8%的碳酸钠中制备
混合通入含水8%的碳酸钠中制备 (该反应放热),并用水吸收
(该反应放热),并用水吸收 制备次氯酸溶液,装置如图所示:
制备次氯酸溶液,装置如图所示:
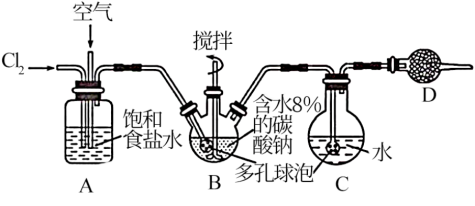
已知:常温常压下,一氧化二氯( )为有毒气体。浓度较高时易与其他物质发生燃烧、爆炸。
)为有毒气体。浓度较高时易与其他物质发生燃烧、爆炸。 以上易分解,极易溶于水并与水反应生成
以上易分解,极易溶于水并与水反应生成 。
。
(1)实验室可用 与浓
与浓 在常温下制备
在常温下制备 ,其化学反应方程式是
,其化学反应方程式是_______ 。
(2)装置 中通入空气的目的是
中通入空气的目的是_______ ,饱和食盐水的作用是_______ 。
(3)装置 需置于冰水中,否则进入C中的
需置于冰水中,否则进入C中的 会大量减少,其原因是
会大量减少,其原因是_______ 。
(4)装置C中制取 的化学反应方程式是
的化学反应方程式是_______ 。
(5)装置 的作用是吸收尾气中的
的作用是吸收尾气中的 、
、 等,装置
等,装置 内适宜填充的试剂是
内适宜填充的试剂是_______ 。(填字母)
A.浓硫酸 B. 碱石灰 C. 氯化钙 D. 石灰水
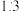 混合通入含水8%的碳酸钠中制备
混合通入含水8%的碳酸钠中制备 (该反应放热),并用水吸收
(该反应放热),并用水吸收 制备次氯酸溶液,装置如图所示:
制备次氯酸溶液,装置如图所示:
已知:常温常压下,一氧化二氯(
 )为有毒气体。浓度较高时易与其他物质发生燃烧、爆炸。
)为有毒气体。浓度较高时易与其他物质发生燃烧、爆炸。 以上易分解,极易溶于水并与水反应生成
以上易分解,极易溶于水并与水反应生成 。
。(1)实验室可用
 与浓
与浓 在常温下制备
在常温下制备 ,其化学反应方程式是
,其化学反应方程式是(2)装置
 中通入空气的目的是
中通入空气的目的是(3)装置
 需置于冰水中,否则进入C中的
需置于冰水中,否则进入C中的 会大量减少,其原因是
会大量减少,其原因是(4)装置C中制取
 的化学反应方程式是
的化学反应方程式是(5)装置
 的作用是吸收尾气中的
的作用是吸收尾气中的 、
、 等,装置
等,装置 内适宜填充的试剂是
内适宜填充的试剂是A.浓硫酸 B. 碱石灰 C. 氯化钙 D. 石灰水
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提取碘的方法之一,其流程如下:

资料显示:
Ⅰ.pH=2 时, NaNO2溶液只能将 I-氧化为 I2,同时生成 NO;
Ⅱ.I2+5Cl2+6H2O=2HIO3+10HCl;
Ⅲ.I2在碱性溶液中反应生成 I-和 IO 。
。
(1)反应①的离子方程式___________ 。
(2)方案甲中,根据 I2的特性,分离操作 X 应为___________ 、___________ 。
(3)Cl2、酸性 KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的 I-却选择了价格较高的NaNO2,原因是___________ 。
(4)写出反应②的离子反应方程式___________
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的 I2、I-。 请检验滤液中的 I-,将实验方案补充完整。实验中可供选择的试剂:稀 H2SO4、淀粉溶液、Fe2(SO4)3溶液。
A.将滤液___________ ,直到水层用淀粉溶液检验不出碘单质存在。
B.从水层取少量溶液于试管中,___________ 。

资料显示:
Ⅰ.pH=2 时, NaNO2溶液只能将 I-氧化为 I2,同时生成 NO;
Ⅱ.I2+5Cl2+6H2O=2HIO3+10HCl;
Ⅲ.I2在碱性溶液中反应生成 I-和 IO
 。
。 (1)反应①的离子方程式
(2)方案甲中,根据 I2的特性,分离操作 X 应为
(3)Cl2、酸性 KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的 I-却选择了价格较高的NaNO2,原因是
(4)写出反应②的离子反应方程式
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的 I2、I-。 请检验滤液中的 I-,将实验方案补充完整。实验中可供选择的试剂:稀 H2SO4、淀粉溶液、Fe2(SO4)3溶液。
A.将滤液
B.从水层取少量溶液于试管中,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】纯 遇热易发生分解,工业上通常制成
遇热易发生分解,工业上通常制成 固体以便运输和储存。制备
固体以便运输和储存。制备 的实验装置如图所示(夹持装置省略),其中A装置制备
的实验装置如图所示(夹持装置省略),其中A装置制备 ,C装置用于制备
,C装置用于制备 。回答下列问题:
。回答下列问题:
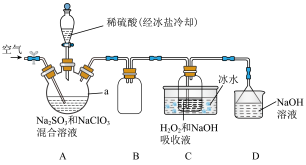
(1)仪器a的名称是___________ 。装置B的作用是___________ 。
(2)装置A中发生反应的离子方程式为___________ 。向装置A中通入空气的目的是___________ 。
(3)装置C中发生反应的化学方程式为___________ ;C装置采用“冰水浴”的目的是___________ 。
(4)研究测得C装置吸收液中的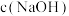 与
与 对粗产品中
对粗产品中 含量的影响如图所示。则最佳条件为
含量的影响如图所示。则最佳条件为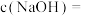
___________  ,
,
___________ 。

 遇热易发生分解,工业上通常制成
遇热易发生分解,工业上通常制成 固体以便运输和储存。制备
固体以便运输和储存。制备 的实验装置如图所示(夹持装置省略),其中A装置制备
的实验装置如图所示(夹持装置省略),其中A装置制备 ,C装置用于制备
,C装置用于制备 。回答下列问题:
。回答下列问题:
(1)仪器a的名称是
(2)装置A中发生反应的离子方程式为
(3)装置C中发生反应的化学方程式为
(4)研究测得C装置吸收液中的
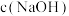 与
与 对粗产品中
对粗产品中 含量的影响如图所示。则最佳条件为
含量的影响如图所示。则最佳条件为
 ,
,

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】在下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A.D为金属单质,其他为化合物。试推断:

(1)写出下列物质的化学式:A:________ B:________ G:________
(2)写出下列反应的化学方程式或离子方程式:
C→F的离子方程式________________________________________
C→E的化学方程式________________________________________
H→I的化学方程式________________________________________

(1)写出下列物质的化学式:A:
(2)写出下列反应的化学方程式或离子方程式:
C→F的离子方程式
C→E的化学方程式
H→I的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下列物质之间有如下反应关系:

已知由E转化成C的现象是:白色沉淀迅速变为灰绿色,最后变为红褐色。回答:
(1)写出下列物质的化学式:A___ ,D___ ,甲___ ,丙___ 。
(2)写出红棕色粉末的一种用途___ 。
(3)写出E→C反应的化学方程式___ 。
(4)将饱和的B溶液滴入沸水中所得分散系中分散质颗粒直径范围为___ 。
(5)写出反应②的离子方程式___ ,该反应中,如果有5.6g铁粉完全反应则生成D的物质的量为___ mol。

已知由E转化成C的现象是:白色沉淀迅速变为灰绿色,最后变为红褐色。回答:
(1)写出下列物质的化学式:A
(2)写出红棕色粉末的一种用途
(3)写出E→C反应的化学方程式
(4)将饱和的B溶液滴入沸水中所得分散系中分散质颗粒直径范围为
(5)写出反应②的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】框图所示的转化关系中,A、C均为常见的金属单质,A、C在冷的H的浓溶液中均会发生钝化;E为固体非金属单质。B为红色固体氧化物,X为常见的无色液体.L焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去)

请回答以下问题:
(1)含碳量在0.03%~2%之间的C的合金,是目前世界上使用量最大的合金,这种合金是___________ ;
A.铝合金 B.青铜 C.镁合金 D.钢铁
(2)F的化学式为________________ ;
(3)K与氨水反应的离子方程式为______________________ ;
(4)A与B生成C和D的反应是___________ (填“放出”或“吸收”)大量热量的反应;
(5)D与L反应的离子方程式为_________________________ 。

请回答以下问题:
(1)含碳量在0.03%~2%之间的C的合金,是目前世界上使用量最大的合金,这种合金是
A.铝合金 B.青铜 C.镁合金 D.钢铁
(2)F的化学式为
(3)K与氨水反应的离子方程式为
(4)A与B生成C和D的反应是
(5)D与L反应的离子方程式为
您最近一年使用:0次
【推荐1】工业上可用红土镍矿(主贾成分为NiO、FeO、Fe2O3)制备镍并回收副产物黄铵铁矾 [化学式可表示为(NH4)xFey(SO4)z(OH)w,摩尔质量为480 g·mol-1]的上艺流程如下。
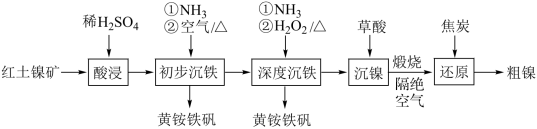
(1)“初步沉铁”中鼓入“空气”的作用是___________ 。
(2)“深度沉铁”时溶液保持的温度比“初步沉铁”时溶液保持的温度低的原因是___________ 。检验深度沉铁完全的方法是___________ 。
(3)已知几种金属离子的氢氧化物开始沉淀和沉淀完全时的pH如下表所示。
“深度沉铁”中通入NH3调节溶液pH的范围是___________ 。
(4)灼烧时得到Ni2O3,请写出灼烧的化学反应方程式为___________ 。
(5)粗镍提纯后,可用于高功率Ni MH( M表示储氢合金)电池。该电池已用于混合动力汽车。总反应方程式如下:Ni(OH)2+M NiOOH +MH。充电时阳极的电板反应方程式为
NiOOH +MH。充电时阳极的电板反应方程式为___________ 。
(6)Min Ristic等曾对黄铵铁矾进行热分解实验。其结果可用下图热重曲线表示(已知:黄铵铁矾在300℃前分解释放的物质为H2O,300-575℃之间只有NH3和H2O放出,此时残留固体只存在Fe、O、S三种元素,670℃以上得到的是纯净的红棕色粉末)。
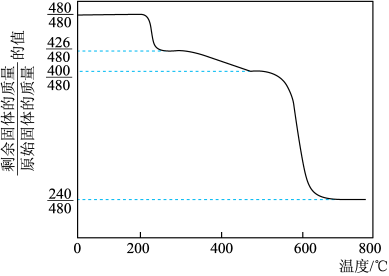
根据以上实验及图中数据确定黄铵铁矾的化学式为___________ 。

(1)“初步沉铁”中鼓入“空气”的作用是
(2)“深度沉铁”时溶液保持的温度比“初步沉铁”时溶液保持的温度低的原因是
(3)已知几种金属离子的氢氧化物开始沉淀和沉淀完全时的pH如下表所示。
| 金属离子的氢氧化物 | Ni(OH)2 | Fe(OH)3 | 黄铵铁矾 |
| 开始沉淀pH | 7.2 | 2.7 | 1.3 |
| 沉淀刚好完全pH | 9.2 | 3.7 | 2.3 |
“深度沉铁”中通入NH3调节溶液pH的范围是
(4)灼烧时得到Ni2O3,请写出灼烧的化学反应方程式为
(5)粗镍提纯后,可用于高功率Ni MH( M表示储氢合金)电池。该电池已用于混合动力汽车。总反应方程式如下:Ni(OH)2+M
 NiOOH +MH。充电时阳极的电板反应方程式为
NiOOH +MH。充电时阳极的电板反应方程式为(6)Min Ristic等曾对黄铵铁矾进行热分解实验。其结果可用下图热重曲线表示(已知:黄铵铁矾在300℃前分解释放的物质为H2O,300-575℃之间只有NH3和H2O放出,此时残留固体只存在Fe、O、S三种元素,670℃以上得到的是纯净的红棕色粉末)。

根据以上实验及图中数据确定黄铵铁矾的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】NiCl2是一种重要催化剂。某科研小组以废弃催化剂(含Ni2+、Cu2+、Fe3+、Ca2+、Mg2+等)为原料,按下列流程回收NiCl2·6H2O晶体,回答下列问题。
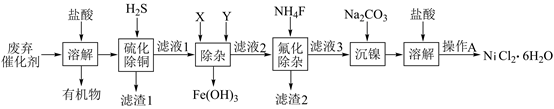
已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的成分主要是_______ 。
(2)若X为Cl2,则其发生的离子方程式是_______ 。若用H2O2代替Cl2,试剂Y的使用量会减少,原因是_______ 。
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于_______ mol/L。
(4)实际生产中,产生的滤渣均需进行洗涤,并将洗涤液与滤液合并,此操作的目的是_______ 。操作A为_______ 、冷却结晶、过滤、洗涤。
(5)将所得NiCl2·6H2O与SOCI2混合加热可制备无水 NiCl2,反应的方程式为_______ 。
(6)产品中镍的质量分数[ω(Ni)]测定:准确称取0.3000g产品于锥形瓶内,依次加入25 mL水、0.5g氟化钠、10 mL氨性缓冲溶液、约0.1g紫脲酸铵指示剂,摇匀,用0.0500 mol/L的 EDTA(Na2H2Y)标准液滴定至试液呈紫红色为终点,消耗标准液体积22.40mL,反应为Ni2++H2Y2-=NiY2-+2H+,则样品中ω(Ni)为_______ (保留两位有效数字)。

已知:Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9
(1)滤渣1的成分主要是
(2)若X为Cl2,则其发生的离子方程式是
(3)氟化除杂时要保证完全除去Ca2+和Mg2+(离子浓度≤10-5mol/L),滤液3中c(F-)不小于
(4)实际生产中,产生的滤渣均需进行洗涤,并将洗涤液与滤液合并,此操作的目的是
(5)将所得NiCl2·6H2O与SOCI2混合加热可制备无水 NiCl2,反应的方程式为
(6)产品中镍的质量分数[ω(Ni)]测定:准确称取0.3000g产品于锥形瓶内,依次加入25 mL水、0.5g氟化钠、10 mL氨性缓冲溶液、约0.1g紫脲酸铵指示剂,摇匀,用0.0500 mol/L的 EDTA(Na2H2Y)标准液滴定至试液呈紫红色为终点,消耗标准液体积22.40mL,反应为Ni2++H2Y2-=NiY2-+2H+,则样品中ω(Ni)为
您最近一年使用:0次
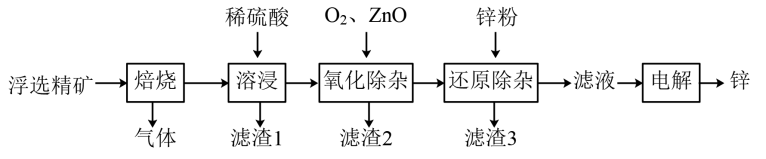
【推荐3】我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)滤渣1的主要成分除SiO2外还有___ ;氧化除杂工序中ZnO的作用是___ ,若不通入氧气,其后果是___ 。
(2)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为_______ 。
(3)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为_____ ;沉积锌后的电解液可返回_____ 工序继续使用。

相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
(1)滤渣1的主要成分除SiO2外还有
(2)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为
(3)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】黄铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,其综合利用对环境保护具有现实意义。利用黄铁矿烧渣为原料制备高档颜料—铁红(Fe2O3)的流程如下:
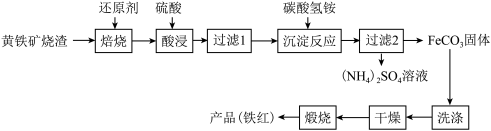
回答下列问题:
(1)“焙烧”时所添加的最佳还原剂是________ (填序号)。
a.焦炭 b.硫黄 c.镁粉 d.锌粉
(2)“过滤1”后的滤液中溶质的主要成分是________________ (填化学式)。
(3)“沉淀反应”时不宜混入过多空气,其原因为______________________ (用离子方程式表示)。
(4)为检验FeCO3是否洗涤干净,可以向最后一次洗涤液中滴加________ 溶液。
(5)在空气中煅烧FeCO3生成铁红和另一种氧化物,反应的化学方程式为________ 。
(6)现有黄铁矿烧渣500t,铁元素的质量分数为16.8%,经过一系列转化后,得到90t铁红,该产品的产率为________ 。(提示: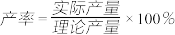 )
)

回答下列问题:
(1)“焙烧”时所添加的最佳还原剂是
a.焦炭 b.硫黄 c.镁粉 d.锌粉
(2)“过滤1”后的滤液中溶质的主要成分是
(3)“沉淀反应”时不宜混入过多空气,其原因为
(4)为检验FeCO3是否洗涤干净,可以向最后一次洗涤液中滴加
(5)在空气中煅烧FeCO3生成铁红和另一种氧化物,反应的化学方程式为
(6)现有黄铁矿烧渣500t,铁元素的质量分数为16.8%,经过一系列转化后,得到90t铁红,该产品的产率为
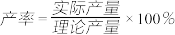 )
)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】硫化铋(Bi2S3)广泛应用于太阳能电池、光电二极管及红外光谱学等。以铋矿渣(含Bi2O3、Fe2O3、CuO、Ag2O、Al2O3等)为原料制备Bi2S3的一种工艺流程如下。
②该工艺条件下,部分金属离子形成氢氧化物沉淀的pH如下表:
③常温下,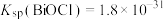 、
、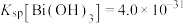 。
。
请回答下列问题:
(1)提高“酸浸”反应速率的措施是___________ (任答1条);“酸浸”中,形成“滤渣”的主要反应的离子方程式是___________ 。
(2)“滤液a”中主要的金属阳离有Fe3+、Cu2+___________ 。
(3)“沉铋”后所得BiOCl固体中含 杂质,设计实验去除BiOCl固体中含有的
杂质,设计实验去除BiOCl固体中含有的 杂质:
杂质:___________ 。
(4)“酸溶”时需加入过量的盐酸,盐酸过量的目的是___________ 、___________ 。
(5)已知常温时,BiOCl在水溶液中存在平衡: ,该反应的平衡常数为K,达到平衡时测得溶液pH=13,
,该反应的平衡常数为K,达到平衡时测得溶液pH=13,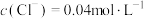 ,则K=
,则K=___________ 。
(6)化合物X的VSEPR模型是___________ 。
(7)已知 (硫代乙酰胺)
(硫代乙酰胺)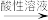
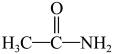 (乙酰胺)+H2S,则“硫化”的离子方程式为
(乙酰胺)+H2S,则“硫化”的离子方程式为___________ 。
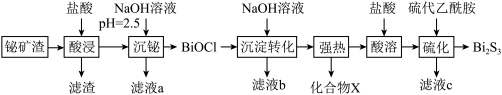
②该工艺条件下,部分金属离子形成氢氧化物沉淀的pH如下表:
| 离子 | Fe3+ | Al3+ | Cu2+ |
| 开始沉淀时的pH | 1.5 | 3.6 | 4.5 |
| 沉淀完全时的pH | 3.2 | 4.7 | 6.7 |
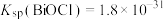 、
、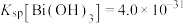 。
。请回答下列问题:
(1)提高“酸浸”反应速率的措施是
(2)“滤液a”中主要的金属阳离有Fe3+、Cu2+
(3)“沉铋”后所得BiOCl固体中含
 杂质,设计实验去除BiOCl固体中含有的
杂质,设计实验去除BiOCl固体中含有的 杂质:
杂质:(4)“酸溶”时需加入过量的盐酸,盐酸过量的目的是
(5)已知常温时,BiOCl在水溶液中存在平衡:
 ,该反应的平衡常数为K,达到平衡时测得溶液pH=13,
,该反应的平衡常数为K,达到平衡时测得溶液pH=13,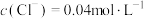 ,则K=
,则K=(6)化合物X的VSEPR模型是
(7)已知
 (硫代乙酰胺)
(硫代乙酰胺)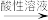
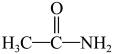 (乙酰胺)+H2S,则“硫化”的离子方程式为
(乙酰胺)+H2S,则“硫化”的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域有重要用途。某兴趣小组用四氯化硅与氮气在氢气气氛保护下,加热发生反应,可得较高纯度的氮化硅及氯化氢,设计如图所示装置。
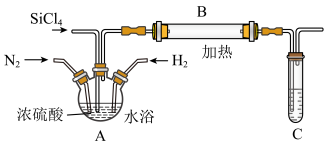
试回答下列问题:
(1)实验室制备氢气常用锌和稀硫酸反应,制取时常在反应混合物中加入少量硫酸铜溶液,其目的是_______ 。
(2)图中装置A的作用是_______ 、调节通入气体速率和充分混合气体。通过观察_______ ,来调节通入气体的速率。
(3)加热B玻璃管之前,为防止意外发生,必须进行的操作是_______ (不用详述步骤),B中发生反应的化学方程式为_______ 。
(4)四氯化硅与水反应生成两种酸,写出用烧碱溶液吸收尾气中四氯化硅的化学方程式:_______ 。

试回答下列问题:
(1)实验室制备氢气常用锌和稀硫酸反应,制取时常在反应混合物中加入少量硫酸铜溶液,其目的是
(2)图中装置A的作用是
(3)加热B玻璃管之前,为防止意外发生,必须进行的操作是
(4)四氯化硅与水反应生成两种酸,写出用烧碱溶液吸收尾气中四氯化硅的化学方程式:
您最近一年使用:0次



