著名化学家徐光宪在稀土化学等领域取得了卓越成就,被誉为“稀土界的袁隆平”。稀土元素包括钪、钇和镧系元素。请回答下列问题:
(1)写出基态Sc原子的核外电子排布式_________ ,其中电子占据的轨道数目为_________ 。
(2)在用重量法测定镧系元素和使镧系元素分离时,总是使之先转换成草酸盐,然后经过灼烧而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3·nH2O+6HCl。
①HOOC-COOH中碳原子的杂化轨道类型为____ ,其中H、C、O的电负性由大到小的顺序为____ 。
②H2O的VSEPR模型为_____ ,写出与H2O互为等电子体的一种阴离子的化学式_____ 。
③HCl和H2O可以形成相对稳定的水合氢离子盐晶体,如HCl·2H2O,HCl·2H2O中含有H5O ,结构为
,结构为 ,在该离子中,存在的作用力有
,在该离子中,存在的作用力有__________ 。
a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键 f.氢键 g.范德华力 h.π键 i.σ键
(3)据报道,在MnO2的催化下,甲醛(HCHO)可被氧化成CO2,则甲醛(HCHO)中的键角____ CO2中的键角(填“=”“>”或“<”)
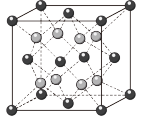
(4)PrO2(二氧化镨)的晶胞结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点。Pr(镨)的配位数________ 。假设相距最近的Pr原子与O原子之间的距离为a pm,则该晶体的密度为____ g⋅cm−3(用NA表示阿伏加 德罗常数的值,不必计算出结果)。已知M(Pr)=141g/mol,M(O)=16g/mol
(1)写出基态Sc原子的核外电子排布式
(2)在用重量法测定镧系元素和使镧系元素分离时,总是使之先转换成草酸盐,然后经过灼烧而得其氧化物,如2LnCl3+3H2C2O4+nH2O=Ln2(C2O4)3·nH2O+6HCl。
①HOOC-COOH中碳原子的杂化轨道类型为
②H2O的VSEPR模型为
③HCl和H2O可以形成相对稳定的水合氢离子盐晶体,如HCl·2H2O,HCl·2H2O中含有H5O
 ,结构为
,结构为 ,在该离子中,存在的作用力有
,在该离子中,存在的作用力有a.配位键 b.极性键 c.非极性键 d.离子键 e.金属键 f.氢键 g.范德华力 h.π键 i.σ键
(3)据报道,在MnO2的催化下,甲醛(HCHO)可被氧化成CO2,则甲醛(HCHO)中的键角
(4)PrO2(二氧化镨)的晶胞结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点。Pr(镨)的配位数

更新时间:2020-09-17 08:15:43
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
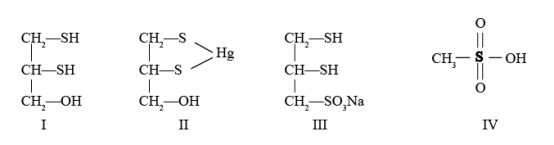
【推荐1】很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
(1)基态硫原子价电子排布式为_______ 。
(2)H2S、CH4、H2O的沸点由高到低顺序为_______ 。
(3)汞的原子序数为80,位于元素周期表第_______ 周期第ⅡB族。
(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______ 。
A. 在I中S原子采取sp3杂化
B. 在Ⅱ中S元素的电负性最大
C. 在Ⅲ中C-C-C键角是180°
D. 在Ⅲ中存在离子键与共价键
E. 在Ⅳ中硫氧键的键能均相等
(5)汞解毒剂的水溶性好,有利于体内 重金属元素汞的解毒。化合物I与化合物Ⅲ相比,水溶性较好的是_______ 。
(6)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图9a所示)中部分Ge原子被Hg和Sb取代后形成。
②图9c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为_______ ;该晶胞中粒子个数比Hg:Ge:Sb = _______ 。
③设X的最简式的式量为Mr,则X晶体的密度为_______ g/cm3(列出算式)。

(1)基态硫原子价电子排布式为
(2)H2S、CH4、H2O的沸点由高到低顺序为
(3)汞的原子序数为80,位于元素周期表第
(4)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有
A. 在I中S原子采取sp3杂化
B. 在Ⅱ中S元素的电负性最大
C. 在Ⅲ中C-C-C键角是180°
D. 在Ⅲ中存在离子键与共价键
E. 在Ⅳ中硫氧键的键能均相等
(5)汞解毒剂的水溶性好,有利于体内 重金属元素汞的解毒。化合物I与化合物Ⅲ相比,水溶性较好的是
(6)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图9a所示)中部分Ge原子被Hg和Sb取代后形成。

①图9b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是
②图9c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为
③设X的最简式的式量为Mr,则X晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】含第VA族的磷、砷(As)等元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)基态P原子的核外电子排布式为____ ,有____ 个未成对电子。
(2)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图甲所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CC14、SF6互为等电子体,则A为____ ,其中心原子杂化轨道类型为____ ,B为____ 。
(3)PO43-的空间构型为____ ,其等电子体有____ (请写出一种)。
(4)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。已知砷化镓的晶胞结构如图乙,晶胞参数a= 565pm。

①砷化镓的化学式为____ ,镓原子的配位数为____ 。
②砷化镓的晶胞密度=____ g/cm3(列式并计算,精确到小数点后两位),m位置Ga原子与n位置As原子之间的距离为____ pm(列式表示)。
(1)基态P原子的核外电子排布式为
(2)常温下PCl5是一种白色晶体,其立方晶系晶体结构模型如图甲所示,由A、B两种微粒构成。将其加热至148℃熔化,形成一种能导电的熔体。已知A、B两种微粒分别与CC14、SF6互为等电子体,则A为
(3)PO43-的空间构型为
(4)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是普通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。已知砷化镓的晶胞结构如图乙,晶胞参数a= 565pm。

①砷化镓的化学式为
②砷化镓的晶胞密度=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】Al、Fe、Cu 是重要的材料元素,在生产生活中有着广泛的应用。请回答下列问题:
(1)基态Fe 的价电子排布图为_______ 。
(2)已知Al 的第一电离能为 578kJ/mol、第二电离能为 1817 kJ/mol、第三电离能为 2745 kJ/mol、第四电离能为 11575 kJ/mol。 请解释其第二电离能增幅较大的原因_______ 。
(3)已知氯化铝熔点为 194℃, 熔融状态下不导电且容易升华,由此可判断氯化铝属于_______ 晶体。
(4)铁系元素能与 CO 形成 Fe(CO)5、Ni(CO)4等金属羰基配合物。 与 CO 互为等电子体的分子和离子分别为_______ 和_______ (各举一种,填化学式);CO 共有_______ 对孤电子对。
(5)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]SO4溶液,该溶液可用于溶解纤维素。在[Cu(NH3)4]SO4中,配离子所含有的化学键为_______ ,提供孤电子对的成键原子是_______ 。
(6)碳酸亚铁中所含非金属元素的电负性由大到小的顺序为_______ (用元素符号表示)。
(7)当温度升高到 912℃,铁转变为面心立方堆积方式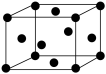 ,距离一个顶点铁原子最近的铁原子有
,距离一个顶点铁原子最近的铁原子有_______ 个,若晶胞边长为a cm,Fe 的摩尔质量为M g·mol-1,阿伏加德罗常数的值为 NA,Fe 晶体的密度ρ=_______ g·cm-3(用含 a、M、NA的代数式表示)。
(1)基态Fe 的价电子排布图为
(2)已知Al 的第一电离能为 578kJ/mol、第二电离能为 1817 kJ/mol、第三电离能为 2745 kJ/mol、第四电离能为 11575 kJ/mol。 请解释其第二电离能增幅较大的原因
(3)已知氯化铝熔点为 194℃, 熔融状态下不导电且容易升华,由此可判断氯化铝属于
(4)铁系元素能与 CO 形成 Fe(CO)5、Ni(CO)4等金属羰基配合物。 与 CO 互为等电子体的分子和离子分别为
(5)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]SO4溶液,该溶液可用于溶解纤维素。在[Cu(NH3)4]SO4中,配离子所含有的化学键为
(6)碳酸亚铁中所含非金属元素的电负性由大到小的顺序为
(7)当温度升高到 912℃,铁转变为面心立方堆积方式
 ,距离一个顶点铁原子最近的铁原子有
,距离一个顶点铁原子最近的铁原子有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质。
(1)基态铜原子的电子排布式为_____________ ;已知高温下4CuO 2Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是
2Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是___________________________ 。
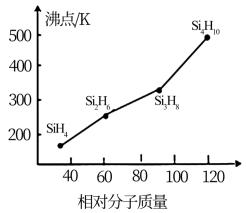
(2)硒、硅均能与氢元素形成气态氢化物,则它们形成的最简单的氢化物中,分子构型分别为____________ , 若“Si-H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se____ Si (填“>”、“<”)。人们把硅与氢元素形成的一类化合物叫硅烷。硅烷的组成、结构与相应的烷烃相似,硅烷的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是________________________________ 。
(3)与铟、镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤电子对的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3。BF3·NH3中B原子的杂化轨道类型为______ , B与N之间形成___________ 键。
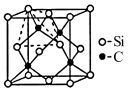
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如下图所示,则金刚砂晶体类型为_________ ,在SiC中,每个C原子周围最近的C原子数目为___ 个;若晶胞的边长为a pm,则金刚砂的密度为____ g/cm3(用NA表示阿伏伽德罗常数的值)。
(1)基态铜原子的电子排布式为
 2Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是
2Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是(2)硒、硅均能与氢元素形成气态氢化物,则它们形成的最简单的氢化物中,分子构型分别为

(3)与铟、镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤电子对的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3。BF3·NH3中B原子的杂化轨道类型为
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如下图所示,则金刚砂晶体类型为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
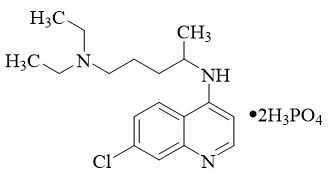
【推荐2】2020年2月15日,由国家科研攻关组的主要成员单位的专家组共同研判磷酸氯喹在细胞水平上能有效抑制新型冠状病毒( )的感染。已知磷酸氯喹的结构如图所示。
)的感染。已知磷酸氯喹的结构如图所示。
(1)基态磷原子的外围电子排布式:_______
(2)磷酸氯喹中N原子的杂化方式为_______ 。
(3) 中
中 的空间构型为
的空间构型为_______ 。
(4)磷酸氯喹所含C、N、O三种元素的第一电离能由大到小的顺序为_______ 。
(5)氨硼烷 是一种潜在的储氢材料,它可由六元环状化合物
是一种潜在的储氢材料,它可由六元环状化合物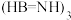 通过反应:
通过反应: 制得。
制得。
①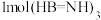 分子中有
分子中有_______  键。
键。
②氨硼烷在高温下释放氢后生成的立方氮化硼晶体具有类似金刚石的结构,但熔点比金刚石低,原因是_______ 。
 )的感染。已知磷酸氯喹的结构如图所示。
)的感染。已知磷酸氯喹的结构如图所示。
(1)基态磷原子的外围电子排布式:
(2)磷酸氯喹中N原子的杂化方式为
(3)
 中
中 的空间构型为
的空间构型为(4)磷酸氯喹所含C、N、O三种元素的第一电离能由大到小的顺序为
(5)氨硼烷
 是一种潜在的储氢材料,它可由六元环状化合物
是一种潜在的储氢材料,它可由六元环状化合物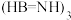 通过反应:
通过反应: 制得。
制得。①
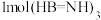 分子中有
分子中有 键。
键。②氨硼烷在高温下释放氢后生成的立方氮化硼晶体具有类似金刚石的结构,但熔点比金刚石低,原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】20世纪50年代科学家提出价层电子对互斥模型(简称VSEPR模型),用于预测简单分子的空间结构。其要点可以概括为:
Ⅰ、用 表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子价层未参与成键的电子对(称为孤电子对),
表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子价层未参与成键的电子对(称为孤电子对), 称为价电子对数。分子中的价电子对总是互相排斥,均匀地分布在中心原子周围的空间。
称为价电子对数。分子中的价电子对总是互相排斥,均匀地分布在中心原子周围的空间。
Ⅱ、分子的空间结构是指分子中的原子在空间的排布,不包括中心原子未成键的孤电子对。
Ⅲ、分子中价电子对之间的斥力的主要顺序为:
ⅰ、孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;
ⅱ、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;
ⅲ、X原子得电子能力越弱, 形成的共用电子对之间的斥力越强;
形成的共用电子对之间的斥力越强;
ⅳ、其他。
请仔细阅读上述材料,回答下列问题:
(1)由 的VSEPR模型填写下表:
的VSEPR模型填写下表:
(2)请用VSEPR模型解释 为直线形分子的原因:
为直线形分子的原因:___________ 。
(3) 分子的空间结构为
分子的空间结构为___________ ,请你预测水分子中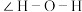 的大小范围并解释原因:
的大小范围并解释原因:___________ 。
(4) 和
和 都属于
都属于 型分子,S、O之间以双键结合,S与
型分子,S、O之间以双键结合,S与 、S与F之间以单键结合。请你预测
、S与F之间以单键结合。请你预测 和
和 分子的空间结构:
分子的空间结构:___________ 。
Ⅰ、用
 表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子价层未参与成键的电子对(称为孤电子对),
表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子价层未参与成键的电子对(称为孤电子对), 称为价电子对数。分子中的价电子对总是互相排斥,均匀地分布在中心原子周围的空间。
称为价电子对数。分子中的价电子对总是互相排斥,均匀地分布在中心原子周围的空间。Ⅱ、分子的空间结构是指分子中的原子在空间的排布,不包括中心原子未成键的孤电子对。
Ⅲ、分子中价电子对之间的斥力的主要顺序为:
ⅰ、孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;
ⅱ、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;
ⅲ、X原子得电子能力越弱,
 形成的共用电子对之间的斥力越强;
形成的共用电子对之间的斥力越强;ⅳ、其他。
请仔细阅读上述材料,回答下列问题:
(1)由
 的VSEPR模型填写下表:
的VSEPR模型填写下表: | 2 | ① |
| 价电子对分布的几何构型 | ② | 四面体形 |
| 价电子对之间的键角 | ③ |  |
(2)请用VSEPR模型解释
 为直线形分子的原因:
为直线形分子的原因:(3)
 分子的空间结构为
分子的空间结构为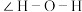 的大小范围并解释原因:
的大小范围并解释原因:(4)
 和
和 都属于
都属于 型分子,S、O之间以双键结合,S与
型分子,S、O之间以双键结合,S与 、S与F之间以单键结合。请你预测
、S与F之间以单键结合。请你预测 和
和 分子的空间结构:
分子的空间结构:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为_____________________ 。
(2)锗、砷、硒的第一电离能大小排序为_____________ 。
(3)H2SeO3的中心原子杂化类型是____________ ;SeO 的立体构型是
的立体构型是___________ 。与SeO 互为等电体的分子有(写一种物质的化学式即可)
互为等电体的分子有(写一种物质的化学式即可)________________ 。
(4)H2Se属于______ (填:极性或非极性)分子;单质硒的熔点为217℃,它属于________ 晶体。
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,若该晶胞密度为ρg•cm-3,硒化锌的摩尔质量为M g/mol。NA代表阿伏加德罗常数,则晶胞参数a为_________________ pm。

(1)基态硒原子的价层电子排布式为
(2)锗、砷、硒的第一电离能大小排序为
(3)H2SeO3的中心原子杂化类型是
 的立体构型是
的立体构型是 互为等电体的分子有(写一种物质的化学式即可)
互为等电体的分子有(写一种物质的化学式即可)(4)H2Se属于
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,若该晶胞密度为ρg•cm-3,硒化锌的摩尔质量为M g/mol。NA代表阿伏加德罗常数,则晶胞参数a为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】碳元素的单质有多种形式,不同单质结构不同。
(1)石墨和金刚石的结构图如下。___________ ,石墨属于___________ 晶体。
②金刚石中,碳原子杂化类型为___________ 。
③已知金刚石晶胞的棱长为acm,阿伏加德罗常数的值为NA,则金刚石晶体密度
___________ 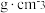 (用代数式表示)。
(用代数式表示)。
④石墨烯一定条件下,可转化为C60.某金属M与C60可制备一种低温超导材料,晶胞如图所示。M原子位于晶胞的棱上与内部,该材料的化学式为___________ 。___________ (填字母)。
b.C60熔点高于金刚石
c.一个C60分子中,σ键数目为120个
d.“纳米车”的诞生,说明人类已经可以在分子层面进行组装操作
(1)石墨和金刚石的结构图如下。

②金刚石中,碳原子杂化类型为
③已知金刚石晶胞的棱长为acm,阿伏加德罗常数的值为NA,则金刚石晶体密度

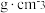 (用代数式表示)。
(用代数式表示)。④石墨烯一定条件下,可转化为C60.某金属M与C60可制备一种低温超导材料,晶胞如图所示。M原子位于晶胞的棱上与内部,该材料的化学式为


b.C60熔点高于金刚石
c.一个C60分子中,σ键数目为120个
d.“纳米车”的诞生,说明人类已经可以在分子层面进行组装操作
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】下表为长式周期表的一部分,其中的编号代表对应的元素。
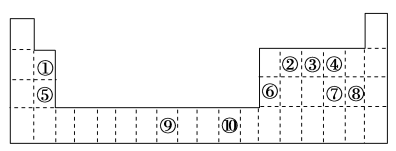
(1)表中位于ds区的元素是________ (填编号),写出该元素基态原子的电子排布式:___________ 。
(2)①和⑧形成的化合物分子中,中心原子的杂化轨道类型为________ ,⑥和⑧形成的化合物的晶体类型是________ 。
(3)②、③、④三种元素中,第一电离能最大的是________ (填编号)。
(4)元素③的简单气态氢化物在水中的溶解度比同族其他元素的氢化物大很多的原因是____________________________________________________________________________________ 。
(5)⑤与④形成的晶体的熔点高于⑤与⑦形成的晶体的熔点,原因____________________________ 。
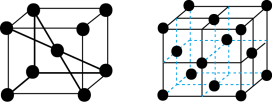
(6)1183K以下,元素⑨的单质为体心立方晶体(晶胞结构如图1),1183K以上转变为面心立方晶体(晶胞结构如图2)。在图2中,与一个原子距离最近且相等的原子个数为________ ,图1与图2所示晶胞中含有的原子个数之比为________ 。

(1)表中位于ds区的元素是
(2)①和⑧形成的化合物分子中,中心原子的杂化轨道类型为
(3)②、③、④三种元素中,第一电离能最大的是
(4)元素③的简单气态氢化物在水中的溶解度比同族其他元素的氢化物大很多的原因是
(5)⑤与④形成的晶体的熔点高于⑤与⑦形成的晶体的熔点,原因

(6)1183K以下,元素⑨的单质为体心立方晶体(晶胞结构如图1),1183K以上转变为面心立方晶体(晶胞结构如图2)。在图2中,与一个原子距离最近且相等的原子个数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铁(Fe)、钴(Co)、镍(Ni)是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体.
(1)基态Co原子的外围电子排布式为________ ,第二周期中基态原子与基态Co原子具有相同未成对电子数的元素是______________ .
(2)Fe、Co、Ni原子半径相似、化学性质相似,原因是_______________ .
(3)配合物Fe(CO)5的中心原子价电子数与配体提供电子总数之和为_________ 。CO与N2互为等电子体,CO分子具有的化学键类型有____________ .
A.σ键 B.π键 C.离子键 D.金属键
(4)Ni(CO)4的结构与相关性质见表,其空间构型为_______ ,Ni的杂化形式为____ ,其为_______ 晶体。
(5)钙钛矿中含有Sn、Ni、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中Sm和O如下图所示,Ni位于O形成正八面体空隙中.晶胞边长为apm,设NA为阿伏加德罗常数的数值,则该氧化物的密度为________ g/cm3(列出计算表达式)。

(6)已知:r(Fe2+)为62pm,r(Co2+)为66pm。在隔绝空气条件下分别加热FeCO3和CoCO3实验测得FeCO3的分解温度低于CoCO3,原因是_______ 。
(1)基态Co原子的外围电子排布式为
(2)Fe、Co、Ni原子半径相似、化学性质相似,原因是
(3)配合物Fe(CO)5的中心原子价电子数与配体提供电子总数之和为
A.σ键 B.π键 C.离子键 D.金属键
(4)Ni(CO)4的结构与相关性质见表,其空间构型为
| 相对分子质量 | 熔点 | 沸点 | 结构 |
| 171 |  | 43℃ |  |

(6)已知:r(Fe2+)为62pm,r(Co2+)为66pm。在隔绝空气条件下分别加热FeCO3和CoCO3实验测得FeCO3的分解温度低于CoCO3,原因是
您最近一年使用:0次
【推荐2】乙烯是重要的有机化学原料,工业上可利用乙烷脱氢制备乙烯。
(1)乙烷裂解为乙烯为自由基反应,其可能的引发反应及对应化学键的解离能如下:
根据表格信息,乙烷裂解引发的反应主要为________________________ 。
(2)经过引发的后续反应历程为(已略去链终止过程):
……
 ΔH1
ΔH1
 ΔH2
ΔH2
①C2H4(g) +H2(g) →C2H6(g)的ΔH=________________________ (用含ΔH1和ΔH2的式子表示)。
②上述历程中“……”所代表的反应为____________________________________ 。
(3)CH3·中的单电子不能占据杂化轨道,则CH3·中碳原子的杂化方式为________________________ 。
(4)乙烷裂解中主要发生的反应及其在不同温度下的平衡常数如下表:
①当裂解反应达到平衡状态时,体系将会产生大量积碳。由表中数据分析,平衡时混合气体中____________ (填化学式)的百分含量最大,原因是______________ 。
②为提高乙烯的产率,工业生产的适宜反应条件为______ (填标号)。
A.高温 较长的反应时间 B.高温 较短的反应时间
C.低温 较长的反应时间 D.低温 较短的反应时间
③在某温度下投入 molC2H6发生上述反应,平衡时混合体系的压强为p,其中C2H6、C2H4、CH4的物质的量分别为mmol、nmol、rmol,未检测出C2H2。则此温度下反应Ⅰ的平衡常数Kp
molC2H6发生上述反应,平衡时混合体系的压强为p,其中C2H6、C2H4、CH4的物质的量分别为mmol、nmol、rmol,未检测出C2H2。则此温度下反应Ⅰ的平衡常数Kp
____________ (以分压表示,分压=总压 物质的量分数)。
物质的量分数)。
(5)工业上制备乙烯常使用Ni-Cr-Fe合金炉,某Ni-Cr-Fe合金的晶胞结构如图所示, 表示Ni原子,
表示Ni原子, 表示Fe原子,由4个Ni原子和2个Fe原子所形成的八面体空隙中心的一半填充Cr原子(如图中
表示Fe原子,由4个Ni原子和2个Fe原子所形成的八面体空隙中心的一半填充Cr原子(如图中 位置),则该合金可表示为
位置),则该合金可表示为__________ (填化学式)。

(1)乙烷裂解为乙烯为自由基反应,其可能的引发反应及对应化学键的解离能如下:
可能的引发反应 | 有关键的解离能( kJ/mol) |
C2H6(g) →C2H5 ·(g) +H·(g) | 410 |
C2H6(g)→ 2CH3·(g) | 368 |
(2)经过引发的后续反应历程为(已略去链终止过程):
……
 ΔH1
ΔH1 ΔH2
ΔH2①C2H4(g) +H2(g) →C2H6(g)的ΔH=
②上述历程中“……”所代表的反应为
(3)CH3·中的单电子不能占据杂化轨道,则CH3·中碳原子的杂化方式为
(4)乙烷裂解中主要发生的反应及其在不同温度下的平衡常数如下表:
反应 | 1100K | 1300K | 1500K |
I.C2H6 C2H4+H2 C2H4+H2 | 1.6 | 18.9 | 72.0 |
II.C2H6  C2H4 +CH4 C2H4 +CH4 | 60.9 | 108.7 | 165.8 |
III.C2H4 C2H2 +H2 C2H2 +H2 | 0.015 | 0.33 | 3.2 |
IV.C2H2 2C+H2 2C+H2 | 6.5×107 | 1.5×106 | 1.0×105 |
②为提高乙烯的产率,工业生产的适宜反应条件为
A.高温 较长的反应时间 B.高温 较短的反应时间
C.低温 较长的反应时间 D.低温 较短的反应时间
③在某温度下投入
 molC2H6发生上述反应,平衡时混合体系的压强为p,其中C2H6、C2H4、CH4的物质的量分别为mmol、nmol、rmol,未检测出C2H2。则此温度下反应Ⅰ的平衡常数Kp
molC2H6发生上述反应,平衡时混合体系的压强为p,其中C2H6、C2H4、CH4的物质的量分别为mmol、nmol、rmol,未检测出C2H2。则此温度下反应Ⅰ的平衡常数Kp
 物质的量分数)。
物质的量分数)。(5)工业上制备乙烯常使用Ni-Cr-Fe合金炉,某Ni-Cr-Fe合金的晶胞结构如图所示,
 表示Ni原子,
表示Ni原子, 表示Fe原子,由4个Ni原子和2个Fe原子所形成的八面体空隙中心的一半填充Cr原子(如图中
表示Fe原子,由4个Ni原子和2个Fe原子所形成的八面体空隙中心的一半填充Cr原子(如图中 位置),则该合金可表示为
位置),则该合金可表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】金属及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)钒广泛用于催化及钢铁工业,基态钒原子的核外电子排布式为______ 。
(2)二茂铁又叫双环戊二烯基铁[ ],熔点是172.5~173℃,100℃以上升华,二茂铁属于
],熔点是172.5~173℃,100℃以上升华,二茂铁属于______ 晶体。
(3)铜可以形成一种离子化合物 ,若要确定
,若要确定 是晶体还是非晶体,最科学的方法是对其进行
是晶体还是非晶体,最科学的方法是对其进行______ 实验,其中阴离子的VSEPR模型是______ 。
(4)钴的配合物 ,配位数是6,把
,配位数是6,把 溶于水后立即加硝酸银溶液,则析出氯化银沉淀。经测定,每1mol
溶于水后立即加硝酸银溶液,则析出氯化银沉淀。经测定,每1mol  只生成1mol AgCl。请写出符合上述条件配合物的化学式:
只生成1mol AgCl。请写出符合上述条件配合物的化学式:______ 。
(5)最近发现,只含镁、镍和碳三种元素的晶体也具有超导性,该物质形成的晶体的立方晶胞结构如图所示。

①与Mg紧邻的Ni有______ 个。
②原子坐标参数可表示晶胞内部各原子的相对位置。该晶胞中原子的坐标参数为a为(0,0,0);b为( ,
, ,0);d为(1,1,1)。则c原子的坐标参数为
,0);d为(1,1,1)。则c原子的坐标参数为______ 。
③若晶胞中Ni、Mg之间的最短距离为a pm,阿伏加 德罗常数的值为NA,则晶体的密度ρ=______  (用含a、NA的代数式表示)。
(用含a、NA的代数式表示)。
(1)钒广泛用于催化及钢铁工业,基态钒原子的核外电子排布式为
(2)二茂铁又叫双环戊二烯基铁[
 ],熔点是172.5~173℃,100℃以上升华,二茂铁属于
],熔点是172.5~173℃,100℃以上升华,二茂铁属于(3)铜可以形成一种离子化合物
 ,若要确定
,若要确定 是晶体还是非晶体,最科学的方法是对其进行
是晶体还是非晶体,最科学的方法是对其进行(4)钴的配合物
 ,配位数是6,把
,配位数是6,把 溶于水后立即加硝酸银溶液,则析出氯化银沉淀。经测定,每1mol
溶于水后立即加硝酸银溶液,则析出氯化银沉淀。经测定,每1mol  只生成1mol AgCl。请写出符合上述条件配合物的化学式:
只生成1mol AgCl。请写出符合上述条件配合物的化学式:(5)最近发现,只含镁、镍和碳三种元素的晶体也具有超导性,该物质形成的晶体的立方晶胞结构如图所示。

①与Mg紧邻的Ni有
②原子坐标参数可表示晶胞内部各原子的相对位置。该晶胞中原子的坐标参数为a为(0,0,0);b为(
 ,
, ,0);d为(1,1,1)。则c原子的坐标参数为
,0);d为(1,1,1)。则c原子的坐标参数为③若晶胞中Ni、Mg之间的最短距离为a pm,阿伏加 德罗常数的值为NA,则晶体的密度ρ=
 (用含a、NA的代数式表示)。
(用含a、NA的代数式表示)。
您最近一年使用:0次



