2011年,谢赫德曼因发现“准晶体”独享诺贝尔化学奖。2009年,科学家们在俄罗斯东部的河流中发现了十分耐磨的天然准晶体矿物Al63Cu24Fe13,有力地证明了准晶体理论。回答下列问题。
(1)可通过_____ 方法区分晶体、准晶体和非晶体。
(2)基态Fe原子的电子排布式是_____ 。铝和铁的第一电离能的大小次序是_____ 。
(3)五羰基合铁[Fe(CO)5]是一种浅黄色难溶于水的液体,其熔点-20℃,沸点103℃。依据以上信息可推断五羰基合铁属于______ (“准晶体”、“离子晶体”、“分子晶体”或“原子晶体”)。
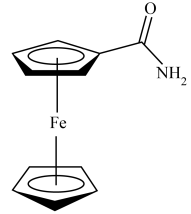
(4)二茂铁甲酰胺的结构如下图所示。其中N原子的杂化方式为______ 。
(5)工业用沉淀法制备磁性材料铁氧体,一般在制备的时候使用NH3和N2H4等弱碱。比较表格中的熔沸点数据,发现N2H4的熔沸点高于NH3的熔沸点,其原因是_____ 。
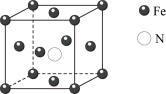
(6)氮和铁也能形成一种磁性材料,其晶胞如下图所示,该磁性材料的化学式为_____ 。晶胞参数为anm,则该晶胞密度的计算式为ρ=____ g/cm3(用NA表示阿伏加 德罗常数的值)。
(1)可通过
(2)基态Fe原子的电子排布式是
(3)五羰基合铁[Fe(CO)5]是一种浅黄色难溶于水的液体,其熔点-20℃,沸点103℃。依据以上信息可推断五羰基合铁属于
(4)二茂铁甲酰胺的结构如下图所示。其中N原子的杂化方式为

(5)工业用沉淀法制备磁性材料铁氧体,一般在制备的时候使用NH3和N2H4等弱碱。比较表格中的熔沸点数据,发现N2H4的熔沸点高于NH3的熔沸点,其原因是
NH3 | N2H4 | |
熔点/℃ | -78 | 2 |
沸点/℃ | -34 | 113 |
(6)氮和铁也能形成一种磁性材料,其晶胞如下图所示,该磁性材料的化学式为

更新时间:2020-09-18 17:54:14
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】T、X、Y、Z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如表所示:
请根据以上信息回答下列问题(答题时如需表示具体元素,填写相应的元素符号):
(1)T、X、Y三种元素的电负性由大到小的顺序是___________ 。
(2)与X单质分子互为等电子体的物质的化学式为(分子、离子各一种)___________ 、___________ 。
(3)X的简单氢化物分子间能形成氢键,Z的简单氢化物分子间不易形成氢键,原因是___________ 。
(4)元素Q的原子序数是Y与Z的原子序数之和。
①元素Q基态原子的价电子排布式为___________ 。
②元素Q与元素T、X能形成平面形的 ,该离子所含的化学键类型为
,该离子所含的化学键类型为___________ 。
| 元素 | 结构或性质信息 |
| T | 基态原子的L层上s轨道电子数和p轨道电子数相等 |
| X | 基态原子最外层未成对电子数在该元素所在周期中最多 |
| Y | 基态原子的第一电离能在该元素所在周期中最小 |
| Z | 其单质在常温、常压下是气体,基态原子的M层上有1个未成对的p电子 |
(1)T、X、Y三种元素的电负性由大到小的顺序是
(2)与X单质分子互为等电子体的物质的化学式为(分子、离子各一种)
(3)X的简单氢化物分子间能形成氢键,Z的简单氢化物分子间不易形成氢键,原因是
(4)元素Q的原子序数是Y与Z的原子序数之和。
①元素Q基态原子的价电子排布式为
②元素Q与元素T、X能形成平面形的
 ,该离子所含的化学键类型为
,该离子所含的化学键类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铝的化合物及合金为重要物质。其三乙基铝[Al(CH2CH3)3]是一种无色液体,是乙烯、丙烯等烯烃聚合的重要催化剂,结构如图。

回答下列问题:
(1)基态C原子与Al原子中未成对的电子数之比为_______ 。H、C、Al电负性最大的是_______ 。根据对角线规则,Al的一些化学性质与元素_______ 相似。
(2)三乙基铝中Al的价层电子对数为_______ ,C杂化轨道类型为_______ 。
(3)三乙基铝溶于苯、二甲苯、汽油等烃类有机溶剂,原因是_______ 。三乙基铝遇水即发生爆炸,与NaOH溶液反应的化学方程式为:Al(CH2CH3)3+3H2O+NaOH=Na[Al(OH)4]+3CH3CH3↑。Na[Al(OH)4]中存在的化学键有_______ ,Al(OH) 的空间构型为
的空间构型为_______ 。
(4)铝合金MoAl12性能优良,其晶胞结构示意图如图所示。其中每个Mo原子周围围绕的Al原子形成正二十面体。每个晶胞中含有MoAl12的单元数有_______ 个,若晶胞参数为anm,MoAl12相对式量为M,则晶体密度为_______ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。


回答下列问题:
(1)基态C原子与Al原子中未成对的电子数之比为
(2)三乙基铝中Al的价层电子对数为
(3)三乙基铝溶于苯、二甲苯、汽油等烃类有机溶剂,原因是
 的空间构型为
的空间构型为(4)铝合金MoAl12性能优良,其晶胞结构示意图如图所示。其中每个Mo原子周围围绕的Al原子形成正二十面体。每个晶胞中含有MoAl12的单元数有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】尖晶石的主要成分是镁铝氧化物,常含有锰、铁、镍等元素,形成种类繁多的尖晶石型化合物,可研制成优质半导体光催化材料。回答下列问题:
(1)基态锰原子的价层电子排布图(轨道表示式)为___________ 。
(2)羰基锰[ ]的结构如图所示,配体为CO,则配体的电子式为
]的结构如图所示,配体为CO,则配体的电子式为___________ ,该结构中 键与
键与 键个数比为
键个数比为___________ 。

(3) 容易形成六配位的配合物,
容易形成六配位的配合物,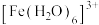 通常会水解生成棕色的
通常会水解生成棕色的 ,通过氢氧根形成双聚体
,通过氢氧根形成双聚体 ,请写出该双聚体的结构(水分子中O—H键省略,其他化学键用短横线“—”表示)
,请写出该双聚体的结构(水分子中O—H键省略,其他化学键用短横线“—”表示)___________ 。
(4)鉴定 的特征反应如下所示:
的特征反应如下所示:
Ni2++2 →
→ +2H+
+2H+
将丁二酮肟加入 溶液中,生成一种鲜红色的二丁二酮肟合镍(Ⅱ)螯合物,在该螯合物中,碳原子的杂化方式是
溶液中,生成一种鲜红色的二丁二酮肟合镍(Ⅱ)螯合物,在该螯合物中,碳原子的杂化方式是___________ ,组成该螯合物的第二周期元素第一电离能从大到小的顺序为___________ 。
(5)某镁铝尖晶石的晶胞由M区和N区组成,其结构如图所示,该化合物的化学式为___________ ,已知该晶胞参数为a pm,NA为阿伏加德罗常数的值,则该晶体的密度
___________ g/cm3 (列出计算表达式)。

(1)基态锰原子的价层电子排布图(轨道表示式)为
(2)羰基锰[
 ]的结构如图所示,配体为CO,则配体的电子式为
]的结构如图所示,配体为CO,则配体的电子式为 键与
键与 键个数比为
键个数比为
(3)
 容易形成六配位的配合物,
容易形成六配位的配合物,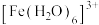 通常会水解生成棕色的
通常会水解生成棕色的 ,通过氢氧根形成双聚体
,通过氢氧根形成双聚体 ,请写出该双聚体的结构(水分子中O—H键省略,其他化学键用短横线“—”表示)
,请写出该双聚体的结构(水分子中O—H键省略,其他化学键用短横线“—”表示)(4)鉴定
 的特征反应如下所示:
的特征反应如下所示:Ni2++2
 →
→ +2H+
+2H+将丁二酮肟加入
 溶液中,生成一种鲜红色的二丁二酮肟合镍(Ⅱ)螯合物,在该螯合物中,碳原子的杂化方式是
溶液中,生成一种鲜红色的二丁二酮肟合镍(Ⅱ)螯合物,在该螯合物中,碳原子的杂化方式是(5)某镁铝尖晶石的晶胞由M区和N区组成,其结构如图所示,该化合物的化学式为


您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(1)盐酸中加入六次甲基四胺对钢铁有一定缓蚀作用,如图为其结构简式,其分子式为(CH2)6N4,其中碳原子采用________ 杂化,其缓蚀作用是因为分子中________ 原子的孤对电子能与铁原子形成配位键,覆盖在钢铁表面。
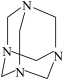
(2)CO与N2属于等电子体,1个CO分子中含有的π键数目是________ 个。C、N、O三种元素的第一电离能最大的是________ 。
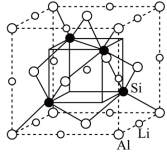
(3)如图是某化合物的晶胞示意图,硅原子与铝原子之间都以共价键连接。
①该化合物的化学式是________ 。
②Al元素基态原子的电子排布式是________ 。
③已知晶胞边长为5.93×10-8 cm,Si与Al之间的共价键键长是______ cm(只要求列算式,不必计算出数值,下同),晶体的密度是______ g·cm-3

(2)CO与N2属于等电子体,1个CO分子中含有的π键数目是
(3)如图是某化合物的晶胞示意图,硅原子与铝原子之间都以共价键连接。
①该化合物的化学式是
②Al元素基态原子的电子排布式是
③已知晶胞边长为5.93×10-8 cm,Si与Al之间的共价键键长是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】金属钴及其化合物在航天、航空、航海和催化剂等领域发挥着重要的作用。回答下列问题:
(1)基态钴原子的价电子排布式为_______ ,其最高能层电子云轮廓图为_______ 形。
(2)钴能够形成以钴中心原子的多种配位化合物。
①CO分子作为配体时,碳原子和氧原子均能够提供孤电子对。CO与钴形成配位化合物时,提供孤电子对的为_______ 原子(填元素名称)。
②高氯酸六氨合钴(II)的结构为 。其外界离子的空间构型为
。其外界离子的空间构型为_______ ;下列对[Co(NH3)6]2+的中心原子采取的杂化类型判断合理的是_______ (填标号)。
A.sp3 B.sp3d C.sp3d2 D.dsp2
(3)工业上用CH4处理N2O的化学方程式为:CH4+N2O N2+CH3OH。
N2+CH3OH。
①写出一种与N2O互为等电子体的阴离子的化学式:_______ 。
②CH3OH与水任意比互溶,其原因除与水分子的极性相似外,还有_______ 。
(4)金属钴有两种堆积方式,其晶体结构如图所示。

①甲图所示的堆积方式中,每个晶胞中实际占有的钴原子数为_______ ;乙图所示的堆积方式中,晶胞的原子空间利用率为_______ 。
②已知:NA为阿伏加德罗常数的值,钴原子半径为r pm。甲图中正六棱柱的高为hpm,则该晶胞的密度为_______ g·cm-3(用含r、h、NA的式子表示,列出计算式即可)。
(1)基态钴原子的价电子排布式为
(2)钴能够形成以钴中心原子的多种配位化合物。
①CO分子作为配体时,碳原子和氧原子均能够提供孤电子对。CO与钴形成配位化合物时,提供孤电子对的为
②高氯酸六氨合钴(II)的结构为
 。其外界离子的空间构型为
。其外界离子的空间构型为A.sp3 B.sp3d C.sp3d2 D.dsp2
(3)工业上用CH4处理N2O的化学方程式为:CH4+N2O
 N2+CH3OH。
N2+CH3OH。①写出一种与N2O互为等电子体的阴离子的化学式:
②CH3OH与水任意比互溶,其原因除与水分子的极性相似外,还有
(4)金属钴有两种堆积方式,其晶体结构如图所示。

①甲图所示的堆积方式中,每个晶胞中实际占有的钴原子数为
②已知:NA为阿伏加德罗常数的值,钴原子半径为r pm。甲图中正六棱柱的高为hpm,则该晶胞的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】A、B、C代表3种元素。请回答下列问题:
(1)A的基态原子的最外层有3个未成对电子,次外层有2个电子。意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的A4分子,该分子的空间构型与P4类似,其中A原子的轨道杂化方式为___________ ,A-A键的键角为___________ 。元素As与A同族。预测As的氢化物分子的立体结构为___________ ,其沸点比AH3的___________ (填“高”或“低”),其判断理由是___________ 。
(2)B元素的正三价离子的3d能级为半充满,则B元素在元素周期表中的位置为___________ 。
(3)C的基态原子的M能层全充满,N能层没有成对电子,只有一个未成对电子,则C的基态原子的电子排布式为___________ 。
(1)A的基态原子的最外层有3个未成对电子,次外层有2个电子。意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的A4分子,该分子的空间构型与P4类似,其中A原子的轨道杂化方式为
(2)B元素的正三价离子的3d能级为半充满,则B元素在元素周期表中的位置为
(3)C的基态原子的M能层全充满,N能层没有成对电子,只有一个未成对电子,则C的基态原子的电子排布式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】据《自然·通讯》(Nature Communications)报道,我国科学家发现了硒化铜纳米催化剂在二氧化碳电化学还原法生产甲醇过程中催化效率高。我国国产洲际战略导弹其制作材料中包含了等多种元素。Cu、Se、Fe、Cr、Ni、C等元素化合物在生产、生活中应用广泛。回答下列问题:
(1)基态铜原子的价电子排布式为_______ 。
(2)电还原法制备甲醇的原理为2CO2+4H2O 2CH3OH+3O2。
2CH3OH+3O2。
①写出该反应中由极性键构成的非极性分子的结构式_______ ;
②写出一个与CO2互为等电子体的离子_______ 。
(3)实验室常用KSCN溶液检验Fe3+。其中N、O、S的第一电离能由大到小的顺序为_______ (用元素符号表示);
(4)苯分子中6个C原子,每个C原子有一个2p轨道参与形成大π键,可记为( 右下角“6”表示6个原子,右上角“6”表示6个共享电子)。已知某化合物的结构简式为
右下角“6”表示6个原子,右上角“6”表示6个共享电子)。已知某化合物的结构简式为 ,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,该大π键可表示为
,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,该大π键可表示为_______ ,Se的杂化方式为_______ 。
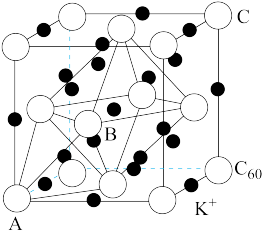
(5)碳的一种同素异形体的晶体可采取非最密堆积,然后在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的_______ 空隙和_______ 空隙(填几何空间构型);若C60分子的坐标参数分别为A(0,0, 0),B( ,0,
,0,  ),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为
),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为_______ 。
(6)Ni可以形成多种氧化物,其中一种NiaO晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0. 88,且晶体中的Ni分别为Ni2+、Ni3+,则晶体中Ni2+与Ni3+的最简整数比为_______ ,晶胞参数为428 pm,则晶体密度为_______ g/cm3(NA表示阿伏加德罗常数的值,列出表达式)。
(1)基态铜原子的价电子排布式为
(2)电还原法制备甲醇的原理为2CO2+4H2O
 2CH3OH+3O2。
2CH3OH+3O2。①写出该反应中由极性键构成的非极性分子的结构式
②写出一个与CO2互为等电子体的离子
(3)实验室常用KSCN溶液检验Fe3+。其中N、O、S的第一电离能由大到小的顺序为
(4)苯分子中6个C原子,每个C原子有一个2p轨道参与形成大π键,可记为(
 右下角“6”表示6个原子,右上角“6”表示6个共享电子)。已知某化合物的结构简式为
右下角“6”表示6个原子,右上角“6”表示6个共享电子)。已知某化合物的结构简式为 ,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,该大π键可表示为
,不能使溴的四氯化碳溶液褪色,由此推知,该分子中存在大π键,该大π键可表示为(5)碳的一种同素异形体的晶体可采取非最密堆积,然后在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的
 ,0,
,0,  ),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为
),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为
(6)Ni可以形成多种氧化物,其中一种NiaO晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0. 88,且晶体中的Ni分别为Ni2+、Ni3+,则晶体中Ni2+与Ni3+的最简整数比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】75号元素铼,熔点仅次于钨,是制造航空发动机的必需元素。地壳中铼的含量极低,多伴生于钼、铜、锌、铅等矿物中。回答下列问题:
(1)锰与铼处于同一族,锰原子价层电子的轨道表示式(价层电子排布图)为_______ ,它处于周期表的_____ 区。
(2)与铼伴生的铜能形成多种配合物。如:醋酸二氨合铜(Ⅰ)[Cu(NH3)2]Ac可用于吸收合成氨中对催化剂有害的CO气体:[Cu(NH3)2Ac+CO+NH3 [Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
[Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
①与铜离子形成配合物的分子或离子应具备的结构特征是___________________________ 。
②配位体NH3中N原子的杂化类型为_____ ,1mol 配离子[Cu(NH3)2]+中含有σ键的数目为______ 。
③写出与CO 互为等电子体的一种离子的化学式__________________ 。
(3)金属铼的熔点高于锰,试从原子结构的角度加以解释_________________________________________________ 。
(4)三氧化铼为立方晶胞,晶胞参数为3.74A(1A=10-10m),铼原子占据顶点,氧原子占据所有棱心。则铼原子的配位数为_______ ,三氧化铼的密度为____ g/cm3。(用NA表示阿伏伽德罗常数的值,写计算式即可)
(1)锰与铼处于同一族,锰原子价层电子的轨道表示式(价层电子排布图)为
(2)与铼伴生的铜能形成多种配合物。如:醋酸二氨合铜(Ⅰ)[Cu(NH3)2]Ac可用于吸收合成氨中对催化剂有害的CO气体:[Cu(NH3)2Ac+CO+NH3
 [Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
[Cu(NH3)3]Ac·CO。(Ac表示醋酸根)①与铜离子形成配合物的分子或离子应具备的结构特征是
②配位体NH3中N原子的杂化类型为
③写出与CO 互为等电子体的一种离子的化学式
(3)金属铼的熔点高于锰,试从原子结构的角度加以解释
(4)三氧化铼为立方晶胞,晶胞参数为3.74A(1A=10-10m),铼原子占据顶点,氧原子占据所有棱心。则铼原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】我国科学家合成介孔Fe—N—C催化剂大幅度提高锌-空气(O2)燃料电池的寿命;研制成的铜催化剂,实现了 CO2高选择电还原制乙烯。请回答下列问题:
(1)锌位于元素周期表___________ 区。基态原子第一电离能:I1(Cu)___________ (填”>””<”或“ = ”) I1(Zn)。
(2)N、C、O、Zn的电负性由大到小的顺序为___________ 。
(3)在N、C、O的最简单氢化物中,沸点最高的是___________ (填化学式,下同),属于非极性分子的有___________ 。
(4)[Zn(NH3)2(H2O)2]2+只有1种结构,则[Zn(NH3)4]2+的立体构型为___________ (填“正方形”或“正四面体形”)。
(5)我国科学家开发的高效稳定荧光OLED器件,结构如图甲。该结构中碳原子杂化类型有___________ 。

甲
(6)同温同压下,相同气体体积的CO2、C2H4中 键数目之比为
键数目之比为___________ 。
(7)碳化铁晶胞如图乙所示,将碳原子看成插入铁晶胞中。已知晶胞参数为 cm,
cm,  表示阿伏加德罗常数的值。两个铁原子间最近距离为
表示阿伏加德罗常数的值。两个铁原子间最近距离为___________ cm,碳化铁晶体的密度为___________ g·cm-3(列出表达式即可)。

乙
(1)锌位于元素周期表
(2)N、C、O、Zn的电负性由大到小的顺序为
(3)在N、C、O的最简单氢化物中,沸点最高的是
(4)[Zn(NH3)2(H2O)2]2+只有1种结构,则[Zn(NH3)4]2+的立体构型为
(5)我国科学家开发的高效稳定荧光OLED器件,结构如图甲。该结构中碳原子杂化类型有

甲
(6)同温同压下,相同气体体积的CO2、C2H4中
 键数目之比为
键数目之比为(7)碳化铁晶胞如图乙所示,将碳原子看成插入铁晶胞中。已知晶胞参数为
 cm,
cm,  表示阿伏加德罗常数的值。两个铁原子间最近距离为
表示阿伏加德罗常数的值。两个铁原子间最近距离为
乙
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】湿法冶炼是以赤铜矿(Cu2O)精矿为主要原料,通过浸出、置换、电解等流程制备高纯度铜的工艺。
已知:Cu2O晶胞为立方体形,边长为4.26×10−8 cm。
(1)根据图示,每个Cu2O晶胞中含O原子的数目为_______ 个。

(2)计算Cu2O晶体的密度ρ=_______ g/cm3.(结果保留两位小数)
(3)测定晶体结构最常用的仪器为
(4)赤铜矿在稀硫酸中浸出,得到硫酸铜溶液,该反应的离子方程式为_______ 。
已知:Cu2O晶胞为立方体形,边长为4.26×10−8 cm。
(1)根据图示,每个Cu2O晶胞中含O原子的数目为

(2)计算Cu2O晶体的密度ρ=
(3)测定晶体结构最常用的仪器为
| A.质谱仪 | B.核磁共振仪 | C.红外光谱仪 | D.X射线衍射仪 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】铁酸锌(ZnFe2O4)是一种重要的磁性材料与催化剂,实验室可以通过前驱固相法制备铁酸锌,具体步骤如下:
Ⅰ.7.840 g (NH4)2Fe(SO4)2·6H2O(M=392 g·mol-1)与2.870 g ZnSO4·7H2O(M=287 g·mol-1)溶于100 mL水中,加热至75℃。
Ⅱ.加热足量0.002 mol/L(NH4)2C2O4溶液到75℃与Ⅰ中溶液混合。
Ⅲ.将混合液在90-100℃加热搅拌5 min,生成固体前驱物[ZnFe2(C2O4)3·6H2O]。
Ⅳ.待混合溶液冷却进行过滤,用冷的蒸馏水洗涤。
Ⅴ.将过滤得到的固体前驱物干燥2 h,然后在700℃灼烧2 h,得到产品1.928 g。
(1)下列仪器在步骤Ⅰ中需使用的是___________ (填标号),无需使用的是___________ (填名称)。
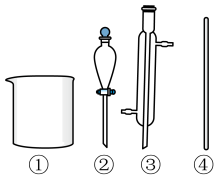
(2)步骤Ⅱ中采用的加热方式是___________ 加热。
(3)步骤Ⅲ中发生的离子反应方程式为___________ 。
(4)步骤Ⅳ中检验固体前驱物洗涤干净的操作和现象为___________ 。
(5)步骤Ⅴ中固体前驱物在高温条件下发生分解,生成三种无色气体,该反应的化学方程式为___________ 。
(6)本实验的产率为___________ 。
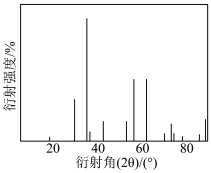
(7)将所得产品用X射线衍射法检测后,得到X射线衍射图谱如图所示,则ZnFe2O4属于___________ (填“晶体”或“非晶体”)。
Ⅰ.7.840 g (NH4)2Fe(SO4)2·6H2O(M=392 g·mol-1)与2.870 g ZnSO4·7H2O(M=287 g·mol-1)溶于100 mL水中,加热至75℃。
Ⅱ.加热足量0.002 mol/L(NH4)2C2O4溶液到75℃与Ⅰ中溶液混合。
Ⅲ.将混合液在90-100℃加热搅拌5 min,生成固体前驱物[ZnFe2(C2O4)3·6H2O]。
Ⅳ.待混合溶液冷却进行过滤,用冷的蒸馏水洗涤。
Ⅴ.将过滤得到的固体前驱物干燥2 h,然后在700℃灼烧2 h,得到产品1.928 g。
(1)下列仪器在步骤Ⅰ中需使用的是

(2)步骤Ⅱ中采用的加热方式是
(3)步骤Ⅲ中发生的离子反应方程式为
(4)步骤Ⅳ中检验固体前驱物洗涤干净的操作和现象为
(5)步骤Ⅴ中固体前驱物在高温条件下发生分解,生成三种无色气体,该反应的化学方程式为
(6)本实验的产率为
(7)将所得产品用X射线衍射法检测后,得到X射线衍射图谱如图所示,则ZnFe2O4属于

您最近一年使用:0次
【推荐3】卤素及其化合物广泛存在于自然界中。回答下列问题:
(1)光气(COCl2)是一种重要的有机中间体,在农药、医药、工程塑料、聚氨酯材料以及军事上都有许多用途。光气的分子立体构型为______________ ,其三种元素的电负性由小到大的顺序为______________ 。与COCl2互为等电子体的分子和离子(各写一种)__________ 。
(2)日常生活中,看到的许多可见光,如霓虹灯,试从原子结构角度解释这一现象?____________________________ 。
(3)区分晶态二氧化硅和非晶态二氧化硅最可靠的科学方法是_____________ 。
(4)一种铜的溴化物晶胞结构如图所示,若将图中的Cu去掉,再把所有的Br换成Cu,得到晶体铜的晶胞结构,则晶体铜的堆积方式为___________ ,某同学将基态铜原子价电子错误的写为3d94s2,违背了核外电子排布规律中的______ 。
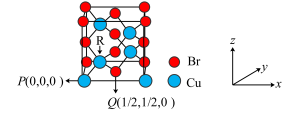
(5)下列关于上述铜的溴化物晶胞结构说法正确的是_________ (选填字母序号)。
A.该化合物的化学式为CuBr2
B.铜的配位数为8
C.与每个Br紧邻的Br有12个
D.由图中P点和Q点的原子坐标参数,确定R点的原子坐标参数为(1/4,1/4,1/4)
(6)若图中P点和R点的原子核间距为a cm,NA为阿伏伽德罗常数的值,则该晶胞密度为______ g/cm3。(列出计算式即可)
(1)光气(COCl2)是一种重要的有机中间体,在农药、医药、工程塑料、聚氨酯材料以及军事上都有许多用途。光气的分子立体构型为
(2)日常生活中,看到的许多可见光,如霓虹灯,试从原子结构角度解释这一现象?
(3)区分晶态二氧化硅和非晶态二氧化硅最可靠的科学方法是
(4)一种铜的溴化物晶胞结构如图所示,若将图中的Cu去掉,再把所有的Br换成Cu,得到晶体铜的晶胞结构,则晶体铜的堆积方式为

(5)下列关于上述铜的溴化物晶胞结构说法正确的是
A.该化合物的化学式为CuBr2
B.铜的配位数为8
C.与每个Br紧邻的Br有12个
D.由图中P点和Q点的原子坐标参数,确定R点的原子坐标参数为(1/4,1/4,1/4)
(6)若图中P点和R点的原子核间距为a cm,NA为阿伏伽德罗常数的值,则该晶胞密度为
您最近一年使用:0次



