25℃时,下列四种溶液:①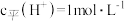 的
的 溶液,②
溶液,② 盐酸,③
盐酸,③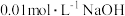 溶液,④
溶液,④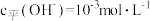 的氨水。则四种溶液中由水电离出的
的氨水。则四种溶液中由水电离出的 浓度之比为( )
浓度之比为( )
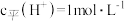 的
的 溶液,②
溶液,② 盐酸,③
盐酸,③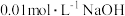 溶液,④
溶液,④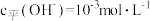 的氨水。则四种溶液中由水电离出的
的氨水。则四种溶液中由水电离出的 浓度之比为( )
浓度之比为( )| A.1∶10∶100∶1000 | B.1∶1∶12∶11 | C.14∶13∶12∶11 | D.14∶13∶2∶3 |
更新时间:2020-09-17 11:48:42
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】室温下,通过下列实验探究 溶液的性质:
溶液的性质:
下列说法正确的是
 溶液的性质:
溶液的性质:| 编号 | 实验操作 |
| 1 | 用 试纸测定 试纸测定 的 的 溶液,测得 溶液,测得 约为2 约为2 |
| 2 | 向 的 的 溶液中逐滴加入等体积 溶液中逐滴加入等体积 的 的 溶液,测得所得溶液的 溶液,测得所得溶液的 约为4 约为4 |
| 3 | 将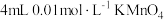 酸性溶液与 酸性溶液与 溶液混合,溶液褪色 溶液混合,溶液褪色 |
A. 的 的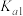 约为 约为 |
B.实验2溶液 由2到4的过程中水的电离程度不断减小 由2到4的过程中水的电离程度不断减小 |
C.实验2所得溶液中继续加 溶液至溶液呈中性: 溶液至溶液呈中性: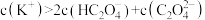 |
D.实验3中酸性 溶液褪色证明 溶液褪色证明 具有漂白性 具有漂白性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列溶液中有关物质的量浓度关系不正确的是
| A.pH相等的NaOH、CH3COONa和NaHCO3三种溶液,则有c(NaOH)<c(CH3COONa)<c(NaHCO3) |
| B.已知25℃时Ksp(AgCl)=1.8×10-10,则在0.3 mol·L-1 NaCl溶液中,Ag+的物质的量浓度最大可达到6.0×10-10 mol·L-1 |
| C.25℃时,0.1 mol·L-1 Na2CO3溶液中水电离出来的c(OH)大于0.1 mol·L-1 NaOH溶液中水电离出来的c(OH-) |
| D.浓度均为0.1 mol/L的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=c(CH2COOH)+2c(H+) |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,向苹果酸[结构简式为HOOCCH(OH)CH2COOH,用H2A表示]溶液中滴加NaOH溶液,所得混合溶液中 或
或 与溶液pH的变化关系如图所示。下 列叙述错误的是
与溶液pH的变化关系如图所示。下 列叙述错误的是

 或
或 与溶液pH的变化关系如图所示。下 列叙述错误的是
与溶液pH的变化关系如图所示。下 列叙述错误的是
A.曲线N表示 随pH的变化关系 随pH的变化关系 |
| B.水的电离程度: c>b>a |
| C.d点溶液中: c(Na+)>c(A2- )> c(H2A)>c(HA- ) |
| D.苹果酸的两级电离常数的乘积Ka1·Ka2的数量级为10 -8 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,下列有关两种溶液的说法不正确的是
| 序号 | ① | ② |
| pH | 12 | 12 |
| 溶液 | 氨水 | 氢氧化钠溶液 |
| A.①②两溶液中c(OH-)相等 |
| B.①②两溶液中水的电离程度相同 |
| C.等体积的①②两溶液分别与0.01mol·L-1的盐酸完全中和,消耗盐酸的体积:①>② |
| D.①②两溶液分别加水稀释10倍,稀释后溶液的pH:①<② |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知NaHSO4在水中的电离方程式为NaHSO4=Na++H++ 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是
 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是| A.该温度下加入等体积pH=10的NaOH溶液可使反应后的溶液恰好呈中性 |
| B.水电离出来的c(H+)=1×10-12mol/L |
C.c(H+)=c(OH-)+c( ) ) |
| D.该温度高于25℃ |
您最近半年使用:0次

 溶液,由水电离的
溶液,由水电离的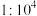
 固体,
固体, 增大,
增大, 不变
不变 和
和 溶液,前者
溶液,前者
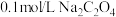 与
与 溶液等体积混合(
溶液等体积混合(


