酸性高锰酸钾溶液与草酸能发生反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。下列各组实验中混合溶液最先褪色的是( )
| 实验 | 反应温度/℃ | KMnO4溶液 | H2C2O4溶液 | H2O | ||
| V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | ||
| A | 25 | 5 | 0.01 | 10 | 0.1 | 5 |
| B | 25 | 5 | 0.01 | 5 | 0.3 | 10 |
| C | 35 | 5 | 0.01 | 10 | 0.1 | 5 |
| D | 35 | 5 | 0.01 | 5 | 0.3 | 10 |
| A.A | B.B | C.C | D.D |
更新时间:2020-09-27 12:05:34
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】为探究 和
和 对
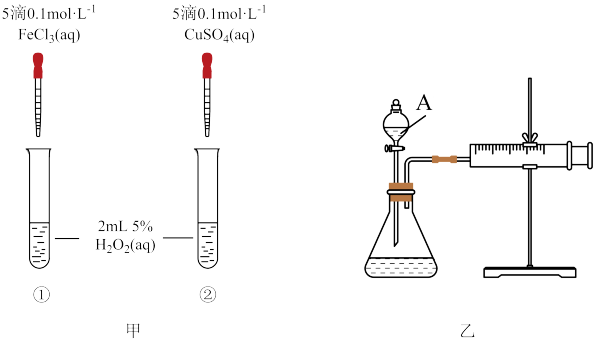
对 分解反应的催化效果,某同学分别设计了图1、图2所示的实验。下列叙述不正确的是( )
分解反应的催化效果,某同学分别设计了图1、图2所示的实验。下列叙述不正确的是( )
 和
和 对
对 分解反应的催化效果,某同学分别设计了图1、图2所示的实验。下列叙述不正确的是( )
分解反应的催化效果,某同学分别设计了图1、图2所示的实验。下列叙述不正确的是( )
| A.图2中的A为分液漏斗 |
| B.图2实验可通过测定相同状况下产生相同体积的气体所用的时间来比较反应速率 |
| C.图1实验可通过观察产生气泡的快慢来比较反应进行的快慢 |
D.若图1实验中反应速率为①>②,则 对 对 分解的催化效果一定比 分解的催化效果一定比 好 好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
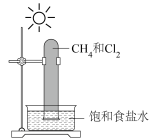
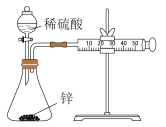
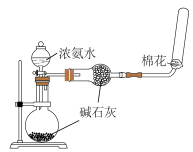
【推荐2】下列实验装置(部分夹持装置已略去)可以达到实验目的的是
| 实验装置 | 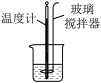 | 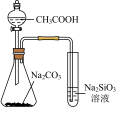 | 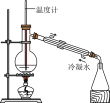 | 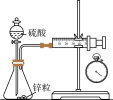 |
| 实验目的 | 中和反应反应热的测定 | 比较酸性:醋酸>碳酸>硅酸 | 石油分馏 | 测定锌与稀硫酸的反应速率 |
| 选项 | A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】探究Na2S2O3 + H2SO4 = Na2SO4 + SO2↑ + S↓ + H2O化学反应速率的影响因素,设计了以下实验,下列说法正确的是
| 锥形瓶 | 0.1 mol/LNa2S2O3溶液的体积/mL | 0.1 mol/LH2SO4溶液的体积/mL | 蒸馏水的体积/mL | 反应温度 | 浑浊出现时间/s | 备注 |
| 1 | 10 | 10 | 0 | 20 ℃ | 10 | |
| 2 | 10 | 5 | V1 | 20℃ | 16 | |
| 3 | 10 | 10 | V2 | 50℃ | 5 | 10秒后浑浊不再增多 |
| 4 | 10 | 4 | V3 | 50 ℃ | 8 |
| A.V1=5, V2=0, V3=6 |
| B.10秒内,3号瓶中Na2S2O3的平均反应速率为0.01mol/(L·s) |
| C.该反应也可通过比较相同时间内生成SO2体积的多少来判断化学反应的快慢 |
| D.由2号瓶和3号瓶的实验结果可推知温度越高反应速率越快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用下列实验装置进行的相关实验能达到相应目的的是
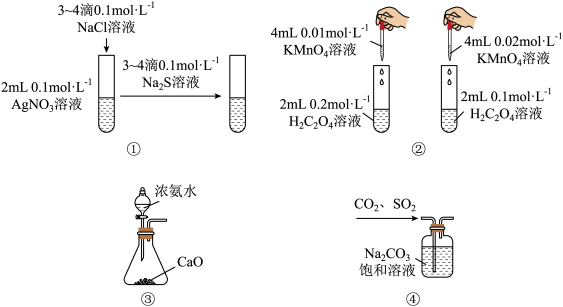

| A.利用装置①验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀 |
| B.利用装置②探究浓度对化学反应速率的影响 |
| C.利用装置③制取氨气 |
| D.利用装置④除去CO2气体中的SO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 判断C元素和S元素的非金属性强弱 | 常温下,测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH | 若Na2CO3溶液pH比Na2SO3溶液的大,则非金属性:S>C |
| B | 以Al2O3为原料制备AlCl3•6H2O | 在Al2O3中加入适量浓盐酸,加热促进溶解,蒸发浓缩至溶液表面出现一层晶膜,静置,冷却结晶 | 若冷却时晶体析出量很少,则说明氯化铝溶解度随温度降低变化不明显,应采取蒸发结晶的方法 |
| C | 验证反应物浓度增大可加快反应速率 | 在3支试管中分别加入0.05mol·L-1、0.2mol·L-1、2mol·L-1草酸溶液各2mL,再同时加入1mL0.01mol·L-1高锰酸钾溶液,观察现象 | 若0.2mol·L-1草酸溶液中紫色最先褪去,则反应物浓度增大时,该反应速率不一定增大,还有其它影响因素,需要进一步探究 |
| D | 检验1—溴丙烷消去产物中的丙烯 | 取5mL1—溴丙烷和10mL饱和氢氧化钾乙醇溶液,均匀加热,将产生的气体通入2mL稀酸性高锰酸钾溶液中 | 若高锰酸钾溶液褪色,则有丙烯生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】向体积为 10 L 的恒容密闭容器中通入 1.5 mol CH4(g)和 1.5 mol H2O(g),发生反应CH4(g)+H2O(g)  CO(g)+3H2(g)。在不同温度(Ta、Tb)下测得容器中 n(CO) 随时间的变化曲线如图。下列说法正确的是
CO(g)+3H2(g)。在不同温度(Ta、Tb)下测得容器中 n(CO) 随时间的变化曲线如图。下列说法正确的是

 CO(g)+3H2(g)。在不同温度(Ta、Tb)下测得容器中 n(CO) 随时间的变化曲线如图。下列说法正确的是
CO(g)+3H2(g)。在不同温度(Ta、Tb)下测得容器中 n(CO) 随时间的变化曲线如图。下列说法正确的是 
| A.Ta<Tb |
| B.该反应是放热反应 |
| C.Tb时,CH4的平衡转化率是 60% |
D.Ta时,平衡后体系的压强为起始压强的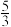 倍 倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知放热反应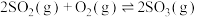 ,若起始时按
,若起始时按 和
和 物质的量比2:1投料,反应达到平衡时
物质的量比2:1投料,反应达到平衡时 的转化率(%)随温度和压强变化如下表:
的转化率(%)随温度和压强变化如下表:
下列说法不正确 的是
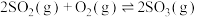 ,若起始时按
,若起始时按 和
和 物质的量比2:1投料,反应达到平衡时
物质的量比2:1投料,反应达到平衡时 的转化率(%)随温度和压强变化如下表:
的转化率(%)随温度和压强变化如下表:| 温度/℃ | 平衡时 的转化率/% 的转化率/% | ||||
| 0.1MPa | 0.5MPa | 1MPa | 2.5MPa | 5MPa | |
| 400 | 99.2 | 99.6 | 99.7 | 99.8 | 99.9 |
| 450 | 97.5 | 98.9 | 99.2 | 99.5 | 99.6 |
| 500 | 93.5 | 96.9 | 97.8 | 98.6 | 99.0 |
A.反应过程中, 和 和 的转化率始终相等 的转化率始终相等 |
B.降低温度或增大压强,可使 的转化率达到100% 的转化率达到100% |
| C.其他条件不变,升高温度,正反应速率和逆反应速率均增大 |
| D.实际生产中,该反应常采用400~500℃、常压并使用催化剂 |
您最近一年使用:0次

 的反应,加入
的反应,加入 ,反应速率加快
,反应速率加快 正反应放热
正反应放热 ,升高温度,反应速率减慢
,升高温度,反应速率减慢 在密闭容器中进行,恒压,充入
在密闭容器中进行,恒压,充入 不改变反应速率
不改变反应速率 稀盐酸与锌反应时,加入少量硫酸铜固体,生成氢气的速率加快
稀盐酸与锌反应时,加入少量硫酸铜固体,生成氢气的速率加快

