醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
 H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是| A.升高温度,平衡正向移动,醋酸的电离常数Ka值增大 |
| B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(H+)增大 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.25℃时,欲使醋酸溶液的pH和电离程度都减小,可加入少量冰醋酸 |
更新时间:2020-10-05 23:22:40
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】常温下 下列物质的水溶液,加热到
下列物质的水溶液,加热到 ,溶液
,溶液 几乎不变的是
几乎不变的是
 下列物质的水溶液,加热到
下列物质的水溶液,加热到 ,溶液
,溶液 几乎不变的是
几乎不变的是| A.氢氧化钾 | B.硫酸铵 | C.盐酸 | D.硫酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】室温下,向10 mL pH=11的氨水中加水稀释后,下列说法正确的是
| A.溶液中导电粒子的数目减少 |
B.溶液中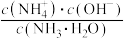 不变 不变 |
C.一水合氨的电离程度增大, 亦增大 亦增大 |
| D.将10 mL pH=11的氨水与10 mL pH=3的盐酸混合,所得溶液的pH=7 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| ① | 相同条件下,分别测量0.1mol/L和0.01mol/L醋酸溶液的导电性,前者的导电性强 | 醋酸浓度越大,电离程度越大 |
| ② | 常温下,分别测定浓度均为0.1mol/LNaF和NaClO溶液的pH,后者的pH大 | 酸性: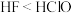 |
| ③ | CuS的悬浊液中加入足量饱和 溶液可生成浅红色沉淀(MnS为浅红色) 溶液可生成浅红色沉淀(MnS为浅红色) | 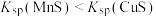 |
| ④ |  和KOH的混合溶液中加入铝粉并加热,管口放湿润的红色石蕊试纸,试纸变为蓝色 和KOH的混合溶液中加入铝粉并加热,管口放湿润的红色石蕊试纸,试纸变为蓝色 |  被还原为 被还原为 |
| A.① | B.② | C.③ | D.④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在CH3COOH H++CH3COO-的电离平衡中,要使电离平衡右移且氢离子浓度增大,应采取的措施是
H++CH3COO-的电离平衡中,要使电离平衡右移且氢离子浓度增大,应采取的措施是
 H++CH3COO-的电离平衡中,要使电离平衡右移且氢离子浓度增大,应采取的措施是
H++CH3COO-的电离平衡中,要使电离平衡右移且氢离子浓度增大,应采取的措施是| A.加入NaOH | B.加入盐酸 |
| C.加水 | D.升高温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列操作中,能使电离平衡H2O⇌H++OH-,向逆反应反向移动的是( )
| A.向水中加入2.0mol/L碳酸钠溶液 | B.向水中加入2.0mol/L 氢氧化钠溶液 |
| C.向水中加入2.0mol/L 氯化钠溶液 | D.将水加热到100℃,使pH=6 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】采取下列措施后,溶液颜色变深的是
| A.加热明矾溶液(滴有酚酞试液) |
| B.氨水(滴有酚酞试液)中加入少量NH4Cl固体 |
| C.加热CH3COONa溶液(滴有酚酞试液) |
| D.小苏打溶液(滴有酚酞试液)中加入少量NaCl固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】醋酸溶液中存在电离平衡:CH3COOH  H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
 H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是| A.升高温度,醋酸的电离常数 Ka增大 |
| B.0.10 mol·L-1的 CH3COOH 溶液加水稀释,溶液中导电粒子的数目增大 |
| C.CH3COOH 溶液中加少量的 CH3COONa 固体,平衡逆向移动 |
| D.25℃时,欲使醋酸溶液的 pH、电离常数 Ka和电离程度都减小,可加入少量冰醋酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】醋酸溶液中存在电离平衡: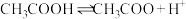 ,下列叙述
,下列叙述不正确 的是
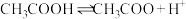 ,下列叙述
,下列叙述| A.升高温度,醋酸的电离常数Ka增大 |
B.0.01 醋酸加水稀释,溶液中导电粒子的数目增大 醋酸加水稀释,溶液中导电粒子的数目增大 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.25℃时,加入少量冰醋酸会使溶液中c(H+)和CH3COOH电离度都增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关pH变化的判断中,正确的是
| A.随着温度的升高,碳酸溶液的pH减小 |
| B.随着温度的升高,纯水的pH减小 |
| C.浓盐酸露置一段时间后,pH减小 |
| D.氢氧化钠溶液久置于空气中,pH增大 |
您最近一年使用:0次

 的弱酸
的弱酸 溶液加水稀释至
溶液加水稀释至 ,下列说法正确的是
,下列说法正确的是 减小
减小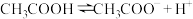 ,要使溶液中
,要使溶液中 的值增大,可以采取的措施有
的值增大,可以采取的措施有

