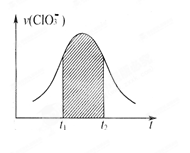
下列各组反应(表中物质均为反应物),反应刚开始,放出H2的速率最大的是
| 编号 | 金属(粉末)均0.1mol | 酸的浓度及体积 | 反应温度 |
| A | Mg | 3mol/L HCl溶液 10 mL | 60℃ |
| B | Mg | 3mol/L H2SO4溶液10 mL | 60℃ |
| C | Fe | 3mol/L HCl溶液 100 mL | 60℃ |
| D | Mg | 6mol/L HNO3溶液10 mL | 60℃ |
| A.A | B.B | C.C | D.D |
18-19高二下·黑龙江大庆·开学考试 查看更多[1]
(已下线)【百强校】黑龙江省大庆实验中学2018-2019学年高二下学期开学考试化学试题
更新时间:2019-03-05 20:28:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】2-甲基丙烯与HCl的加成反应有两种产物,这两种加成反应过程与其相应的能量变化曲线关系如下图所示。在恒容绝热密闭容器中通入一定量的2-甲基丙烯与HCl的混合物进行有关反应。下列说法正确的是
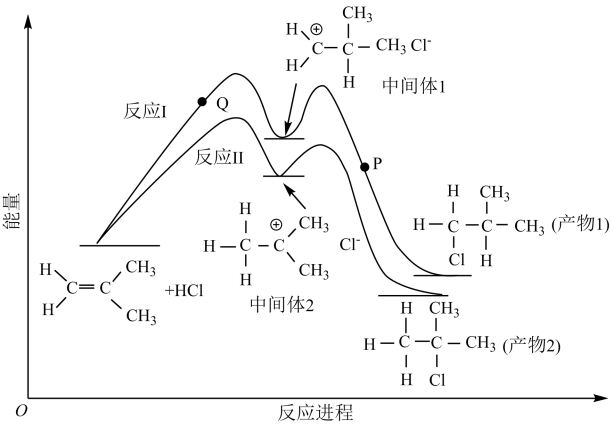

| A.产物稳定性的强弱:产物1>产物2 |
| B.反应的活化能大小:反应I>反应II |
| C.升高温度,反应I的逆反应速率变化值小于反应II的逆反应速率变化值 |
D.2-甲基丙烯与 的加成反应产物中, 的加成反应产物中,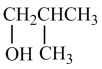 更稳定 更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
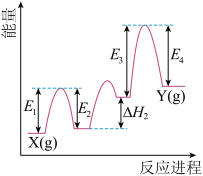
【推荐2】我国学者结合实验与计算机模拟结果,研究了均相NO-CO的反应历程,该反应经历了I、II、III三个过渡态。下图中显示的是反应路径中每一个阶段内各驻点的能量相对于此阶段内反应物能量的能量之差,则下列说法中正确的是


A. 比 比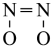 更容易与CO发生反应 更容易与CO发生反应 |
B.  |
| C.整个反应分为三个基元反应阶段,其中第二个反应阶段活化能最大 |
| D.其他条件不变,增大压强或使用催化剂均可以增大反应速率同时提高反应物的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化学振荡反应是指在化学反应中出现其反应物(或生成物)的浓度均匀一致地随时间而来回振荡的现象。碘钟反应是常见的振荡反应,在烧杯中加入H2O2溶液、酸性KIO3溶液、MnSO4和丙二酸的混合溶液、少许可溶性淀粉试剂后,碘钟反应正式开启,初始颜色为无色,溶液颜色变化如图。下列说法错误的是
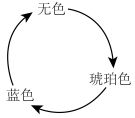

| A.无色变为琥珀色过程中,已知涉及反应2HIO+2Mn2++2H+=I2+2Mn3++2H2O,则氧化性:HIO>Mn3+ |
| B.反应由琥珀色变为蓝色过程中有氧化还原反应发生 |
| C.出现蓝色,是因为此时反应生成了大量I2 |
| D.该碘钟反应的振荡周期与温度无关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】容积固定为3L的某密闭容器中加入1mol A、2mol B,一定温度下发生如下发应:A(s)+2B(g) C(g)+D(g),经反应5 min后,测得C的浓度为0.3mol·L-1 。则下列说法正确的是
C(g)+D(g),经反应5 min后,测得C的浓度为0.3mol·L-1 。则下列说法正确的是
 C(g)+D(g),经反应5 min后,测得C的浓度为0.3mol·L-1 。则下列说法正确的是
C(g)+D(g),经反应5 min后,测得C的浓度为0.3mol·L-1 。则下列说法正确的是| A.5 min 内D的平均反应速率为0.02 mol·L-1·min-1 |
| B.第5min时C的反应速率为0.06 mol·L-1·min-1 |
| C.经5min后,向容器内再加入A,正反应速率变大 |
| D.平衡状态时,生成1molD时同时生成1molA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】用铁片与稀硫酸反应制氢气时,下列措施不能使反应速率加快的是
| A.加热 | B.滴加少量CuSO4溶液 |
| C.不用稀硫酸,改用98%的浓硫酸 | D.再加入相同的一个铁片 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列做法,不能使Zn+2HCl = ZnCl2 + H2↑的反应速率增大的是
| A.增大盐酸的浓度 | B.降低温度 |
| C.用锌粉代替锌粒 | D.滴加少量CuCl2溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】用稀硫酸与过量锌粒反应制取氢气,欲加快化学反应速率而不改变产生氢气的量,下列措施可行的是
| A.滴加少量水 | B.改用等质量的锌片 | C.滴加少量硫酸铜溶液 | D.滴加少量浓硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】Na2S2O3溶液与稀硫酸的反应为Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
| 实验 | 温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/(mL) | c/(mol·L-1) | V/(mL) | c/(mol·L-1) | V/(mL) | ||
| A | 20 | 5 | 0.1 | 5 | 0.2 | 10 |
| B | 20 | 5 | 0.2 | 10 | 0.1 | 5 |
| C | 40 | 5 | 0.1 | 5 | 0.2 | 10 |
| D | 40 | 5 | 0.2 | 10 | 0.1 | 5 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积)。下列分析正确的是
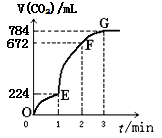

| A.OE段表示的平均速率最大 |
| B.EF段,用CaCO3表示该反应的平均反应速率为0.02mol/(L·min) |
| C.OE、EF、FG三段中,该反应用CO2表示的平均反应速率之比为2:6:7 |
| D.G点以后收集到的CO2不再增多,可能是盐酸浓度太小了 |
您最近一年使用:0次

 NO+CO2 的速率与浓度关系为v=kc(NO2),其中k为速率常数,恒温时k是定值。下列说法正确的是
NO+CO2 的速率与浓度关系为v=kc(NO2),其中k为速率常数,恒温时k是定值。下列说法正确的是