在室温下,发生下列几种反应:①16H++10Z-+2XO =2X2++5Z2+8H2O,②2A2++B2=2A3++2B-,③2B-+Z2=B2+2Z-。回答下列问题:
=2X2++5Z2+8H2O,②2A2++B2=2A3++2B-,③2B-+Z2=B2+2Z-。回答下列问题:
(1)要除去含有A2+、Z-和B-混合溶液中的A2+,而不氧化Z-和B-,应加入上面式子中的_____ 。
(2)在溶液中_____ (填“能”或“否”)发生反应8H++5A2++XO =X2++5A3++4H2O。
=X2++5A3++4H2O。
 =2X2++5Z2+8H2O,②2A2++B2=2A3++2B-,③2B-+Z2=B2+2Z-。回答下列问题:
=2X2++5Z2+8H2O,②2A2++B2=2A3++2B-,③2B-+Z2=B2+2Z-。回答下列问题:(1)要除去含有A2+、Z-和B-混合溶液中的A2+,而不氧化Z-和B-,应加入上面式子中的
(2)在溶液中
 =X2++5A3++4H2O。
=X2++5A3++4H2O。
更新时间:2020-10-21 09:22:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)按要求写出方程式:
① 在水溶液中的电离方程式:
在水溶液中的电离方程式:_______ 。
②少量二氧化碳通入足量澄清石灰水(离子方程式):_______ 。
(2)铜能与浓硝酸反应,化学方程式为:
①还原产物是_______ (用化学式表示,下同)。
②还原剂与氧化剂的数目比是_______ ,每生成一个 转移
转移_______ 个 。
。
③写出该反应的离子方程式_______ 。
(1)按要求写出方程式:
①
 在水溶液中的电离方程式:
在水溶液中的电离方程式:②少量二氧化碳通入足量澄清石灰水(离子方程式):
(2)铜能与浓硝酸反应,化学方程式为:

①还原产物是
②还原剂与氧化剂的数目比是
 转移
转移 。
。③写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】①SO3+H2O===H2SO4②Cl2+H2O===HCl+HClO ③2F2+2H2O===4HF+O2④2K+2H2O===2KOH+H2↑⑤CO2+2NaOH===Na2CO3+H2O
(1)上述反应中不属于氧化还原反应的有____ (填序号,下同);
(2)H2O只做氧化剂的是____ ,H2O只做还原剂的是____ ,
(3)属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是____ 。
(4)④的离子方程式_________________________ 。 ⑤的离子方程式_______________ 。
(1)上述反应中不属于氧化还原反应的有
(2)H2O只做氧化剂的是
(3)属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是
(4)④的离子方程式
您最近一年使用:0次
【推荐1】 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
(1)请用双线桥法表示上述反应电子转移情况_______ 。
(2)浓盐酸在反应中显示出来的性质是_______(填字母代号)。
(3)参与反应的氧化剂与还原剂的系数比_______ ,氧化产物为_______ ,还原产物为_______ 。
(4)根据氧化还原反应规律,推断 的氧化性
的氧化性_______  的氧化性(填“>”或“<”)。
的氧化性(填“>”或“<”)。
 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
(1)请用双线桥法表示上述反应电子转移情况
(2)浓盐酸在反应中显示出来的性质是_______(填字母代号)。
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
(4)根据氧化还原反应规律,推断
 的氧化性
的氧化性 的氧化性(填“>”或“<”)。
的氧化性(填“>”或“<”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列氧化还原反应相关问题:
I.
(1)配平下面的氧化还原方程式_________ 。
______ _____
_____ _____
_____ _____
_____ _____
_____ 。
。
(2)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出
表现出_______ (填“氧化性”或“还原性”)
(3)已知 可以与
可以与 反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:
反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:_______ 。
II. 和浓盐酸在一定温度下反应会生成黄绿色的易爆物
和浓盐酸在一定温度下反应会生成黄绿色的易爆物 。其变化可表述为
。其变化可表述为 。
。
(4)请分析该反应中的氧化产物为_______ 。
(5)浓盐酸在反应中显示出来的性质是_______ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(6)在碱性条件下加入 ,可实现将
,可实现将 转化为
转化为 ,
, 被还原为
被还原为 ,其离子方程式为
,其离子方程式为_______ 。还原性:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
I.
(1)配平下面的氧化还原方程式
______
 _____
_____ _____
_____ _____
_____ _____
_____ 。
。(2)误食
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出
表现出(3)已知
 可以与
可以与 反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:
反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:II.
 和浓盐酸在一定温度下反应会生成黄绿色的易爆物
和浓盐酸在一定温度下反应会生成黄绿色的易爆物 。其变化可表述为
。其变化可表述为 。
。(4)请分析该反应中的氧化产物为
(5)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(6)在碱性条件下加入
 ,可实现将
,可实现将 转化为
转化为 ,
, 被还原为
被还原为 ,其离子方程式为
,其离子方程式为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I. 易溶于水,外观和食盐相似,有咸味,人误食会中毒。
易溶于水,外观和食盐相似,有咸味,人误食会中毒。
(1) 中氮元素的化合价为
中氮元素的化合价为___________ 价。
(2)已知 能发生反应:
能发生反应: 。
。
①用单线桥法表示该反应中电子转移情况___________ 。
②淀粉週碘单质会变蓝色,则鉴别 固体和
固体和 固体,选用的物质为
固体,选用的物质为___________ (填标号)。
a.水 b.淀粉一碘化钾溶液 c.白醋 d.白酒
II.
(3)工业废水中含有的重铬酸根离子(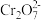 )有毒,必须处理达标后才能排放。工业上常用绿矾
)有毒,必须处理达标后才能排放。工业上常用绿矾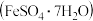 作处理剂,能将
作处理剂,能将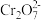 中
中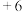 价
价 转化为
转化为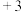 价
价 。则反应中氧化剂(氧化性离子)与还原剂(还原性离子)的个数之比为
。则反应中氧化剂(氧化性离子)与还原剂(还原性离子)的个数之比为___________ 。
(4)已知:①铁钉在氯气中被锈蚀成棕褐色含 的物质,而在稀硫酸中生成浅绿色溶液
的物质,而在稀硫酸中生成浅绿色溶液 含
含 ;②
;② 。则
。则 、
、 、
、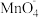 氧化性由强到弱排序为
氧化性由强到弱排序为___________ 。
 易溶于水,外观和食盐相似,有咸味,人误食会中毒。
易溶于水,外观和食盐相似,有咸味,人误食会中毒。(1)
 中氮元素的化合价为
中氮元素的化合价为(2)已知
 能发生反应:
能发生反应: 。
。①用单线桥法表示该反应中电子转移情况
②淀粉週碘单质会变蓝色,则鉴别
 固体和
固体和 固体,选用的物质为
固体,选用的物质为a.水 b.淀粉一碘化钾溶液 c.白醋 d.白酒
II.
(3)工业废水中含有的重铬酸根离子(
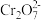 )有毒,必须处理达标后才能排放。工业上常用绿矾
)有毒,必须处理达标后才能排放。工业上常用绿矾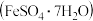 作处理剂,能将
作处理剂,能将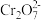 中
中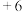 价
价 转化为
转化为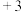 价
价 。则反应中氧化剂(氧化性离子)与还原剂(还原性离子)的个数之比为
。则反应中氧化剂(氧化性离子)与还原剂(还原性离子)的个数之比为(4)已知:①铁钉在氯气中被锈蚀成棕褐色含
 的物质,而在稀硫酸中生成浅绿色溶液
的物质,而在稀硫酸中生成浅绿色溶液 含
含 ;②
;② 。则
。则 、
、 、
、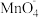 氧化性由强到弱排序为
氧化性由强到弱排序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】维生素 C(又名抗坏血酸,分子式为 C6H8O6)具有较强的还原性,放置在空气中易被氧化,其质量分数可通过在弱酸性溶液中用已知物质的量浓度的 I2 溶液进行测定。该反应 的化学方程式如下:C6H8O6+ I2 = C6H6O6 +2HI。现欲测定某样品中维生素 C 的质量分 数,具体的步骤及测得的数据如下:取10mL6mol/LCH3COOH(提供酸性环境),加入100 mL 蒸馏水,将溶液加热煮沸后放置冷却。精确称取 0.2000g 样品,溶解于上述冷却的 溶液中,立即用物质的量浓度为 0.05000 mol/L 的 I2 溶液进行反应,刚好完全反应时共消耗21.00 mL I2 溶液。
(1)CH3COOH 稀溶液要先经煮沸、冷却后才能使用,煮沸的是为了赶走溶液在溶液中的_____ (填物质的化学式)
(2)样品中维生素 C 的质量分数为______ 。计算过程
(1)CH3COOH 稀溶液要先经煮沸、冷却后才能使用,煮沸的是为了赶走溶液在溶液中的
(2)样品中维生素 C 的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】反应体系中的物质有: 、
、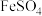 、
、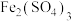 、
、 、
、 、
、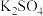 、
、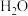 。
。
(1)请将 之外的反应物与生成物分别填入以下空格内(不用配平)。
之外的反应物与生成物分别填入以下空格内(不用配平)。_____

(2)反应中,被还原的元素是(标出价态)________ 。
(3)将氧化剂与还原剂及配平后的系数填入下列空格中(如果系数为1也要填写),并用单线条法标出电子转移的方向和数目。_____

 、
、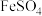 、
、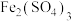 、
、 、
、 、
、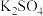 、
、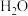 。
。(1)请将
 之外的反应物与生成物分别填入以下空格内(不用配平)。
之外的反应物与生成物分别填入以下空格内(不用配平)。
(2)反应中,被还原的元素是(标出价态)
(3)将氧化剂与还原剂及配平后的系数填入下列空格中(如果系数为1也要填写),并用单线条法标出电子转移的方向和数目。

您最近一年使用:0次
【推荐3】一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”.如2Fe3++Cu=2Fe2++Cu2+,可拆写为氧化反应式:Cu→Cu2++2e-,还原反应式:2Fe3++2e-→2Fe2+.在稀硫酸中,KMnO4和H2O2能发生氧化还原反应5H2O2+2MnO +6H+===5O2↑+2Mn2++8H2O。
+6H+===5O2↑+2Mn2++8H2O。
(1)将此氧化还原反应拆成半反应式,氧化式:_________ ,还原式:_________ 。
(2)反应中氧化剂是________ ;被氧化元素是__________ ;若有0.5 mol H2O2参加此反应,电子转移个数为____________ 。
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为________________________ ;这时若有0.5 mol H2O2发生分解,电子转移个数为______ 。
 +6H+===5O2↑+2Mn2++8H2O。
+6H+===5O2↑+2Mn2++8H2O。(1)将此氧化还原反应拆成半反应式,氧化式:
(2)反应中氧化剂是
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为
您最近一年使用:0次
【推荐1】“神舟十号”登天、“嫦娥二号”奔月,谱写了我国航天事业的新篇章。请回答下列问题:
(1)火箭升空需要高能的燃料,经常使用N2O4和N2H4作为燃料,请配平该反应方程式:____ N2O4 + ____ N2H4 →_____ N2 + ____ H2O。该反应中氧化产物与还原产物的物质的量之比为__________ 。该反应应用于火箭推进器,除释放大量的热和快速产生大量气体外,还有一个明显的优点是_______________________________ 。
(2)某些火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4molN2H4(l)和0.8molH2O2(l)混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量)。该反应的热化学方程式为______________ 。
(3)在载人航天器的生态系统中,不仅要求分离除去CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO+O2。其中生成的CO可用作燃料。已知该装置某极的电极反应式为:4OH- - 4e- = O2↑ + 2H2O,则另一极的电极反应式为:_____________ 。
(1)火箭升空需要高能的燃料,经常使用N2O4和N2H4作为燃料,请配平该反应方程式:
(2)某些火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4molN2H4(l)和0.8molH2O2(l)混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101kPa下测得的热量)。该反应的热化学方程式为
(3)在载人航天器的生态系统中,不仅要求分离除去CO2,还要求提供充足的O2。某种电化学装置可实现如下转化:2CO2=2CO+O2。其中生成的CO可用作燃料。已知该装置某极的电极反应式为:4OH- - 4e- = O2↑ + 2H2O,则另一极的电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
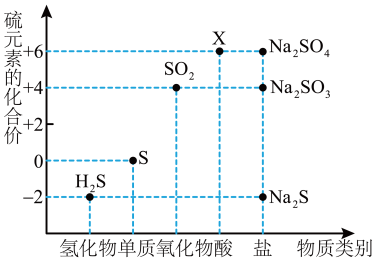
(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的___________ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有___________ (填化学式)。
(3)将 与
与 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(4)配平下列反应_________________ 。
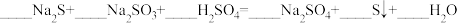
(5)一定条件下,在 密闭容器中发生反应:
密闭容器中发生反应: ,开始时加入
,开始时加入 、
、 、
、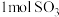 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 ,用
,用 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为___________ ,在 末
末 的浓度为
的浓度为___________ 。若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”)
①升高温度,化学反应速率___________ ;
②再充入 ,化学反应速率
,化学反应速率___________ ;
③将容器体积变为 ,化学反应速率
,化学反应速率___________ 。

(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将
 与
与 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为(4)配平下列反应
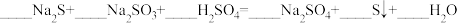
(5)一定条件下,在
 密闭容器中发生反应:
密闭容器中发生反应: ,开始时加入
,开始时加入 、
、 、
、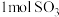 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 ,用
,用 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为 末
末 的浓度为
的浓度为①升高温度,化学反应速率
②再充入
 ,化学反应速率
,化学反应速率③将容器体积变为
 ,化学反应速率
,化学反应速率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】铁是应用最广泛的金属,铁的氯化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)在实验室中,FeCl2可用铁粉和___ (填名称)反应制备。
(2)Fe3O4可用多种方法制得,其中由一种单质和一种化合物通过化合反应制备的化学方程式为___ 。
(3)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是___ ,对应的化学方程式为___ 。
(4)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe3+:___ 。
(5)现有一含有FeCl2和FeCl3的混合物样品,实验测得n(Fe):n(C1)=1:2.1,则该样品中FeCl3的物质的量分数为___ 。
(6)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:___ 。
(1)在实验室中,FeCl2可用铁粉和
(2)Fe3O4可用多种方法制得,其中由一种单质和一种化合物通过化合反应制备的化学方程式为
(3)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是
(4)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe3+:
(5)现有一含有FeCl2和FeCl3的混合物样品,实验测得n(Fe):n(C1)=1:2.1,则该样品中FeCl3的物质的量分数为
(6)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:
您最近一年使用:0次



