烟气脱硫后的物质可以再生、再利用。
(1)一种干法脱硫技术以CuO为吸收剂,并用CH4再生CuO,原理如下:
2CuO(s)+2SO2(g)+O2(g)=2CuSO4(s)△H1=akJ·mol-1
2CuSO4(s)+CH4(g)=2Cu(s)+2SO2(g)+CO2(g)+2H2O(l)△H2=bkJ·mol-1
2Cu(s)+O2(g)=2CuO(s)△H3=ckJ·mol-1
反应CH4(g)+2O2(g)=CO2(g)+2H2O(l)的△H=___ (用含a、b、c的代数式表示)。
(2)钠碱法脱硫后的吸收液中主要成分为NaHSO3、Na2SO3。用三室阴阳膜组合膜电解吸收液可再生得到Na2SO3,原理如图1所示。
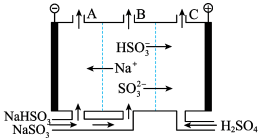
①写出电解时HSO 在阳极发生反应的电极反应式:
在阳极发生反应的电极反应式:___ 。
②如将阴离子交换膜换成阳离子交换膜,则出口B溶液中的溶质主要是___ (填化学式)。
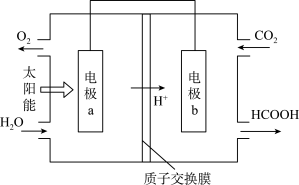
(3)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作___ 极,表面发生的电极反应为___ 。
(1)一种干法脱硫技术以CuO为吸收剂,并用CH4再生CuO,原理如下:
2CuO(s)+2SO2(g)+O2(g)=2CuSO4(s)△H1=akJ·mol-1
2CuSO4(s)+CH4(g)=2Cu(s)+2SO2(g)+CO2(g)+2H2O(l)△H2=bkJ·mol-1
2Cu(s)+O2(g)=2CuO(s)△H3=ckJ·mol-1
反应CH4(g)+2O2(g)=CO2(g)+2H2O(l)的△H=
(2)钠碱法脱硫后的吸收液中主要成分为NaHSO3、Na2SO3。用三室阴阳膜组合膜电解吸收液可再生得到Na2SO3,原理如图1所示。

①写出电解时HSO
 在阳极发生反应的电极反应式:
在阳极发生反应的电极反应式:②如将阴离子交换膜换成阳离子交换膜,则出口B溶液中的溶质主要是
(3)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。电极b作

更新时间:2020-11-02 18:40:04
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】氮氧化物和硫氧化物污染已经成为世界性的环境问题,但只要合理利用也是重要的资源。
(1)亚硝酰氯(NOCl)是有机合成中的重要试剂。它可由Cl2和NO在通常条件下反应制得,反应方程式为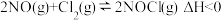 。在一个2 L的恒容密闭容器中充入2 molNO(g)和1 molCl2(g),在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间(单位:min)的关系如表所示:温度/℃
。在一个2 L的恒容密闭容器中充入2 molNO(g)和1 molCl2(g),在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间(单位:min)的关系如表所示:温度/℃
①T1_______ T2(填“>"、“<”或“=”)。
②温度为T2℃时,在相同容器中,充入4 mol NO(g)和2 mol Cl2(g),则NO的平衡转化率_______ 50%(填“>”、“<”或“=”)。
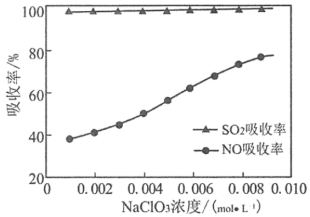
(2)用石灰乳与NaClO3的混合物吸收SO2和NO可得到CaSO4和Ca(NO3)2,NaClO3浓度变化对SO2和NO吸收率影响如图所示,NaClO3浓度变化对SO2吸收率几乎无影响,而对NO吸收率影响很大的原因是_______ 。
(3)①用CaSO3水悬浮液吸收经O3预处理过的含NO、NO2的烟气时,清液(pH约为8)中 将NO2转化成
将NO2转化成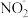 。清液中的离子反应方程式为
。清液中的离子反应方程式为_______ 。
②CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中
_______ [用 、
、 和
和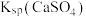 表示]。
表示]。
③CaSO3水悬浮液中加入Na2SO4浓溶液能提高NO2的吸收速率,其主要原因是_______ 。
(1)亚硝酰氯(NOCl)是有机合成中的重要试剂。它可由Cl2和NO在通常条件下反应制得,反应方程式为
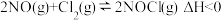 。在一个2 L的恒容密闭容器中充入2 molNO(g)和1 molCl2(g),在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间(单位:min)的关系如表所示:温度/℃
。在一个2 L的恒容密闭容器中充入2 molNO(g)和1 molCl2(g),在温度分别为T1、T2时测得NO的物质的量(单位:mol)与时间(单位:min)的关系如表所示:温度/℃| 0 | 5 | 8 | 13 | |
| T1 | 2 | 1.5 | 1.3 | 1.0 |
| T2 | 2 | 1.15 | 1.0 | 1.0 |
①T1
②温度为T2℃时,在相同容器中,充入4 mol NO(g)和2 mol Cl2(g),则NO的平衡转化率
(2)用石灰乳与NaClO3的混合物吸收SO2和NO可得到CaSO4和Ca(NO3)2,NaClO3浓度变化对SO2和NO吸收率影响如图所示,NaClO3浓度变化对SO2吸收率几乎无影响,而对NO吸收率影响很大的原因是

(3)①用CaSO3水悬浮液吸收经O3预处理过的含NO、NO2的烟气时,清液(pH约为8)中
 将NO2转化成
将NO2转化成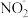 。清液中的离子反应方程式为
。清液中的离子反应方程式为②CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中

 、
、 和
和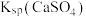 表示]。
表示]。③CaSO3水悬浮液中加入Na2SO4浓溶液能提高NO2的吸收速率,其主要原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】I.合成氨的原料气由天然气与水蒸气和空气高温反应而得。涉及的主要反应如下:
(a)CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
(b)2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=? kJ/mol
(c)CO(g)+H2O(g)=H2(g)+CO2(g) ΔH3=-41.2 kJ/mol
下表给出了一系列常见化学键的键能(单位:kJ/mol):
(1)写出1 mol甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:_______ (利用键能数据估算该反应焓变)。
(2)根据(1)的计算结果和已知数据,计算可得:ΔH2=_______ kJ/mol。
(3)在一定条件下,在容积恒定为V L的密闭容器中充入a mol CO与2a mol H2在催化剂作用下合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH4=x kJ/mol。CO转化率与温度、压强的关系如图所示:
CH3OH(g) ΔH4=x kJ/mol。CO转化率与温度、压强的关系如图所示:
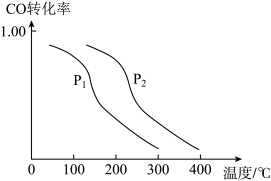
①由图可知:x_______ 0(选填“>”“<”或“=”),P1_______ P2(选填“>”“<”或“=”)。
②下列措施中能够同时满足增大正反应速率和提高CO转化率的是:_______ (选填序号)。
a.使用高效催化剂 b.降低反应温度
c.增大体系压强 d.不断将甲醇从体系混合物中分离出来
II.工业上利用合适的催化剂可以直接将CO2转化为乙酸,不同温度下,催化剂的催化效率与乙酸的生成速率的关系如图所示
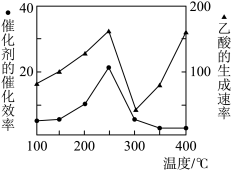
(4)温度在250℃到300℃时,乙酸的生成速率降低的原因可是_______
(5)温度超过300度时,催化剂的催化效率大大降低,但是乙酸的生成速率反而继续上升,出现这种现象的原因可能是_______
(a)CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH1=+206.1 kJ/mol
(b)2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=? kJ/mol
(c)CO(g)+H2O(g)=H2(g)+CO2(g) ΔH3=-41.2 kJ/mol
下表给出了一系列常见化学键的键能(单位:kJ/mol):
| 化学键 | C-H | O=O | C=O | O-H |
| 键能 | 412 | 497 | 799 | 463 |
(1)写出1 mol甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:
(2)根据(1)的计算结果和已知数据,计算可得:ΔH2=
(3)在一定条件下,在容积恒定为V L的密闭容器中充入a mol CO与2a mol H2在催化剂作用下合成甲醇:CO(g)+2H2(g)
 CH3OH(g) ΔH4=x kJ/mol。CO转化率与温度、压强的关系如图所示:
CH3OH(g) ΔH4=x kJ/mol。CO转化率与温度、压强的关系如图所示:
①由图可知:x
②下列措施中能够同时满足增大正反应速率和提高CO转化率的是:
a.使用高效催化剂 b.降低反应温度
c.增大体系压强 d.不断将甲醇从体系混合物中分离出来
II.工业上利用合适的催化剂可以直接将CO2转化为乙酸,不同温度下,催化剂的催化效率与乙酸的生成速率的关系如图所示

(4)温度在250℃到300℃时,乙酸的生成速率降低的原因可是
(5)温度超过300度时,催化剂的催化效率大大降低,但是乙酸的生成速率反而继续上升,出现这种现象的原因可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】甲醇(CH3OH)在化工生产中应用广泛。其中利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
I.CO(g) + H2O(g) CO2(g) + H2(g) ΔH1 = -41.0 kJ·mol-1
CO2(g) + H2(g) ΔH1 = -41.0 kJ·mol-1
II.CO(g) + 2H2(g) CH3OH(g) ΔH2 = -90. 0 kJ·mol-1
CH3OH(g) ΔH2 = -90. 0 kJ·mol-1
(1)写出CO2和 H2生成CH3OH和H2O蒸汽的热化学方程式___________
(2)在一恒温1L恒容容器中充入1mol CO2和3mol H2进行反应,测得CO2和CH3OH浓度随时间变化如图所示。
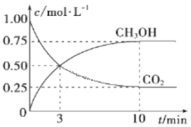
① 下列能说明该反应达平衡状态的是___________ (填序号)。
A.v正(CH3OH) = 3v逆(H2)B.混合气体的密度不变
C.c(CH3OH) = c(H2O)D.混合气体总物质的量不变
② 该化学反应平衡常数k=___________ (保留两位小数)。若温度体积保持不变,将反应物和生成物物质的量均增加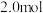 ,则此时反应
,则此时反应___________ (填“正向”“逆向”或“不”)移动。
③为提高 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是___________ (填序号)。
a.高温高压 b.低温低压 c.高温低压 d.低温高压
④ 250 ℃时,在恒容密闭容器中由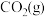 催化氢化合成
催化氢化合成 ,如图为不同投料比[
,如图为不同投料比[ ]时某反应物X的平衡转化率的变化曲线。反应物X是
]时某反应物X的平衡转化率的变化曲线。反应物X是___________ (填“ ”或“
”或“ ”)。
”)。

I.CO(g) + H2O(g)
 CO2(g) + H2(g) ΔH1 = -41.0 kJ·mol-1
CO2(g) + H2(g) ΔH1 = -41.0 kJ·mol-1II.CO(g) + 2H2(g)
 CH3OH(g) ΔH2 = -90. 0 kJ·mol-1
CH3OH(g) ΔH2 = -90. 0 kJ·mol-1(1)写出CO2和 H2生成CH3OH和H2O蒸汽的热化学方程式
(2)在一恒温1L恒容容器中充入1mol CO2和3mol H2进行反应,测得CO2和CH3OH浓度随时间变化如图所示。

① 下列能说明该反应达平衡状态的是
A.v正(CH3OH) = 3v逆(H2)B.混合气体的密度不变
C.c(CH3OH) = c(H2O)D.混合气体总物质的量不变
② 该化学反应平衡常数k=
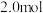 ,则此时反应
,则此时反应③为提高
 的产率,理论上应采用的条件是
的产率,理论上应采用的条件是a.高温高压 b.低温低压 c.高温低压 d.低温高压
④ 250 ℃时,在恒容密闭容器中由
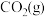 催化氢化合成
催化氢化合成 ,如图为不同投料比[
,如图为不同投料比[ ]时某反应物X的平衡转化率的变化曲线。反应物X是
]时某反应物X的平衡转化率的变化曲线。反应物X是 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】根据如图所示电化学实验装置图,回答有关问题。
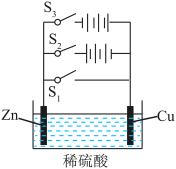
(1)若只闭合S1,该装置属于_______ ,能量转化形式为_______ ,锌极作_______ 极。
(2)若只闭合S2,该装置属于_______ ,能量转化形式为_______ ,锌极上的电极反应式为_______ 。
(3)若只闭合S3,该装置属于_______ ,铜极作_______ 极,锌极上的电极反应式为_______ ,总反应的化学方程式为_______ 。

(1)若只闭合S1,该装置属于
(2)若只闭合S2,该装置属于
(3)若只闭合S3,该装置属于
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】二氧化硫常用作消毒剂和漂白剂,也是一种重要的工业原料。
(1)将a mol SO2通入1 L 1 mol/L NaOH溶液中充分反应后,阴离子总数_______ 阳离子总数(填选项前的字母)。
A.a>1时大于 B.a=1时等于 C.大于 D.小于
(2)保险粉(Na2S2O4)广泛用于印染行业和食品储存行业。可以将SO2通入草酸钠(Na2C2O4)和NaOH的混合溶液中制取保险粉。制取保险粉的离子方程式为____________________ 。
(3)工业上常以SO2为原料制取Na2S2O3。步骤如下:
①将Na2S和Na2CO3按2︰1的物质的量之比配成混合溶液。
②将混合溶液注入敞口反应釜中,加热反应釜将温度控制在50℃左右。
③向反应釜中缓缓通入SO2至稍微过量使Na2S和Na2CO3完全反应。
④反应结束后加热浓缩溶液,冷却至30℃以下析出大量Na2S2O3晶体。
⑤滤出晶体,母液循环利用。
据此请回答:
(ⅰ)工业制取Na2S2O3的反应的化学方程式为___________________________________ 。
(ⅱ)工业生产的首要目的是盈利,为节约成本并减少对环境的污染,应尽可能的提高产率,制取步骤中体现了这一思想的有______________ (填步骤序号)。
(ⅲ)工业生产的Na2S2O3含有两种杂质,这两种杂质是Na2SO3和__________ 。以下条件中可以求出产品中Na2S2O3的物质的量分数的是_________ 。(填选项前的字母)
A.产品中钠原子和硫原子的物质的量之比
B.产品中钠原子和氧原子的物质的量之比
C.产品中硫原子和氧原子的物质的量之比
D.以上均能
(4)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:
2SO2+2n Cu+(n+1)O2+(2-2 n) H2O=2n CuSO4+(2-2n) H2SO4
每吸收标准状况下11.2 L SO2,被SO2还原的O2的质量为______ g。
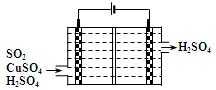
②利用下图所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的离子方程式___________________________ 。
(1)将a mol SO2通入1 L 1 mol/L NaOH溶液中充分反应后,阴离子总数
A.a>1时大于 B.a=1时等于 C.大于 D.小于
(2)保险粉(Na2S2O4)广泛用于印染行业和食品储存行业。可以将SO2通入草酸钠(Na2C2O4)和NaOH的混合溶液中制取保险粉。制取保险粉的离子方程式为
(3)工业上常以SO2为原料制取Na2S2O3。步骤如下:
①将Na2S和Na2CO3按2︰1的物质的量之比配成混合溶液。
②将混合溶液注入敞口反应釜中,加热反应釜将温度控制在50℃左右。
③向反应釜中缓缓通入SO2至稍微过量使Na2S和Na2CO3完全反应。
④反应结束后加热浓缩溶液,冷却至30℃以下析出大量Na2S2O3晶体。
⑤滤出晶体,母液循环利用。
据此请回答:
(ⅰ)工业制取Na2S2O3的反应的化学方程式为
(ⅱ)工业生产的首要目的是盈利,为节约成本并减少对环境的污染,应尽可能的提高产率,制取步骤中体现了这一思想的有
(ⅲ)工业生产的Na2S2O3含有两种杂质,这两种杂质是Na2SO3和
A.产品中钠原子和硫原子的物质的量之比
B.产品中钠原子和氧原子的物质的量之比
C.产品中硫原子和氧原子的物质的量之比
D.以上均能
(4)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:
2SO2+2n Cu+(n+1)O2+(2-2 n) H2O=2n CuSO4+(2-2n) H2SO4
每吸收标准状况下11.2 L SO2,被SO2还原的O2的质量为
②利用下图所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的离子方程式

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】下图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:

(1)通入甲烷的铂电极上发生的电极反应式为_______ 。
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为_______ L(标准状况下);若此时乙池溶液的体积为400mL,则乙池中溶液的H+的浓度为_______ 。
(3)若要用此装置在铁片上镀银,则:
①M电极的材料是_______ ,(“铁片”“银片”“石墨”中选填)电极反应式为_______ ;N电极的材料是_______ ,(“铁片”“银片”“石墨”中选填)电解质溶液是_______ 。
②若M、N极质量相同, 电镀进行一段时间后,当两极质量相差2.16g时,外电路共通过电子的物质的量是_______ mol。

(1)通入甲烷的铂电极上发生的电极反应式为
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为
(3)若要用此装置在铁片上镀银,则:
①M电极的材料是
②若M、N极质量相同, 电镀进行一段时间后,当两极质量相差2.16g时,外电路共通过电子的物质的量是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是一个电化学过程的示意图,请按要求填空:

(1)通入CH3CH2OH的电极名称是______________ ,B电极的名称是_____________ 。
(2)通入CH3CH2OH一极的电极反应式为_____________________________________ 。
(3)乙池中总反应的化学方程式为___________________________________________ 。
(4)当乙池中A(Fe)极的质量增加12.8g时,甲池中消耗O2_______ mL(标况下)
(5)火箭发射时可用肼(N2H4)为燃料,以二氧化氮做氧化剂,它们相互反应生成氮气和水蒸气。
①写出在碱性条件下负极反应式为:___________________________________________ 。
②已知:N2(g)+2O2(g)=2NO2(g),ΔH=+67.7 kJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g),ΔH=-534 kJ·mol-1,则N2H4和NO2反应的热化学方程式__________________________________________ 。

(1)通入CH3CH2OH的电极名称是
(2)通入CH3CH2OH一极的电极反应式为
(3)乙池中总反应的化学方程式为
(4)当乙池中A(Fe)极的质量增加12.8g时,甲池中消耗O2
(5)火箭发射时可用肼(N2H4)为燃料,以二氧化氮做氧化剂,它们相互反应生成氮气和水蒸气。
①写出在碱性条件下负极反应式为:
②已知:N2(g)+2O2(g)=2NO2(g),ΔH=+67.7 kJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g),ΔH=-534 kJ·mol-1,则N2H4和NO2反应的热化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】I、某研究性学习小组为探究Fe3+与Ag反应,进行如下实验:按下图连接装置并加入药品(盐桥中的物质不参与反应)。

(1)K闭合时,指针向左偏转,石墨作________ (填“正极”或“负极”);石墨电极上的电极反应方程式为___________ 。
(2)一段时间后指针归零,向左侧U形管中滴加几滴FeCl2浓溶液,发现指针向右偏转,写出此时银电极的反应式:_________________ 。
(3)结合上述实验分析,写出Fe3+和Ag反应的离子方程式______________ 。
II、某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。
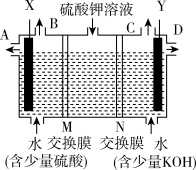
(1)X极与电源的_____ (填正或负)极相连,氢气从____ (选填A、 B、C或D)口导出。
(2)离子交换膜只允许一类离子通过,则M为________ (填阴离子或阳离子)交换膜。
(3)若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为______________ 。

(1)K闭合时,指针向左偏转,石墨作
(2)一段时间后指针归零,向左侧U形管中滴加几滴FeCl2浓溶液,发现指针向右偏转,写出此时银电极的反应式:
(3)结合上述实验分析,写出Fe3+和Ag反应的离子方程式
II、某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。

(1)X极与电源的
(2)离子交换膜只允许一类离子通过,则M为
(3)若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】I.氢气是一种清洁能源,其来源可以是:
途径1.用太阳能分解水生成氢气 途径2.用聚焦太阳能反应器发生以下反应:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206 kJ·mol-1
已知:在25℃、101kPa时 2CO(g)+ O2(g) ===2CO2(g) ΔH=-566.0 kJ·mol-1
(1)在25℃、101kPa时,1克H2完全燃烧生成气态水时放热120.9kJ热量。补全该反应的热化学方程式:2H2(g)+O2(g)===2H2O(g)ΔH =_________
(2)已知拆开与形成1mol化学键需要相同的能量,途径2中,拆开1mol H-H键需能量是ckJ、1molH-O键是bkJ、1mol C-H键是akJ,则拆开1mol CO(g)化学键需要能量是_______ kJ (用含字母的式子表示)
(3)CH4燃烧生成CO2和气态H2O的热化学方程式为__________
II.用酸性氢氧燃料电池为电源进行电解的实验装置如图所示。
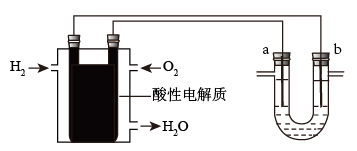
(4)燃料电池工作时,正极反应为:______________ 。
(5)U形管中装CuSO4溶液时,a、b两极均是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积比是:________ 。
(6)U形管中装饱和NaCl水溶液时,电解总反应的离子方程式是______________ 。
(7)用惰性电极电解M(NO3)x的水溶液,当阴极上增重m克时,在阳极上同时产生nL氧气(标准状况),从而可知M的相对原子质量是_________ 。(用含字母的式子表示)
途径1.用太阳能分解水生成氢气 途径2.用聚焦太阳能反应器发生以下反应:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206 kJ·mol-1
已知:在25℃、101kPa时 2CO(g)+ O2(g) ===2CO2(g) ΔH=-566.0 kJ·mol-1
(1)在25℃、101kPa时,1克H2完全燃烧生成气态水时放热120.9kJ热量。补全该反应的热化学方程式:2H2(g)+O2(g)===2H2O(g)ΔH =
(2)已知拆开与形成1mol化学键需要相同的能量,途径2中,拆开1mol H-H键需能量是ckJ、1molH-O键是bkJ、1mol C-H键是akJ,则拆开1mol CO(g)化学键需要能量是
(3)CH4燃烧生成CO2和气态H2O的热化学方程式为
II.用酸性氢氧燃料电池为电源进行电解的实验装置如图所示。

(4)燃料电池工作时,正极反应为:
(5)U形管中装CuSO4溶液时,a、b两极均是石墨,在相同条件下a极产生的气体与电池中消耗的H2体积比是:
(6)U形管中装饱和NaCl水溶液时,电解总反应的离子方程式是
(7)用惰性电极电解M(NO3)x的水溶液,当阴极上增重m克时,在阳极上同时产生nL氧气(标准状况),从而可知M的相对原子质量是
您最近一年使用:0次



