请回答下列问题。
(1)设NA表示阿伏加德罗常数:
①6.8g熔触的KHSO4中含有___ 个阳离子;
②0.1molNa2O2与水完全反应,转移______ 个电子;
③标准状况下,22.4L氩气含有原子数为____________ ;
④常温常压下,32gO2和O3的混合物含有_____ NA个氧原子。
(2)食盐不慎洒落在天然气的火焰上,观察的现象是________ ,该变化是________ 变化(填“物理”或“化学”)。
(3)清理卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与84消毒液(主要成分是次氯酸钠)而发生氯气中毒事件。请从氧化还原反应的角度分析原因:________________ 。
(4)下列反应可用于检查司机是否酒后开车:2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3(绿色)+3CH3COOH+2K2SO4+( )。方程式中空格内的系数和物质(化学式)为_____ 该反应中氧化产物是___________ ;还原产物是___________ ;反应中生成0.1molCr3+离子,转移的电子总数为________ 个。
(5)由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜
能够透过半透膜___________ 。
(1)设NA表示阿伏加德罗常数:
①6.8g熔触的KHSO4中含有
②0.1molNa2O2与水完全反应,转移
③标准状况下,22.4L氩气含有原子数为
④常温常压下,32gO2和O3的混合物含有
(2)食盐不慎洒落在天然气的火焰上,观察的现象是
(3)清理卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与84消毒液(主要成分是次氯酸钠)而发生氯气中毒事件。请从氧化还原反应的角度分析原因:
(4)下列反应可用于检查司机是否酒后开车:2K2Cr2O7+3C2H5OH+8H2SO4=2Cr2(SO4)3(绿色)+3CH3COOH+2K2SO4+( )。方程式中空格内的系数和物质(化学式)为
(5)由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。现有10mL明胶的水溶液与5mLK2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
 能够透过半透膜
能够透过半透膜
19-20高一·浙江·阶段练习 查看更多[1]
(已下线)【浙江新东方】11
更新时间:2020-11-09 16:18:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】(1)质量之比为16:7:6的三种气体SO2、CO、NO,分子个数之比为________ ;氧原子个数之比为________ ;相同条件下的体积之比为________ 。
(2)标准状况下,1.7 g NH3的体积为________ L,它与标准状况下________ L H2S含有相同数目的氢原子。
(3)某气体氧化物的化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为______ ,R的相对原子质量为________ 。
(2)标准状况下,1.7 g NH3的体积为
(3)某气体氧化物的化学式为RO2,在标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为
您最近一年使用:0次
【推荐2】亚硝酸钠(NaNO2)是一种工业盐,外观与食盐非常相似,但毒性较强,食品中添加亚硝酸钠必须严格控制用量。某化学兴趣小组设计实验探究NaNO2的性质。
(1)NaNO2_______ (填“是”或“不是”)电解质,根据NaNO2的化合价,推测NaNO2具有_______ (填“氧化性”、“还原性”或“氧化性和还原性”)。
(2)实验操作如表所示,请完善表格中的实验现象和结论(已知 遇淀粉变蓝)。
遇淀粉变蓝)。
④写出实验3中发生反应的化学方程式:_______ 。
⑤通过上述实验可知,NaNO2、KMnO4、I2的氧化性由强到弱的顺序为_______ 。
(3)根据我国食品添加剂使用标准,亚硝酸钠在肉制品中的最大使用量是0.15 g/kg。则300 g15%的NaNO2溶液最多可生产的肉制品的质量为_______ kg。
(1)NaNO2
(2)实验操作如表所示,请完善表格中的实验现象和结论(已知
 遇淀粉变蓝)。
遇淀粉变蓝)。| 实验 | 实验操作及现象或结果 | 结论 |
| 1 | 取5 mLNaNO2溶液于试管中,加入少量KI溶液,充分反应后,再滴加淀粉溶液,溶液变蓝 | NaNO2具有① |
| 2 | 取2 mLKMnO4溶液(先酸化好)于试管中,滴加足量的NaNO2溶液,可观察到的实验现象为② | NaNO2具有还原性 |
| 3 | NaNO2固体与70%硫酸反应生成了NO和NO2两种气体 | NaNO2具有③ |
④写出实验3中发生反应的化学方程式:
⑤通过上述实验可知,NaNO2、KMnO4、I2的氧化性由强到弱的顺序为
(3)根据我国食品添加剂使用标准,亚硝酸钠在肉制品中的最大使用量是0.15 g/kg。则300 g15%的NaNO2溶液最多可生产的肉制品的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)写出下列物质在水溶液中的电离方程式:
①NaHSO4______
②H2SO4______
③Ba(OH)2______
④NaHCO3______
(2)3.01×1023个H2O的物质的量为___________ mol,其中,所有原子的物质的量为___________ mol,所含电子的物质的量为___________ mol。
(3)___________ gH2O中的氧原子数目与标准状况下22.4LCO2中的氧原子数目相同。
(4)2gNaOH溶于水配制成___________ mL溶液时其物质的量浓度为2mol/L。
(1)写出下列物质在水溶液中的电离方程式:
①NaHSO4
②H2SO4
③Ba(OH)2
④NaHCO3
(2)3.01×1023个H2O的物质的量为
(3)
(4)2gNaOH溶于水配制成
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。如图是硫元素价类二维图。请回答下列问题:

(1)已知物质 是一种可溶性正盐,能被酸性
是一种可溶性正盐,能被酸性 溶液氧化为
溶液氧化为 被还原为
被还原为 ,请写出此反应的离子方程式
,请写出此反应的离子方程式___________ 。
(2)实验室提供以下试剂: 的浓溶液、
的浓溶液、 的稀溶液、酸性
的稀溶液、酸性 溶液、
溶液、 溶液、
溶液、 、品红溶液。若要实现
、品红溶液。若要实现 的转化,可选择的试剂是
的转化,可选择的试剂是___________ 、___________ (填化学式);设计实验,证明能实现该转化的操作和现象为___________ 。
(3)某兴趣小组用如图所示装置模拟空气中二氧化硫含量的测定。当注入标准状况下 空气时,酸性
空气时,酸性 溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为
溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为___________ (用含 代数式表示,体积分数即物质的量分数)。
代数式表示,体积分数即物质的量分数)。

(4)某化工厂用如图所示工艺流程除去燃煤产生的 。
。
①过程Ⅰ发生的反应为 ,其氧化剂与还原剂的质量之比为
,其氧化剂与还原剂的质量之比为___________ 。
②过程Ⅱ发生反应的化学方程式为___________ 。


(1)已知物质
 是一种可溶性正盐,能被酸性
是一种可溶性正盐,能被酸性 溶液氧化为
溶液氧化为 被还原为
被还原为 ,请写出此反应的离子方程式
,请写出此反应的离子方程式(2)实验室提供以下试剂:
 的浓溶液、
的浓溶液、 的稀溶液、酸性
的稀溶液、酸性 溶液、
溶液、 溶液、
溶液、 、品红溶液。若要实现
、品红溶液。若要实现 的转化,可选择的试剂是
的转化,可选择的试剂是(3)某兴趣小组用如图所示装置模拟空气中二氧化硫含量的测定。当注入标准状况下
 空气时,酸性
空气时,酸性 溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为
溶液恰好褪色,停止实验。该空气中二氧化硫的体积分数为 代数式表示,体积分数即物质的量分数)。
代数式表示,体积分数即物质的量分数)。
(4)某化工厂用如图所示工艺流程除去燃煤产生的
 。
。①过程Ⅰ发生的反应为
 ,其氧化剂与还原剂的质量之比为
,其氧化剂与还原剂的质量之比为②过程Ⅱ发生反应的化学方程式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂白液、漂白粉都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是84消毒液,可以说化学让生活更美好。下图为84消毒液说明书。请回答下列问题。
(1)84消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克Cl2的氧化能力(Cl均转化为Cl-)。若该84消毒液商品的有效氯按53.25g·L-1计算,该消毒液的NaClO的物质的量浓度是___________ 。
(2)常温下用烧碱溶液吸收Cl2制备84消毒液。写出该反应的离子方程式:___________ ,若将Cl2通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO3的混合液。当混合液中Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为___________ ,从氧化还原角度分析Cl2表现了___________ 性。
(3)家庭用84消毒液用法强调,为家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是(用离子方程式表示)___________ (已知酸性:H2CO3>HClO>HCO )。
)。
(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会___________ (填“增强”或“减弱”)。
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、84消毒液,主要目的是___________。
 | 药品名称 | 84消毒液 |
| 主要成分 | NaClO,有效氯含量50.00g·L-1~60.00g·L-1 | |
| 注意事项 | 不可与其他洗涤剂或消毒液混合使用 | |
| 用法用量 | 稀释后浸泡或洗刷白色衣物、浴缸等1∶200水溶液 餐饮具、瓜果等1∶100水溶液 |
(2)常温下用烧碱溶液吸收Cl2制备84消毒液。写出该反应的离子方程式:
 的个数比为15∶2时,混合液中ClO-和ClO
的个数比为15∶2时,混合液中ClO-和ClO 的个数比为
的个数比为(3)家庭用84消毒液用法强调,为家庭物品消毒时,要做适当的稀释,喷洒后也不要急于用清水擦拭,要浸泡,这样效果会更好,原因是(用离子方程式表示)
 )。
)。(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过强,杀毒作用会
(5)Cl2可直接用于杀菌消毒,但常常把氯气制成漂白粉、84消毒液,主要目的是___________。
| A.增强漂白能力和消毒作用 |
| B.使它转化为较稳定物质,便于保存和运输 |
| C.使它转化为较易溶于水的物质 |
| D.提高氯的质量分数,有利于漂白、消毒 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】“环境就是民生,青山就是美丽、蓝天也是幸福”。回答下列问题:
(1)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。
①某氮肥厂产生的氨氮废水中的氮元素多以 和
和 形式存在,为达到变废为宝回收利用的目的。可采取的方法是
形式存在,为达到变废为宝回收利用的目的。可采取的方法是___________ 。
②某团队设计处理流程如下:
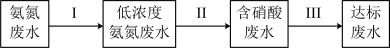
过程Ⅱ为硝化过程,在微生物的作用下实现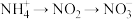 的转化,在碱性条件下被氧气氧化成NO
的转化,在碱性条件下被氧气氧化成NO 的总反应离子方程式为
的总反应离子方程式为___________ ;
过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇CH3OH被氧化为CO2)实现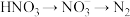 的转化,反应的化学方程式为
的转化,反应的化学方程式为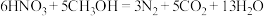 ,氧化产物是
,氧化产物是___________ ,当有1mol硝酸完全转化时,转移的电子数目为___________ 。
(2)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为___________ 。也可用NaClO2在酸性条件下氧化处理SO2,反应的离子方程式是___________ 。
②某兴趣小组对取得的酸雨样品进行pH测定,随着时间的推移,得到以下数据(pH越小,酸性越强)。
引起雨水pH变化的主要原因是___________ (用化学方程式表示)。
(3)碳捕集技术是减少二氧化碳排放的一种途径,基本思路是将工业排放的二氧化碳分离出来。若用氢氧化钠溶液吸收二氧化碳,反应后碳酸盐和碳酸氢盐的物质的量比为1∶1,反应的离子方程式为___________ 。
(1)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。
①某氮肥厂产生的氨氮废水中的氮元素多以
 和
和 形式存在,为达到变废为宝回收利用的目的。可采取的方法是
形式存在,为达到变废为宝回收利用的目的。可采取的方法是②某团队设计处理流程如下:

过程Ⅱ为硝化过程,在微生物的作用下实现
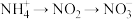 的转化,在碱性条件下被氧气氧化成NO
的转化,在碱性条件下被氧气氧化成NO 的总反应离子方程式为
的总反应离子方程式为过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇CH3OH被氧化为CO2)实现
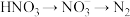 的转化,反应的化学方程式为
的转化,反应的化学方程式为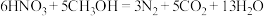 ,氧化产物是
,氧化产物是(2)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为
②某兴趣小组对取得的酸雨样品进行pH测定,随着时间的推移,得到以下数据(pH越小,酸性越强)。
| 时间/h | 开始 | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
(3)碳捕集技术是减少二氧化碳排放的一种途径,基本思路是将工业排放的二氧化碳分离出来。若用氢氧化钠溶液吸收二氧化碳,反应后碳酸盐和碳酸氢盐的物质的量比为1∶1,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】饮用水的质量关乎人类健康。回答下列问题:
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式________ 。
(2)常温下,将氯气通入稀NaOH溶液中得到漂白液(主要成分为NaClO),该反应的离子方程式为________ 。
(3)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为:在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为________ 。
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式
(2)常温下,将氯气通入稀NaOH溶液中得到漂白液(主要成分为NaClO),该反应的离子方程式为
(3)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为:在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氯是一种生产生活中常见的元素,下图是几种含氯产品。

(1)Cl2是有毒气体,为了防止多余Cl2污染空气,需要上图装置进行尾气处理,用化学方程式表示该原理___________ 。气体应该由___________ (填a或b)管通入。若要吸收标准状况下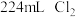 ,至少需要1mol/L的上述溶液
,至少需要1mol/L的上述溶液___________ mL。
(2)工业上制取漂白粉的化学方程式是___________ 。
(3)抗击新冠肺炎的战役中使用了大量的84消毒液。同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。将5mL市售84消毒液稀释100倍,测得稀释后溶液的 ,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
已知溶液中 、HClO和
、HClO和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
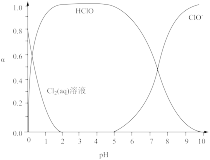
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色___________ (填“越快”或“越慢”)。
②结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是___________ 。

(1)Cl2是有毒气体,为了防止多余Cl2污染空气,需要上图装置进行尾气处理,用化学方程式表示该原理
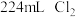 ,至少需要1mol/L的上述溶液
,至少需要1mol/L的上述溶液(2)工业上制取漂白粉的化学方程式是
(3)抗击新冠肺炎的战役中使用了大量的84消毒液。同学们探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验。将5mL市售84消毒液稀释100倍,测得稀释后溶液的
 ,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:
,将稀释后溶液各20mL分别加入a、b、c三个洁净的烧杯中:| 烧杯 | 溶液pH | 现象 |
| a | 10 | 10min后,红纸基本不褪色;4h后红纸褪色 |
| b | 7 | 10min后,红纸颜色变浅;4h后红纸褪色 |
| c | 4 | 10min后,红纸颜色比b烧杯中10min后的浅;4h后红纸褪色 |
 、HClO和
、HClO和 的物质的量分数(a)随溶液pH变化的关系如图所示:
的物质的量分数(a)随溶液pH变化的关系如图所示:
①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色
②结合图象进行分析,b、c两烧杯中实验现象出现差异的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组进行了如下实验。请回答:
(1)用一氧化碳还原氧化铁,反应的化学方程式为_______ 。反应完毕后,他们将得到的铁屑装入下图所示装置进行实验,A中的玻璃丝可以阻止固体离开A管,B中碱石灰的作用是_______ 。一段时间后,他们将A中的固体溶于水,并向所得溶液中滴入几滴KSCN溶液。
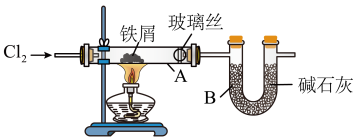
①若观察到溶液出现红色,证明溶液中含有_______ (填离子符号)。
②若未观察到溶液出现红色,可能的原因是_______ 。
(2)用足量的稀盐酸溶解一定量的Fe2O3,得到棕黄色溶液。甲同学向溶液中加入铜粉欲获得铁,他_______ (填“能”或“不能”)成功,原因是_______
(3)已知铝粉与氧化铁能发生反应2Al+Fe2O3 2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为
2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为_______ 。某同学认为用足量稀盐酸浸泡也能达到相同的结果,他的观点_______ (填“正确”或“不正确”)。
(1)用一氧化碳还原氧化铁,反应的化学方程式为

①若观察到溶液出现红色,证明溶液中含有
②若未观察到溶液出现红色,可能的原因是
(2)用足量的稀盐酸溶解一定量的Fe2O3,得到棕黄色溶液。甲同学向溶液中加入铜粉欲获得铁,他
(3)已知铝粉与氧化铁能发生反应2Al+Fe2O3
 2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为
2Fe+Al2O3小组成员将反应的产物用足量的NaOH溶液浸泡,除去其中的Al2O3,分离得到Fe,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有下列10种物质:①液态HCl,②NH4Cl,③蔗糖,④Cl2,⑤NaOH溶液,⑥熔融碳酸钠,⑦碳酸氢钠固体,⑧淀粉,⑨CaO,⑩H2O。回答下列问题:
(1)上述物质中,属于电解质的是_______ (填序号,下同),属于非电解质的是_______ ,在上述状态下能够导电的是_______ 。
(2)写出⑤和⑦反应的离子方程式:_______ 。
(3)在酒精灯火焰上灼烧,火焰呈黄色的,为_______ 。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的NaHCO3能治疗胃酸过多,请写出其反应的离子方程式:_______ 。
(5)除去Na2CO3粉末中混有的少量NaHCO3的方法是_______ ,化学方程式为_______ 。
(1)上述物质中,属于电解质的是
(2)写出⑤和⑦反应的离子方程式:
(3)在酒精灯火焰上灼烧,火焰呈黄色的,为
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的NaHCO3能治疗胃酸过多,请写出其反应的离子方程式:
(5)除去Na2CO3粉末中混有的少量NaHCO3的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】草木灰中含有可溶性钾盐(主要成分是 、
、 、
、 )。骉学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结晶。
)。骉学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结晶。
(1)由草木灰提取钾盐并检验钾元素的存在,下列实验操作中正确的是___________ 。

(2)为检验草木灰中的其它离子,取少量晶体溶于水,并把溶液分成三份,完成以下实验报告(在横线上填写相关的内容):
(3)步骤III所得的结论,你认为是否正确?为什么?___________
(4)写出步骤II有关现象的化学方程式___________ 、___________ 。
 、
、 、
、 )。骉学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结晶。
)。骉学生按下列操作提取草木灰中的钾盐:①取草木灰加水溶解;②过滤、取滤液;③蒸发滤液;④冷却结晶。(1)由草木灰提取钾盐并检验钾元素的存在,下列实验操作中正确的是

(2)为检验草木灰中的其它离子,取少量晶体溶于水,并把溶液分成三份,完成以下实验报告(在横线上填写相关的内容):
| 实验步骤 | 实验现象 | 实验结论 |
I. 取第一份溶液和适量稀盐酸加入试管中,把澄清的石灰水加入烧杯中 | 证明含有碳酸根离子 | |
| II.取第二份溶液,先后滴加 | 证明含有硫酸根离子 | |
III.取第三份溶液加入过量 溶液,过滤,除去 溶液,过滤,除去 和 和 ,再滴加 ,再滴加 溶液和稀硝酸 溶液和稀硝酸 | 有 | 证明含有氯离子 |
(4)写出步骤II有关现象的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】科学家在研究化学物质时,常对其进行分类,以便对同类物质的组成和性质进行深入研究,物质分类及转化思想贯穿整个化学学科学习的始终。
下列物质:①纯H2SO4②硝酸钾溶液③铜④二氧化碳⑤Ba(OH)2固体⑥KHSO4固体⑦蔗糖⑧熔融KCl⑨氨水
(1)能导电的是______ (填序号,下同),属于电解质的是______ ,属于非电解质的是______ 。
(2)写出⑤、⑥在水溶液中的电离方程式:⑤_____ ,⑥______ 。
(3)根据物质的组成②⑥⑧可以分为一类,其分类标准是:______ ,检验②中金属阳离子的实验方法是______ (填实验操作的名称),确定该离子存在的现象是______ 。
下列物质:①纯H2SO4②硝酸钾溶液③铜④二氧化碳⑤Ba(OH)2固体⑥KHSO4固体⑦蔗糖⑧熔融KCl⑨氨水
(1)能导电的是
(2)写出⑤、⑥在水溶液中的电离方程式:⑤
(3)根据物质的组成②⑥⑧可以分为一类,其分类标准是:
您最近一年使用:0次



