碱式硫酸铁[化学式Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,可由FeSO4和KClO3在水溶液中反应得到,有关反应的化学方程式如下:6FeSO4+KClO3+________=6Fe(OH)SO4+KCl
(1)请将上述化学方程式补充完整。________
(2)用双线桥法标出上述反应中转移电子的方向和数目。________
(3)上述反应中的还原剂是________ ,被还原的元素是________ ,每1molFeSO4参加反应,转移电子_________ mol。
(1)请将上述化学方程式补充完整。
(2)用双线桥法标出上述反应中转移电子的方向和数目。
(3)上述反应中的还原剂是
更新时间:2020-11-21 20:52:28
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知反应①SO3+H2O=H2SO4;②Cl2+H2O=HCl+HClO;③2F2+2H2O=4HF+O2;④2Na+2H2O=2NaOH+H2↑,根据上述反应,试回答:
(1)上述反应中不属于氧化还原反应的有_______ 。
(2)H2O被氧化的是_______ ,被还原的是_______ 。
(3)是氧化还原反应,但水既不被氧化,又不被还原的是_______ 。
(1)上述反应中不属于氧化还原反应的有
(2)H2O被氧化的是
(3)是氧化还原反应,但水既不被氧化,又不被还原的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
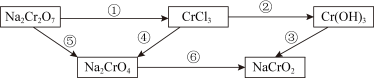
(1)铬是水体的主要污染物之一、处理铬的实验循环示意图如下。在有编号的步骤中,含铬化合物发生氧化反应的是___________ ,需要加入还原剂的是___________ (填编号)(提示:铬元素化合价有+6、+3价)。
(2)已知一定条件下可发生如下反应:6NO+4NH3=6H2O+5N2
①用双线桥法表示该反应中电子转移的方向和数目:___________ 。
②若有34g氨气发生反应,则反应所得还原产物与氧化产物的质量差为___________ g。
(3)从氧化剂和还原剂的角度,分析下列三个反应中H2O2的作用。
①H2O2+H2S=2H2O+S↓ H2O2的作用_______
②H2O2+Cl2=2HCl+O2 H2O2的作用_______
③2H2O2=2H2O+ O2↑ H2O2的作用_______
(1)铬是水体的主要污染物之一、处理铬的实验循环示意图如下。在有编号的步骤中,含铬化合物发生氧化反应的是

(2)已知一定条件下可发生如下反应:6NO+4NH3=6H2O+5N2
①用双线桥法表示该反应中电子转移的方向和数目:
②若有34g氨气发生反应,则反应所得还原产物与氧化产物的质量差为
(3)从氧化剂和还原剂的角度,分析下列三个反应中H2O2的作用。
①H2O2+H2S=2H2O+S↓ H2O2的作用
②H2O2+Cl2=2HCl+O2 H2O2的作用
③2H2O2=2H2O+ O2↑ H2O2的作用
您最近一年使用:0次
【推荐3】二氧化氯(ClO2)是国际公认的广谱、高效和安全的杀菌剂。
(1)制备C1O2的一种方法是在酸性条件下用草酸(碳的价态+3价)和氯酸钠反应,配平该反应的化学方程式,并标出电子转移的方向和数目:________ 。
_____H2C2O4+_____NaClO3+____H2SO4→_____ Na2SO4+___CO2↑+_____ClO2↑+___ H2O
(2)上述反应中被氧化的元素是____ ,氧化产物是_____ 。
(3)若反应中生成1.12L(标况) ClO2,转移电子数目为________ 。
(4)ClO2具有强氧化性,若ClO2和Cl2在消毒时自身均被还原为Cl-,计算ClO2的消毒能力是等质量Cl2的_____ 倍(保留2位小数)。
(5)若以NaClO2为原料制备ClO2,需要加入具有____ (填“氧化性”或“还原性”)的物质。
(1)制备C1O2的一种方法是在酸性条件下用草酸(碳的价态+3价)和氯酸钠反应,配平该反应的化学方程式,并标出电子转移的方向和数目:
_____H2C2O4+_____NaClO3+____H2SO4→_____ Na2SO4+___CO2↑+_____ClO2↑+___ H2O
(2)上述反应中被氧化的元素是
(3)若反应中生成1.12L(标况) ClO2,转移电子数目为
(4)ClO2具有强氧化性,若ClO2和Cl2在消毒时自身均被还原为Cl-,计算ClO2的消毒能力是等质量Cl2的
(5)若以NaClO2为原料制备ClO2,需要加入具有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】已知少量Fe与稀HNO3发生反应Fe+4HNO3=Fe(NO3)3+NO↑+2H2O。
(1)上述反应的离子方程式为___________ 。
(2)上述反应中,氧化剂是___________ (填化学式),氧化产物是___________ (填化学式)。
(3)若反应中消耗了2molHNO3,则生成标况下NO的体积为___________ 。
(4)用单线桥 法标出该反应的电子转移_________ 。
(1)上述反应的离子方程式为
(2)上述反应中,氧化剂是
(3)若反应中消耗了2molHNO3,则生成标况下NO的体积为
(4)用
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】将Cu投入足量的FeCl3的水溶液中,两者发生反应的化学方程式如下:2FeCl3+Cu= 2FeCl2+CuCl2。
(1)请用双线桥法标出电子转移的方向和数目___________ 。
(2)在该反应中,氧化剂是___________ , ___________ 元素被氧化。
(3)当有0.3mol电子发生转移时,发生反应的Cu的质量为___________ g。
(1)请用双线桥法标出电子转移的方向和数目
(2)在该反应中,氧化剂是
(3)当有0.3mol电子发生转移时,发生反应的Cu的质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】实验室可用MnO2和浓盐酸反应制取氯气:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(1)用单线桥标出电子转移的方向和数目________________________ 。
(2)将上述化学方程式改写为离子方程式________________________ 。
(3)浓盐酸在反应中显示出来的性质是____________ (填序号) 。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生2mol Cl2,则被氧化的HCl_____ mol,转移的电子的数目为________ 。
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。(1)用单线桥标出电子转移的方向和数目
(2)将上述化学方程式改写为离子方程式
(3)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生2mol Cl2,则被氧化的HCl
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】现有下列十种物质:①Cu(OH)2 ②干冰 ③Cu ④纯碱 ⑤BaCl2 ⑥Ca(OH)2 ⑦稀硝酸 ⑧盐酸 ⑨A12(SO4)3 ⑩KHSO4
(1)按物质的分类方法填写表格的空白处(填写序号):
写出④在水中的电离方程式为___________ 。
(2)写出下列物质相互之间反应的离子方程式:⑤+⑨___________
(3)经测定0.1mol/L⑩的水溶液与0.1mol/L⑧中的氢离子浓度基本相同,往固体①中加入过量的0.1mol/L⑩的水溶液,发生反应的离子方程式是___________ 。
(4)③与⑦发生反应的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,当有19.2gCu发生反应时,转移电子的物质的量为___________ mol,产生的NO在标准状况下的体积为___________ L。
(1)按物质的分类方法填写表格的空白处(填写序号):
| 分类标准 | 氧化物 | 非电解质 |
| 属于该类的物质 |
(2)写出下列物质相互之间反应的离子方程式:⑤+⑨
(3)经测定0.1mol/L⑩的水溶液与0.1mol/L⑧中的氢离子浓度基本相同,往固体①中加入过量的0.1mol/L⑩的水溶液,发生反应的离子方程式是
(4)③与⑦发生反应的化学方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,当有19.2gCu发生反应时,转移电子的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】由于NaNO2有毒,将含该物质的废水直接排放会引起水体的严重污染,所以这种废水必须经处理后才能排放。处理方法之一的原理如下:
 NaNO2+
NaNO2+ KI+
KI+ →
→ NO↑+
NO↑+ I2+
I2+ K2SO4+
K2SO4+ Na2SO4+
Na2SO4+
(1)请完成并配平该化学方程式___ 。
(2)在上述反应中,若要生成25.4gI2,则电子转移了____ 个。
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是____ 。现用铵盐来处理亚硝酸钠就能解决这个问题,写出这个离子方程式:___ 。
(4)亚硝酸钠可以与酸反应生成亚硝酸,亚硝酸是不稳定的弱酸,它只存在于冷的稀溶液中,易发生分解反应:3HNO2=2NO↑+HNO3+H2O。请从浓醋酸、氨水、纯碱、稀盐酸、碘化钾溶液、淀粉溶液中选择适当的物质,设计两个简单的实验鉴别NaNO2和NaCl。
方案1:所加试剂是____ (限用一种试剂),现象是____ 。
方案2:所加试剂是____ ,现象是____ 。
 NaNO2+
NaNO2+ KI+
KI+ →
→ NO↑+
NO↑+ I2+
I2+ K2SO4+
K2SO4+ Na2SO4+
Na2SO4+
(1)请完成并配平该化学方程式
(2)在上述反应中,若要生成25.4gI2,则电子转移了
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
(4)亚硝酸钠可以与酸反应生成亚硝酸,亚硝酸是不稳定的弱酸,它只存在于冷的稀溶液中,易发生分解反应:3HNO2=2NO↑+HNO3+H2O。请从浓醋酸、氨水、纯碱、稀盐酸、碘化钾溶液、淀粉溶液中选择适当的物质,设计两个简单的实验鉴别NaNO2和NaCl。
方案1:所加试剂是
方案2:所加试剂是
您最近一年使用:0次



