已知水在25 ℃和100 ℃时,电离平衡曲线如图所示:

(1)25 ℃时水的电离平衡曲线应为________ (填“A”或“B”),请说明理由____________ 。
(2)下列措施能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的是_____ (填序号)。
A 向纯水中投入少量Na2O2固体 B 将水加热至煮沸
C 向水中通入CO2 D 向水中加入NaCl

(1)25 ℃时水的电离平衡曲线应为
(2)下列措施能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的是
A 向纯水中投入少量Na2O2固体 B 将水加热至煮沸
C 向水中通入CO2 D 向水中加入NaCl
更新时间:2020-11-09 22:24:59
|
相似题推荐
填空题
|
容易
(0.94)
【推荐1】回答下列问题:
(1)0.2 mol·L-1 NaHSO4和0.1 mol·L-1 BaCl2溶液按等体积混合后,则溶液的pH等于________ 。
(2) 时,用pH=4和pH=11的强酸和强碱混合,使pH=10,则两溶液的体积比为
时,用pH=4和pH=11的强酸和强碱混合,使pH=10,则两溶液的体积比为________ 。
(3) 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为___________ mol·L-1。
(4) 时,
时,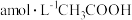 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
___________ 。
(1)0.2 mol·L-1 NaHSO4和0.1 mol·L-1 BaCl2溶液按等体积混合后,则溶液的pH等于
(2)
 时,用pH=4和pH=11的强酸和强碱混合,使pH=10,则两溶液的体积比为
时,用pH=4和pH=11的强酸和强碱混合,使pH=10,则两溶液的体积比为(3)
 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为(4)
 时,
时,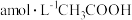 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】常温下0.01mol·L-1 NaOH溶液的pH=__________ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐3】水在25℃和95℃的电离平衡曲线如图所示:

(1)95℃时,水的电离平衡曲线应为___________ (填“A”或“B”),此时Kw=___________ 。
(2)95℃时水的离子积与25℃时水的离子积数值不同,原因是_______ 。25℃时,将pH=a、体积为Va的某一元强酸与pH=b、体积Vb的某一元强碱混合,若a+b=13,混合溶液pH=7,则Va∶Vb=________ 。

(1)95℃时,水的电离平衡曲线应为
(2)95℃时水的离子积与25℃时水的离子积数值不同,原因是
您最近一年使用:0次
填空题
|
容易
(0.94)
解题方法
【推荐2】常温下0.01mol·L-1 NaOH溶液的pH=__________ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】水的离子积常数:
(1)水的电离平衡常数表达式为K=____________ 。
(2)水的离子积常数表达式为KW=____________ 。
①常温时,Kw=____________ ,不仅适用于纯水,还适用于稀的____________ 。
②不同溶液中,c(H+)、c(OH-)可能不同,但任何溶液中由水电离出的c(H+)与c(OH-)总是______ 的。
(3)KW及影响因素:
a.25 ℃时:KW=____________ 。
b.水的电离是____________ 的可逆过程,故温度升高,KW______ 。
c.水的离子积常数只受______ 的影响,与c(H+)、c(OH-)的变化无关。
(1)水的电离平衡常数表达式为K=
(2)水的离子积常数表达式为KW=
①常温时,Kw=
②不同溶液中,c(H+)、c(OH-)可能不同,但任何溶液中由水电离出的c(H+)与c(OH-)总是
(3)KW及影响因素:
a.25 ℃时:KW=
b.水的电离是
c.水的离子积常数只受
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】①常温下,0.05mol/L硫酸溶液中,c(H+)=_______ mol/L,水电离的c(H+)=_________ mol/L。
②某温度,纯水中c(H+)=3×10-7mol/L,则:纯水中c(OH-)=_____ mol/L,此时温度____________ (填“高于”“低于”或“等于”)25℃。
若温度不变,滴入盐酸后c(H+)=5×10-4mol/L,则溶液中c(OH-)=_______ mol/L,由水电离的C(H+)=___________ mol/L。
②某温度,纯水中c(H+)=3×10-7mol/L,则:纯水中c(OH-)=
若温度不变,滴入盐酸后c(H+)=5×10-4mol/L,则溶液中c(OH-)=
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】中学化学实验中,淡黄色的pH试纸常用于测定溶液的酸碱性。在25 ℃时,若溶液呈中性,试纸不变色;呈酸性,试纸变红色;呈碱性,试纸变蓝色。而要精确测定溶液的pH,需用pH计。pH计主要通过测定溶液中H+浓度来测定溶液的pH。
(1)已知水中存在如下平衡:H2O+H2O H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是________ (填字母)。
A.向水中加入NaHSO4
B.向水中加入Na2CO3
C.加热水至100 ℃[其中c(H+)=1×10-6 mol·L-1]
D.在水中加入(NH4)2SO4
(2)现欲测定100 ℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显________ 色,溶液呈________ 性(填“酸”、“碱”或“中”);若用pH计测定,则pH________ 7(填“>”、“<”或“=”),溶液呈________ 性(填“酸”、“碱”或“中”)。
(1)已知水中存在如下平衡:H2O+H2O
 H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是A.向水中加入NaHSO4
B.向水中加入Na2CO3
C.加热水至100 ℃[其中c(H+)=1×10-6 mol·L-1]
D.在水中加入(NH4)2SO4
(2)现欲测定100 ℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐3】水在25℃和95℃的电离平衡曲线如图所示:

(1)95℃时,水的电离平衡曲线应为___________ (填“A”或“B”),此时Kw=___________ 。
(2)95℃时水的离子积与25℃时水的离子积数值不同,原因是_______ 。25℃时,将pH=a、体积为Va的某一元强酸与pH=b、体积Vb的某一元强碱混合,若a+b=13,混合溶液pH=7,则Va∶Vb=________ 。

(1)95℃时,水的电离平衡曲线应为
(2)95℃时水的离子积与25℃时水的离子积数值不同,原因是
您最近一年使用:0次

 ,其他水溶液中是否也存在
,其他水溶液中是否也存在


