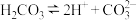25℃时,5种银盐的溶度积常数( )如表所示:
)如表所示:
下列说法正确的是
 )如表所示:
)如表所示:| 物质 |  |  |  | 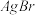 |  |
溶度积常数( ) ) |  | 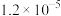 | 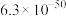 |  | 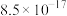 |
| A.氯化银、溴化银和碘化银的溶解度依次增大 |
| B.将硫酸银溶解于水形成饱和溶液后,向其中加入少量硫化钠溶液,不可能得到黑色沉淀 |
C.在 的 的 溶液中加入1滴( 溶液中加入1滴( 约20滴) 约20滴) 的 的 溶液(忽略溶液体积变化),不能观察到白色沉淀 溶液(忽略溶液体积变化),不能观察到白色沉淀 |
| D.将足量浅黄色溴化银固体浸泡在饱和氯化钠溶液中,有少量白色固体生成 |
更新时间:2020-10-13 11:01:00
|
相似题推荐
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】已知Ksp(AgCl)>Ksp(AgBr)>Ksp(AgI),下列有关说法正确的是
| A.向0.1mol·L-1的AgNO3溶液中加入等体积0.1mol·L-1的NaCl和0.1mol·L-1的NaBr混合液,生成的沉淀主要是AgCl |
| B.取等体积的AgCl和AgI饱和溶液混合,再加入足量AgNO3溶液,生成的沉淀主要是AgI |
| C.向含AgBr的饱和溶液中加入AgBr固体,则c(Ag+)变大 |
| D.向含AgI的饱和溶液中加入AgCl固体,则c(Ag+)变大 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】纯净的氯化钠是不潮解的,但粗盐很容易潮解,这主要是因为其中含有杂质MgCl2的缘故。为得到纯净的氯化钠,有人设计了一个实验:把买来的粗盐放入纯氯化钠饱和溶液一段时间,过滤,洗涤,可得纯净的氯化钠晶体。则下列说法正确的是
| A.设计实验的根据是NaCl的溶解平衡 |
| B.设计实验的根据是MgCl2比NaCl易溶于水 |
| C.在整个过程中NaCl饱和溶液浓度会变大(温度不变) |
| D.粗盐的晶粒大一些有利于提纯 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐1】下列实验操作、现象与结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向FeCl3和KSCN混合溶液中,加入少量KCl的固体 | 溶液颜色变浅 | FeCl3+2KSCN Fe(SCN)3+3KCl平衡向逆反应方向移动 Fe(SCN)3+3KCl平衡向逆反应方向移动 |
| B | 浓度均为0.10mol/L的Na2CO3和Na2S的混合溶液中滴入少量AgNO3溶液 | 产生黑色沉淀 | Ksp(Ag2S)>Ksp(Ag2CO3) |
| C | 向装有X溶液的试管中滴入NaOH溶液,将干燥的红色石蒸试纸置于试管口 | 无明显现象 | X溶液中无NH |
| D | 常温下,向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者红色更深 | 结合质子的能力:CO >HCO >HCO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】化学与社会、生活和科技密切相关。下列说法错误的是
| A.厨房中用热的纯碱液清除油污 |
| B.房屋装修入住前要保持一定的温度并通风 |
C. 可作为沉淀剂除去污水中重金属离子 可作为沉淀剂除去污水中重金属离子 |
| D.在汽车排气管上安装催化转化器治理汽车尾气的原理是催化剂能够改变化学反应进行的方向 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】下列说法正确的是( )
| A.向AgCl饱和溶液中加入NaCl固体,c(Cl-)增大,Ksp增大 |
B.已知 的 的 ,则所有含有固体MgCO3的溶液中,都有 ,则所有含有固体MgCO3的溶液中,都有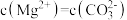 ,且 ,且 |
C.可通过比较 和 和 的Ksp的大小比较它们的溶解性 的Ksp的大小比较它们的溶解性 |
D.25 ℃时 ,故新生成的 AgCl可转化为AgI ,故新生成的 AgCl可转化为AgI |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】关于沉淀溶解平衡和溶度积常数,下列说法不正确的是
| A.Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
| B.已知25℃时Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe(OH)3+3H+⇌Fe3++3H2O的平衡常数K=4.0×104 |
| C.将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]>Ksp(CaSO4) |
| D.已知25℃时,Ksp[Mg(OH)2]=1.8×10-11,在MgCl2溶液中加入氨水调混合液的pH=11,产生沉淀,则此时溶液中的c(Mg2+)=1.8×10-5mol·L-1 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐1】室温下,下列实验不能 达到预期实验目的是
| 序号 | 实验内容 | 实验目的 |
| A | 取5mL0.1 KI溶液,加入1mL 0.1 KI溶液,加入1mL 0.1  溶液,用 溶液,用 萃取分液后,向水层滴入 萃取分液后,向水层滴入 溶液,溶液变血红色 溶液,溶液变血红色 | 证明 与 与 所发生的反应为可逆反应 所发生的反应为可逆反应 |
| B | 向10mL0.2   溶液中滴入滴0.1 溶液中滴入滴0.1  溶液,产生白色沉淀后,再滴加2滴0.1 溶液,产生白色沉淀后,再滴加2滴0.1   ,又生成红褐色沉淀 ,又生成红褐色沉淀 | 证明在相同温度下的Ksp: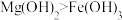 |
| C | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色变浅 固体,溶液红色变浅 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| D | 测定同温度同浓度的MOH溶液和 溶液的pH,MOH溶液pH更小 溶液的pH,MOH溶液pH更小 | 证明MOH是弱碱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】下列实验操作、现象与结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向FeCl3和KSCN混合溶液中,加入少量KCl的固体 | 溶液颜色变浅 | FeCl3+2KSCN Fe(SCN)3+3KCl平衡向逆反应方向移动 Fe(SCN)3+3KCl平衡向逆反应方向移动 |
| B | 浓度均为0.10mol/L的Na2CO3和Na2S的混合溶液中滴入少量AgNO3溶液 | 产生黑色沉淀 | Ksp(Ag2S)>Ksp(Ag2CO3) |
| C | 向装有X溶液的试管中滴入NaOH溶液,将干燥的红色石蒸试纸置于试管口 | 无明显现象 | X溶液中无NH |
| D | 常温下,向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者红色更深 | 结合质子的能力:CO >HCO >HCO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐3】已知20℃,Ksp[Mg(OH)2]=1.6×10-11,Ksp[Co(OH)2]=6.4×10-15,Co(OH)2为玫瑰红色难溶物,某同学进行如表实验,依据实验操作及现象,下列说法错误的是
| 实验操作 | 现象 | |
| 实验一 | 将镁条用砂纸打磨光亮后置于饱和氯化钠溶液中,滴加几滴酚酞 | 有无色气体和较多白色沉淀产生,溶液变红色 |
| 实验二 | 取出镁条,将悬浊液加热 | 红色加深 |
| 实验三 | 冷却后滴加适量CoCl2溶液 | 部分白色难溶物变成玫瑰红色难溶物 |
| A.镁条和水发生置换反应生成H2和Mg(OH)2 |
| B.NaCl增大了Mg(OH)2(s)在20℃水中的溶解度 |
| C.Mg(OH)2(s)⇌Mg2+(aq)+2OH-(aq)∆H>0 |
| D.加入适量CoCl2溶液后,c(Mg2+):c(Co2+)=2500:1 |
您最近一年使用:0次

 溶液中
溶液中 的水解反应方程式:
的水解反应方程式:
 的溶解平衡表达式:
的溶解平衡表达式: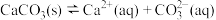
 的水解方程式:
的水解方程式: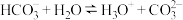
 的电离方程式:
的电离方程式: