Cl2O是黄棕色具有强烈刺激性气味的气体,熔点是-116℃,沸点是3.8℃;是一种强氧化剂,易溶于水且会与水反应生成次氯酸;高浓度的Cl2O易爆炸;Cl2O与有机物、还原剂接触或加热时会发生燃烧并爆炸。一种制取Cl2O的装置如图所示:
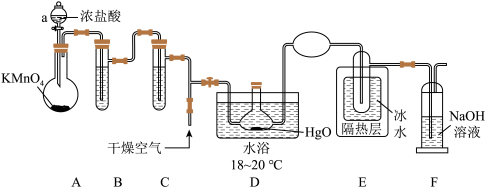
已知:①Cl2的熔点为-101℃,沸点是-34.6℃;②HgO+2Cl2=HgCl2+Cl2O
(1)仪器a的名称是___ ,装置A中制备Cl2的化学方程式为___ 。
(2)装置C的作用是___ 。
(3)通入干燥空气的目的是___ 。
(4)装置D与E之间不用橡胶管连接的原因是___ ,NaOH溶液的作用是___ (用离子反应方程式表示)。

已知:①Cl2的熔点为-101℃,沸点是-34.6℃;②HgO+2Cl2=HgCl2+Cl2O
(1)仪器a的名称是
(2)装置C的作用是
(3)通入干燥空气的目的是
(4)装置D与E之间不用橡胶管连接的原因是
更新时间:2020-11-25 16:49:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】如表是元素周期表的一部分,①~⑧代表对应的元素。

回答下列问题:
(1)①的一种核素的中子数为2,该核素的符号为_____ 。
(2)③在元素周期表中的位置是_____ ;⑧的原子结构示意图为_____ 。
(3)写出②的最高价氧化物的结构式_____ 。
(4)④和⑦的简单氢化物沸点更高的是_____ (填序号)。
(5)写出⑧的单质与⑤最高价氧化物对应水化物在常温下反应的离子方程式_____ 。
(6)设计实验比较⑤和⑥的金属性强弱______ 。

回答下列问题:
(1)①的一种核素的中子数为2,该核素的符号为
(2)③在元素周期表中的位置是
(3)写出②的最高价氧化物的结构式
(4)④和⑦的简单氢化物沸点更高的是
(5)写出⑧的单质与⑤最高价氧化物对应水化物在常温下反应的离子方程式
(6)设计实验比较⑤和⑥的金属性强弱
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是实验室制备氯气并验证氯气性质的装置(其中夹持装置已省略)。
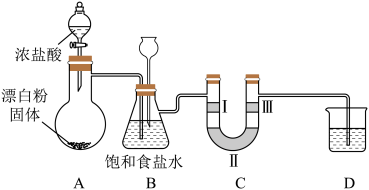
已知:装置A是氯气的发生装置,反应的化学方程式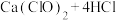 (浓)
(浓)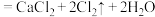
据此回答下列问题:
(1)上述反应中的氧化剂是_____ 。装置A中盛有漂白粉固体的玻璃仪器名称为_______ 。
(2)装置B也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:_______ 。
(3)装置C的作用是验证氯气是否具有漂白性,则装置C中I、II、III处依次应放入的物质是_______ (填字母)。
(4)装置D的作用是_______ ,其中发生的反应是_______ (用化学反应方程式表示)。

已知:装置A是氯气的发生装置,反应的化学方程式
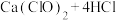 (浓)
(浓)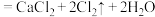
据此回答下列问题:
(1)上述反应中的氧化剂是
(2)装置B也是安全瓶,目的是监测实验进行时装置C中是否发生堵塞,请写出装置C中发生堵塞时装置B中的实验现象:
(3)装置C的作用是验证氯气是否具有漂白性,则装置C中I、II、III处依次应放入的物质是
| 序号 | I | II | III |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】以饱和食盐水为原料可以制得多种化工产品,其中部分物质的制取如图所示,水已略去,已知 为黄绿色气体,
为黄绿色气体, 气体在标准状况下的密度为
气体在标准状况下的密度为 ,
, 与
与 的反应可以用来生产漂白液,生成的
的反应可以用来生产漂白液,生成的 为漂白液的有效成分。
为漂白液的有效成分。

回答下列问题:
(1)气体 的化学式为
的化学式为___________ ;C在盛有 的集气瓶中燃烧时的现象为
的集气瓶中燃烧时的现象为___________ 。
(2)检验 中阴离子的方法为
中阴离子的方法为___________ 。
(3)标准状况下, 与足量
与足量 反应生成
反应生成 的质量为
的质量为______  。
。
(4)实验室一般用 的浓溶液配制其稀溶液,若配制
的浓溶液配制其稀溶液,若配制 的稀溶液,需用量筒量取
的稀溶液,需用量筒量取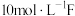 的浓溶液
的浓溶液______  。下列操作可能导致所配溶液浓度偏高的是
。下列操作可能导致所配溶液浓度偏高的是______ (填字母)。
A.量取 的浓溶液时仰视读数 B.转移前容量瓶中有水
的浓溶液时仰视读数 B.转移前容量瓶中有水
C.转移时液体溅出 D.定容时俯视读数
(5)A中金属元素的某种氧化物可以与 反应制取
反应制取 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
 为黄绿色气体,
为黄绿色气体, 气体在标准状况下的密度为
气体在标准状况下的密度为 ,
, 与
与 的反应可以用来生产漂白液,生成的
的反应可以用来生产漂白液,生成的 为漂白液的有效成分。
为漂白液的有效成分。
回答下列问题:
(1)气体
 的化学式为
的化学式为 的集气瓶中燃烧时的现象为
的集气瓶中燃烧时的现象为(2)检验
 中阴离子的方法为
中阴离子的方法为(3)标准状况下,
 与足量
与足量 反应生成
反应生成 的质量为
的质量为 。
。(4)实验室一般用
 的浓溶液配制其稀溶液,若配制
的浓溶液配制其稀溶液,若配制 的稀溶液,需用量筒量取
的稀溶液,需用量筒量取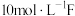 的浓溶液
的浓溶液 。下列操作可能导致所配溶液浓度偏高的是
。下列操作可能导致所配溶液浓度偏高的是A.量取
 的浓溶液时仰视读数 B.转移前容量瓶中有水
的浓溶液时仰视读数 B.转移前容量瓶中有水C.转移时液体溅出 D.定容时俯视读数
(5)A中金属元素的某种氧化物可以与
 反应制取
反应制取 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气,并模拟工业制漂白粉。请回答下列问题:
实验室制备和收集氯气的常用装置如下图。

(1)利用该装置制备氯气的化学方程式为___________ ,该反应中氧化剂和还原剂物质的量之比为___________ 。
(2)在实验过程中饱和食盐水的作用是___________ 。
(3)实验装置接口的连接顺序为___________ :
e→___________→___________→___________→___________→I→h→g→f。
(4)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,漂白粉的有效成分是___________ (填化学式)。
(5)瓶装漂白粉久置于空气中呈稀粥状而失效。试用化学方程式表示漂白粉在空气中易失效的原因:①___________ ;②___________ 。
实验室制备和收集氯气的常用装置如下图。

(1)利用该装置制备氯气的化学方程式为
(2)在实验过程中饱和食盐水的作用是
(3)实验装置接口的连接顺序为
e→___________→___________→___________→___________→I→h→g→f。
(4)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,漂白粉的有效成分是
(5)瓶装漂白粉久置于空气中呈稀粥状而失效。试用化学方程式表示漂白粉在空气中易失效的原因:①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾( )在能源、环保等方面有着广泛的用途。如图是实验室制备
)在能源、环保等方面有着广泛的用途。如图是实验室制备 的实验装置图,请回答下列问题:
的实验装置图,请回答下列问题:

(1)图中装有浓盐酸的仪器名称为_______ 。
(2)浓盐酸与高锰酸钾发生反应: ,
, ,理论上应消耗还原剂
,理论上应消耗还原剂_______  。
。
(3)乙装置中的试剂为_______ ,作用是_______
(4)写出丁装置中发生反应的离子方程式:_______ 。
(5)丙装置中生成 的离子方程式为
的离子方程式为_______ 。每消耗 ,理论上可以产生
,理论上可以产生 的质量为
的质量为_______
 )在能源、环保等方面有着广泛的用途。如图是实验室制备
)在能源、环保等方面有着广泛的用途。如图是实验室制备 的实验装置图,请回答下列问题:
的实验装置图,请回答下列问题:
(1)图中装有浓盐酸的仪器名称为
(2)浓盐酸与高锰酸钾发生反应:
 ,
, ,理论上应消耗还原剂
,理论上应消耗还原剂 。
。(3)乙装置中的试剂为
(4)写出丁装置中发生反应的离子方程式:
(5)丙装置中生成
 的离子方程式为
的离子方程式为 ,理论上可以产生
,理论上可以产生 的质量为
的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)实验室制氯气的反应原理为________ (方程式)KMnO4的氧化性比MnO2强得多,实验室也可以用KMnO4固体和浓盐酸反应制取氯气,反应方程式如下: 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①氧化剂和还原剂的物质的量之比为_______ ;
②当有lmol电子发生转移时,生成氯气的体积(标准状况)_________________ 。
③如果将20mL 12mol·L-1的浓盐酸与足量KMnO4充分反应,实际能收集到的氯气在标准状况下的体积将________ 。
A.≥1.68L B.>1.68L C.≤1.68L D.<1.68L
(2)现用如图所示的实验仪器及药品制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。

①按气流方向连接各仪器接口顺序是:a→____ 、____ → h 、i →____ 、____ →____ 。
②装置中,饱和食盐水的作用是____________ ;B装置中发生反应的化学方程式为___________ 。
(3)工业上以氯气和石灰乳为原料制取漂白粉,其化学反应方程式为___________ 。
①氧化剂和还原剂的物质的量之比为
②当有lmol电子发生转移时,生成氯气的体积(标准状况)
③如果将20mL 12mol·L-1的浓盐酸与足量KMnO4充分反应,实际能收集到的氯气在标准状况下的体积将
A.≥1.68L B.>1.68L C.≤1.68L D.<1.68L
(2)现用如图所示的实验仪器及药品制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹省略)。

①按气流方向连接各仪器接口顺序是:a→
②装置中,饱和食盐水的作用是
(3)工业上以氯气和石灰乳为原料制取漂白粉,其化学反应方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硫酸铜是一种常见的无机化合物,可形成CuSO4 .5H2O、CuSO4 .H2O等多种结 晶水合物,它可用作杀菌剂,还可用于电镀和电解精炼铜。回答下列问题:
(1)CuSO4 .5H2O的俗名是________ 。
(2)工业利用“冶炼硫酸铜”(主要成分CuSO4含少量Fe2+、AsO2-、Ca2+等杂质)提纯 制备“电镀硫酸铜”(CuSO4 .H2O)的生产流程如下:

溶解所用的酸最适宜的是_____ ,氧化的产物中有比H3AsO4和______ ,调节pH时生成固体的主要成分除FeAsO4、Fe((OH)) 3外还有______ ,生成FeAsO4反应的离子方程是________ ,操作a需经过蒸发浓缩、____ 、过滤、洗涤、干燥等步骤,其中洗涤的过程中常用无水乙醇,其作用是______________________ 。

(3)用CuSO4溶液电解精炼铜的装置如图所示,粗铜中含 锌、银、铂杂质,阳极发生的电极反应式_______ : 目前世界正在 大力开展用Cu+的络合物作电解质溶液制备纯铜的研究,电解Cu+的 络合物与电解CuSO4溶液相比较,优点是________________ ,
(1)CuSO4 .5H2O的俗名是
(2)工业利用“冶炼硫酸铜”(主要成分CuSO4含少量Fe2+、AsO2-、Ca2+等杂质)提纯 制备“电镀硫酸铜”(CuSO4 .H2O)的生产流程如下:

溶解所用的酸最适宜的是

(3)用CuSO4溶液电解精炼铜的装置如图所示,粗铜中含 锌、银、铂杂质,阳极发生的电极反应式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提取碘的方法之一,其流程如下:

资料显示:
Ⅰ.pH=2 时, NaNO2溶液只能将 I-氧化为 I2,同时生成 NO;
Ⅱ.I2+5Cl2+6H2O=2HIO3+10HCl;
Ⅲ.I2在碱性溶液中反应生成I-和IO3-。
(1)反应①的离子方程式_____ 。
(2)方案甲中,根据 I2的特性,分离操作 X 的名称是_____ 。
(3)Cl2、酸性 KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的 I-却选择了价格较高的NaNO2,原因是_____ 。
(4)方案乙中,已知反应③过滤后,滤液中仍存在少量的 I2、I-、IO3-。 请检验滤液中的I-,将实验方案补充完整。实验中可供选择的试剂:稀 H2SO4、淀粉溶液、Fe2(SO4)3溶液。
A.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
B._____ 。

资料显示:
Ⅰ.pH=2 时, NaNO2溶液只能将 I-氧化为 I2,同时生成 NO;
Ⅱ.I2+5Cl2+6H2O=2HIO3+10HCl;
Ⅲ.I2在碱性溶液中反应生成I-和IO3-。
(1)反应①的离子方程式
(2)方案甲中,根据 I2的特性,分离操作 X 的名称是
(3)Cl2、酸性 KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的 I-却选择了价格较高的NaNO2,原因是
(4)方案乙中,已知反应③过滤后,滤液中仍存在少量的 I2、I-、IO3-。 请检验滤液中的I-,将实验方案补充完整。实验中可供选择的试剂:稀 H2SO4、淀粉溶液、Fe2(SO4)3溶液。
A.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
B.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】我国科学家发现氢化钙( )纳米颗粒助力氢危疫癌症治疗。资料显示:
)纳米颗粒助力氢危疫癌症治疗。资料显示: 易与水反应。某小组选择下列装置制备氢化钙并测定其纯度。
易与水反应。某小组选择下列装置制备氢化钙并测定其纯度。

回答下列问题:
(1)实验室里将钙保存在___________ 中。
(2)气流从左至右,装置排序为___________ (填字母,装置可重复使用)。
(3)装置B的作用有___________ (用离子方程式表示)和吸收挥发出来的氯化氢。
(4)实验中,先启动A中反应,当E装置___________ (填实验现象)时点燃C处酒精灯,这样操作的目的是___________ 。
(5)当C装置中钙完全反应时,停止A装置中反应的操作是___________ 。
(6)测定产品纯度。取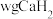 产品溶于足量蒸馏水中,加入过量
产品溶于足量蒸馏水中,加入过量 溶液,过滤,用稀硫酸溶解
溶液,过滤,用稀硫酸溶解 ,用
,用 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液 。
。
① 与水反应的化学方程式为
与水反应的化学方程式为___________ ;
②该 样品纯度为
样品纯度为___________ (用含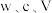 的代数式表示);若产品中混有CaO、Ca杂质,测得结果
的代数式表示);若产品中混有CaO、Ca杂质,测得结果___________ (填“偏高”“偏低”或“无影响”)。
 )纳米颗粒助力氢危疫癌症治疗。资料显示:
)纳米颗粒助力氢危疫癌症治疗。资料显示: 易与水反应。某小组选择下列装置制备氢化钙并测定其纯度。
易与水反应。某小组选择下列装置制备氢化钙并测定其纯度。
回答下列问题:
(1)实验室里将钙保存在
(2)气流从左至右,装置排序为
(3)装置B的作用有
(4)实验中,先启动A中反应,当E装置
(5)当C装置中钙完全反应时,停止A装置中反应的操作是
(6)测定产品纯度。取
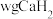 产品溶于足量蒸馏水中,加入过量
产品溶于足量蒸馏水中,加入过量 溶液,过滤,用稀硫酸溶解
溶液,过滤,用稀硫酸溶解 ,用
,用 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液 。
。①
 与水反应的化学方程式为
与水反应的化学方程式为②该
 样品纯度为
样品纯度为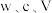 的代数式表示);若产品中混有CaO、Ca杂质,测得结果
的代数式表示);若产品中混有CaO、Ca杂质,测得结果
您最近一年使用:0次



