重铬酸钾(K2Cr2O7)是工业生产和实验室的重要氧化剂。实验室模拟工业生产重铬酸钾时用铬铁矿(主要成分为FeO·Cr2O3)、纯碱、烧碱、氯酸钾等为原料先制得铬酸钠(Na2CrO4),涉及的主要反应是6FeO·Cr2O3 + 24NaOH +7KClO3 12Na2CrO4 +3Fe2O3 +7KCl + 12H2O,然后将铬酸钠转化为K2Cr2O7。其主要工艺如下:
12Na2CrO4 +3Fe2O3 +7KCl + 12H2O,然后将铬酸钠转化为K2Cr2O7。其主要工艺如下:
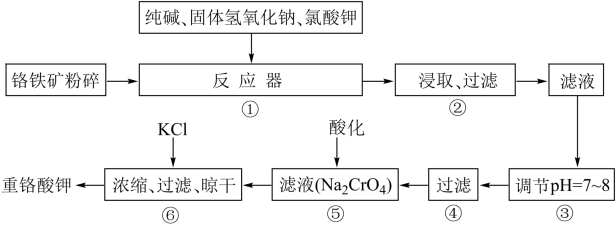
试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:__________________________________________ 。
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式:_____________________________________ 。
(3)操作③的目的是什么,用简要的文字和化学方程式说明:________________________ 。
(4)操作④中,酸化时,CrO 转化为Cr2O
转化为Cr2O ,写出平衡转化的离子方程式:
,写出平衡转化的离子方程式:___________ 。
(5)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol/LH2SO4溶液和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O =2I-+S4O
=2I-+S4O )。
)。
①判断达到滴定终点的依据是:_____________________________________________ ;
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中的重铬酸钾的纯度为______ (设K2Cr2O7的摩尔质量为294g·mol -1,整个过程中其它杂质不参与反应)。
 12Na2CrO4 +3Fe2O3 +7KCl + 12H2O,然后将铬酸钠转化为K2Cr2O7。其主要工艺如下:
12Na2CrO4 +3Fe2O3 +7KCl + 12H2O,然后将铬酸钠转化为K2Cr2O7。其主要工艺如下:
试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式:
(3)操作③的目的是什么,用简要的文字和化学方程式说明:
(4)操作④中,酸化时,CrO
 转化为Cr2O
转化为Cr2O ,写出平衡转化的离子方程式:
,写出平衡转化的离子方程式:(5)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol/LH2SO4溶液和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O
 =2I-+S4O
=2I-+S4O )。
)。①判断达到滴定终点的依据是:
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中的重铬酸钾的纯度为
更新时间:2020-11-19 15:04:23
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选甲基橙作指示剂。
(1)配制250mL 0.2000 mol/L盐酸标准溶液,所需玻璃仪器有______ 、______ 量筒、烧杯、玻璃棒。
(2)盛装0.2000 mol/L盐酸标准液应该用______ 式滴定管。(填“酸”或“碱”)
(3)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_________ ,直到加入一滴盐酸后,溶液由_________ ,即到终点。
(4)滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管;
④装标准溶液和待测液并调整液面(记录初始读数);
⑤用蒸馏水洗涤玻璃仪器;⑥滴定操作
正确的操作顺序为:_________ 。
(5)有关数据记录如下:
则NaOH溶液的物质的量浓度为__________ mol/L。
(6)若滴定时锥形瓶未干燥,则测定结果____________ ;若滴定前平视读数,滴定终点时仰视读数,则所测碱的浓度值_________ 。(填“无影响”、“偏高”或“偏低”)。
(1)配制250mL 0.2000 mol/L盐酸标准溶液,所需玻璃仪器有
(2)盛装0.2000 mol/L盐酸标准液应该用
(3)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视
(4)滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管;
④装标准溶液和待测液并调整液面(记录初始读数);
⑤用蒸馏水洗涤玻璃仪器;⑥滴定操作
正确的操作顺序为:
(5)有关数据记录如下:
| 实验序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.60 | 20.70 |
| 2 | 20.00 | 6.00 | 25.90 |
| 3 | 20.00 | 1.40 | 23.20 |
则NaOH溶液的物质的量浓度为
(6)若滴定时锥形瓶未干燥,则测定结果
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】中学化学常见的滴定法包括中和滴定法、氧化还原反应滴定法等。
(1)探究小组甲用酸性KMnO4溶液滴定某补血剂[主要成分硫酸亚铁晶体(FeSO4•7H2O)]中铁元素的含量。
①下列滴定装置中(夹持部分略去),最合理的是:__________ (填字母序号)。

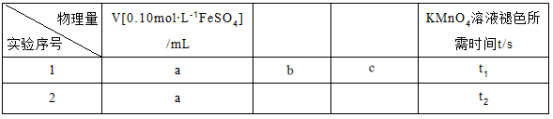
②该小组拟在同浓度的FeSO4溶液中,探究酸性KMnO4溶液浓度对Fe2+被氧化时反应速率的影响。限选试剂与仪器:0.10mol∙L-1FeSO4、0.02mol∙L-1酸性KMnO4、蒸馏水、锥形瓶、试管、胶头滴管、量筒、秒表。参照下表格式,完成实验表格(列出所选试剂体积和数据;数据用字母表示)。_____________ 、_____________ 、_____________ 、_____________ 。
(2)常温下,探究小组乙将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液的pH随加入盐酸体积的变化曲线如图所示。
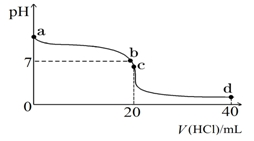
①a点处假设溶液的pH=10,则该点处由水电离产生的c(OH-)=__________________ 。
②取c点时的饱和溶液并向其加入水玻璃(硅酸钠水溶液),振荡、静置。写出实验现象并用必要的文字和相关离子方程式给予解释:___________________________________ 。
③d点所示溶液中离子浓度由大到小的排序是_______________________________ 。
(1)探究小组甲用酸性KMnO4溶液滴定某补血剂[主要成分硫酸亚铁晶体(FeSO4•7H2O)]中铁元素的含量。
①下列滴定装置中(夹持部分略去),最合理的是:

②该小组拟在同浓度的FeSO4溶液中,探究酸性KMnO4溶液浓度对Fe2+被氧化时反应速率的影响。限选试剂与仪器:0.10mol∙L-1FeSO4、0.02mol∙L-1酸性KMnO4、蒸馏水、锥形瓶、试管、胶头滴管、量筒、秒表。参照下表格式,完成实验表格(列出所选试剂体积和数据;数据用字母表示)。

(2)常温下,探究小组乙将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液的pH随加入盐酸体积的变化曲线如图所示。

①a点处假设溶液的pH=10,则该点处由水电离产生的c(OH-)=
②取c点时的饱和溶液并向其加入水玻璃(硅酸钠水溶液),振荡、静置。写出实验现象并用必要的文字和相关离子方程式给予解释:
③d点所示溶液中离子浓度由大到小的排序是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视________ 。直到因加入一滴盐酸后,溶液由黄色变为橙色,并________ 为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是( ) 。
A 酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B 滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C 酸式滴定管在滴定前有气泡,滴定后气泡消失
D 读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
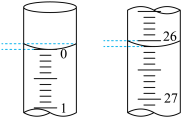
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为________ mL,终点读数为________ mL;所用盐酸溶液的体积为________ mL。
(4)某学生根据3次实验分别记录有关数据如表:
依据上表数据列式计算该NaOH溶液的物质的量浓度_______________ 。
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
A 酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B 滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C 酸式滴定管在滴定前有气泡,滴定后气泡消失
D 读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为

(4)某学生根据3次实验分别记录有关数据如表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
| 滴定前读数 | 滴定后读数 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该NaOH溶液的物质的量浓度
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】氨是重要的工业原料,在农业、医药,国防和化工等领域有重要应用。
I.某温度下水的离子积常数为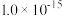 ,向
,向 的氨水中逐滴加入
的氨水中逐滴加入 的盐酸,所得溶液的
的盐酸,所得溶液的 ,溶液中
,溶液中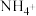 和
和 物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。
物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。
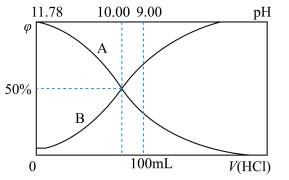
(1)表示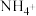 物质的量分数变化的曲线是
物质的量分数变化的曲线是___________ (填“A”或“B”)。
(2)该温度下, 的电离平衡常数为
的电离平衡常数为___________ 。
(3)当加入盐酸体积为 时,溶液中
时,溶液中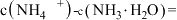
_______  (用数字表示精确值)。
(用数字表示精确值)。
Ⅱ.铵盐在日常生活中用处广泛, 常作食品加工中的食品添加剂,用于焙烤食品。请回答下列问题:
常作食品加工中的食品添加剂,用于焙烤食品。请回答下列问题:
(4) 可作净水剂,其原理是
可作净水剂,其原理是_________________________________ (用离子方程式说明)。
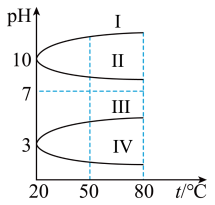
(5)下列图像为 的几种电解质溶液的pH随温度变化的曲线。
的几种电解质溶液的pH随温度变化的曲线。
其中符合 溶液的pH随温度变化的曲线是
溶液的pH随温度变化的曲线是___________ (填罗马数字), 溶液的pH随温度变化的原因是
溶液的pH随温度变化的原因是_________________________________ 。
(6)相同条件下,下列五种溶液中 由到小的大顺序是
由到小的大顺序是___________ (填序号)。
①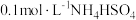 溶液
溶液
② 溶液
溶液
③ 溶液
溶液
④ 溶液
溶液
⑤ 氨水
氨水
I.某温度下水的离子积常数为
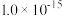 ,向
,向 的氨水中逐滴加入
的氨水中逐滴加入 的盐酸,所得溶液的
的盐酸,所得溶液的 ,溶液中
,溶液中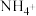 和
和 物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。
物质的量分数与加入盐酸的体积的关系如图所示,根据图象回答下列问题。
(1)表示
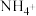 物质的量分数变化的曲线是
物质的量分数变化的曲线是(2)该温度下,
 的电离平衡常数为
的电离平衡常数为(3)当加入盐酸体积为
 时,溶液中
时,溶液中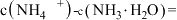
 (用数字表示精确值)。
(用数字表示精确值)。Ⅱ.铵盐在日常生活中用处广泛,
 常作食品加工中的食品添加剂,用于焙烤食品。请回答下列问题:
常作食品加工中的食品添加剂,用于焙烤食品。请回答下列问题:(4)
 可作净水剂,其原理是
可作净水剂,其原理是(5)下列图像为
 的几种电解质溶液的pH随温度变化的曲线。
的几种电解质溶液的pH随温度变化的曲线。其中符合
 溶液的pH随温度变化的曲线是
溶液的pH随温度变化的曲线是 溶液的pH随温度变化的原因是
溶液的pH随温度变化的原因是
(6)相同条件下,下列五种溶液中
 由到小的大顺序是
由到小的大顺序是①
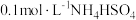 溶液
溶液②
 溶液
溶液③
 溶液
溶液④
 溶液
溶液⑤
 氨水
氨水
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】久置的 溶液变黄,一般认为是二价铁被氧化为三价铁的缘故。某研究小组为研究溶液中
溶液变黄,一般认为是二价铁被氧化为三价铁的缘故。某研究小组为研究溶液中 被
被 氧化的过程,查阅资料发现:溶液中
氧化的过程,查阅资料发现:溶液中 的氧化过程分为先后两步,首先是
的氧化过程分为先后两步,首先是 水解接着水解产物被
水解接着水解产物被 氧化。于是小组同学决定研究常温下不同pH对
氧化。于是小组同学决定研究常温下不同pH对 被
被 氧化的影响,并测定了
氧化的影响,并测定了 氧化率随时间变化的关系,结果如图。
氧化率随时间变化的关系,结果如图。
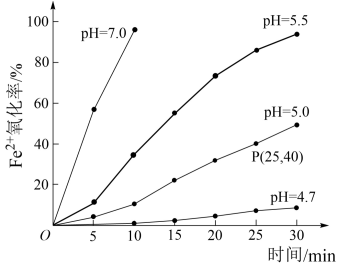
回答下列问题:
(1)写出 水解的离子方程式
水解的离子方程式________________ ;要抑制 水解,可以采取的措施是
水解,可以采取的措施是________ 。
(2)若配制的 溶液浓度为
溶液浓度为 ,反应过程中溶液体积不变,计算图中P点
,反应过程中溶液体积不变,计算图中P点 的氧化速率
的氧化速率________________ 。
(3)在酸性条件下, 被
被 氧化的反应方程式为:
氧化的反应方程式为: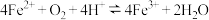 ,已知常温下该反应的平衡常数很大。则下列说法正确的是
,已知常温下该反应的平衡常数很大。则下列说法正确的是________ 。
a. 转化为
转化为 的趋势很大 b.
的趋势很大 b. 转化为
转化为 的速率很大
的速率很大
c.该反应进行得很完全 d.酸性条件下 不会被氧化
不会被氧化
(4)结合图象分析可知,pH越大 氧化率越
氧化率越________ (填“大”或“小”)。
(5)研究小组在查阅资料时还得知:氧气的氧化性随溶液的酸性增强而增强。通过以上研究可知,配制 溶液的正确做法是
溶液的正确做法是________________________ 。
 溶液变黄,一般认为是二价铁被氧化为三价铁的缘故。某研究小组为研究溶液中
溶液变黄,一般认为是二价铁被氧化为三价铁的缘故。某研究小组为研究溶液中 被
被 氧化的过程,查阅资料发现:溶液中
氧化的过程,查阅资料发现:溶液中 的氧化过程分为先后两步,首先是
的氧化过程分为先后两步,首先是 水解接着水解产物被
水解接着水解产物被 氧化。于是小组同学决定研究常温下不同pH对
氧化。于是小组同学决定研究常温下不同pH对 被
被 氧化的影响,并测定了
氧化的影响,并测定了 氧化率随时间变化的关系,结果如图。
氧化率随时间变化的关系,结果如图。
回答下列问题:
(1)写出
 水解的离子方程式
水解的离子方程式 水解,可以采取的措施是
水解,可以采取的措施是(2)若配制的
 溶液浓度为
溶液浓度为 ,反应过程中溶液体积不变,计算图中P点
,反应过程中溶液体积不变,计算图中P点 的氧化速率
的氧化速率(3)在酸性条件下,
 被
被 氧化的反应方程式为:
氧化的反应方程式为: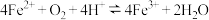 ,已知常温下该反应的平衡常数很大。则下列说法正确的是
,已知常温下该反应的平衡常数很大。则下列说法正确的是a.
 转化为
转化为 的趋势很大 b.
的趋势很大 b. 转化为
转化为 的速率很大
的速率很大c.该反应进行得很完全 d.酸性条件下
 不会被氧化
不会被氧化(4)结合图象分析可知,pH越大
 氧化率越
氧化率越(5)研究小组在查阅资料时还得知:氧气的氧化性随溶液的酸性增强而增强。通过以上研究可知,配制
 溶液的正确做法是
溶液的正确做法是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】下图中A、B、C、D分别为AlCl3、NaOH、NH4HSO4、Na2CO3溶液,实验过程和记录如下图所示(无关物质已经略去):
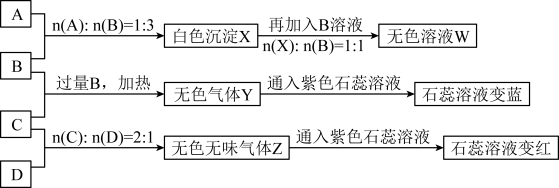
请回答:
(1)W的溶液加热蒸干并灼烧最后所得固体为__________ 。
(2)D溶液pH___ (填“大于”、“小于”或“等于”)7,原因是(用离子方程式表示)_______ 。
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是_________ 。(用化学式表示)
(4)等物质的浓度的C溶液与NH4Cl溶液相比较,c(NH4+):前者_____ 后者(填“<”“>”“=”)。
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是____ 。

请回答:
(1)W的溶液加热蒸干并灼烧最后所得固体为
(2)D溶液pH
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是
(4)等物质的浓度的C溶液与NH4Cl溶液相比较,c(NH4+):前者
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】磁选后的炼铁高钛炉渣,主要成分有 、
、 、
、 、
、 、
、 以及少量的
以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
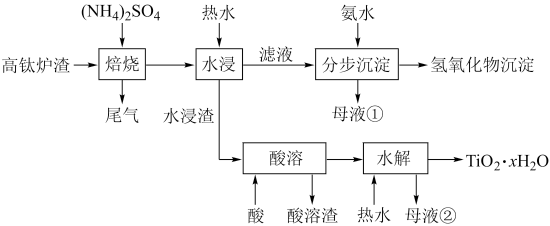
该工艺条件下,有关金属离子开始沉淀和沉淀完全的 见下表
见下表
回答下列问题:
(1)“焙烧”中, 、
、 几乎不发生反应,
几乎不发生反应, 、
、 、
、 、
、 转化为相应的硫酸盐,写出
转化为相应的硫酸盐,写出 转化为
转化为 的化学方程式
的化学方程式_______ 。
(2)“水浸”后“滤液”的 约为2.0,在“分步沉淀”时用氨水逐步调节
约为2.0,在“分步沉淀”时用氨水逐步调节 至11.6,依次析出的金属离子是
至11.6,依次析出的金属离子是_______ 。
(3)“水浸渣”在160℃“酸溶”最适合的酸是_______ 。“酸溶渣”的成分是_______ 、_______ 。
(4)“酸溶”后,将溶液适当稀释并加热, 水解析出
水解析出 沉淀,该反应的离子方程式是
沉淀,该反应的离子方程式是_______ 。
(5)将“母液①”和“母液②”混合,吸收尾气,经处理得_______ ,循环利用。
 、
、 、
、 、
、 、
、 以及少量的
以及少量的 。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
。为节约和充分利用资源,通过如下工艺流程回收钛、铝、镁等。
该工艺条件下,有关金属离子开始沉淀和沉淀完全的
 见下表
见下表| 金属离子 |  |  |  |  |
开始沉淀的 | 2.2 | 3.5 | 9.5 | 12.4 |
沉淀完全 的 的 | 3.2 | 4.7 | 11.1 | 13.8 |
(1)“焙烧”中,
 、
、 几乎不发生反应,
几乎不发生反应, 、
、 、
、 、
、 转化为相应的硫酸盐,写出
转化为相应的硫酸盐,写出 转化为
转化为 的化学方程式
的化学方程式(2)“水浸”后“滤液”的
 约为2.0,在“分步沉淀”时用氨水逐步调节
约为2.0,在“分步沉淀”时用氨水逐步调节 至11.6,依次析出的金属离子是
至11.6,依次析出的金属离子是(3)“水浸渣”在160℃“酸溶”最适合的酸是
(4)“酸溶”后,将溶液适当稀释并加热,
 水解析出
水解析出 沉淀,该反应的离子方程式是
沉淀,该反应的离子方程式是(5)将“母液①”和“母液②”混合,吸收尾气,经处理得
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
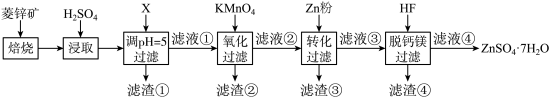
【推荐2】硫酸锌(ZnSO4)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO3,杂质为SiO2以及Ca、Mg、Fe、Cu等的化合物。其制备流程如下:
回答下列问题:
(1)加入物质X调溶液 ,最适宜使用的X是
,最适宜使用的X是_______ (填标号)。
A. B.
B. C.
C.
滤渣①的主要成分是_______ 、_______ 、_______ 。
| 离子 |  |  |  |  |  |
 |  | 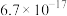 | 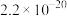 |  | 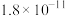 |
(1)加入物质X调溶液
 ,最适宜使用的X是
,最适宜使用的X是A.
 B.
B. C.
C.
滤渣①的主要成分是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铋酸钠( ,相对分子质量为280)常用作分析试剂、氧化剂,还用于制药工业。它是一种浅黄色至褐色的无定形粉末。工业上以辉铋矿(主要成分是
,相对分子质量为280)常用作分析试剂、氧化剂,还用于制药工业。它是一种浅黄色至褐色的无定形粉末。工业上以辉铋矿(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备铋酸钠的流程如下:
等杂质)为原料制备铋酸钠的流程如下:
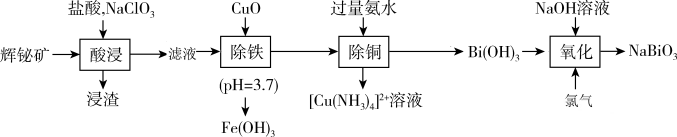
已知:滤液中含有 、
、 、
、 和
和 、
、 等离子。
等离子。
回答下列问题:
(1)浸渣的主要成分是_______ (填化学式);提高“酸浸”速率的措施有_______ (写出其中一条即可)。
(2)“酸浸”时, 参与的反应中氧化剂与还原剂的物质的量之比为
参与的反应中氧化剂与还原剂的物质的量之比为_______ 。
(3)加入CuO粉末调节滤液 可除去其中的
可除去其中的 ,其原因是
,其原因是_______ 。
(4)“除铜”过程中, 先与氨水反应生成
先与氨水反应生成 沉淀,再溶于氨水生成
沉淀,再溶于氨水生成 。常温下,加入氨水使
。常温下,加入氨水使 沉淀完全,则所调节溶液的
沉淀完全,则所调节溶液的
_______ 。(计算结果保留1位小数)。(已知: 沉淀完全时的浓度为
沉淀完全时的浓度为 mol·L
mol·L ,
,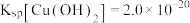 ,
, )
)
(5)已知 不溶于冷水,取少量
不溶于冷水,取少量 于试管中,加入浓盐酸,产生黄绿色气体,该反应的离子方程式为
于试管中,加入浓盐酸,产生黄绿色气体,该反应的离子方程式为_______ 。从 热溶液中得到
热溶液中得到 晶体的操作依次为
晶体的操作依次为_______ 、洗涤、干燥。
(6)取上述所制备的 产品10.00 g,加入足量稀硫酸和
产品10.00 g,加入足量稀硫酸和 稀溶液使其完全反应,再用1.20 mol·L
稀溶液使其完全反应,再用1.20 mol·L
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色褪去,且半分钟内不再恢复原色,即达到滴定终点,重复此操作2~3次,平均消耗
,当溶液紫红色褪去,且半分钟内不再恢复原色,即达到滴定终点,重复此操作2~3次,平均消耗 标准溶液的体积为28.00 mL,该产品的纯度为
标准溶液的体积为28.00 mL,该产品的纯度为_______ %(计算结果保留3位有效数字)。(已知: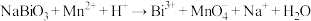 ,
,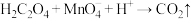
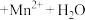 ,两离子反应方程式均未配平)
,两离子反应方程式均未配平)
 ,相对分子质量为280)常用作分析试剂、氧化剂,还用于制药工业。它是一种浅黄色至褐色的无定形粉末。工业上以辉铋矿(主要成分是
,相对分子质量为280)常用作分析试剂、氧化剂,还用于制药工业。它是一种浅黄色至褐色的无定形粉末。工业上以辉铋矿(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备铋酸钠的流程如下:
等杂质)为原料制备铋酸钠的流程如下:
已知:滤液中含有
 、
、 、
、 和
和 、
、 等离子。
等离子。回答下列问题:
(1)浸渣的主要成分是
(2)“酸浸”时,
 参与的反应中氧化剂与还原剂的物质的量之比为
参与的反应中氧化剂与还原剂的物质的量之比为(3)加入CuO粉末调节滤液
 可除去其中的
可除去其中的 ,其原因是
,其原因是(4)“除铜”过程中,
 先与氨水反应生成
先与氨水反应生成 沉淀,再溶于氨水生成
沉淀,再溶于氨水生成 。常温下,加入氨水使
。常温下,加入氨水使 沉淀完全,则所调节溶液的
沉淀完全,则所调节溶液的
 沉淀完全时的浓度为
沉淀完全时的浓度为 mol·L
mol·L ,
,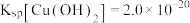 ,
, )
)(5)已知
 不溶于冷水,取少量
不溶于冷水,取少量 于试管中,加入浓盐酸,产生黄绿色气体,该反应的离子方程式为
于试管中,加入浓盐酸,产生黄绿色气体,该反应的离子方程式为 热溶液中得到
热溶液中得到 晶体的操作依次为
晶体的操作依次为(6)取上述所制备的
 产品10.00 g,加入足量稀硫酸和
产品10.00 g,加入足量稀硫酸和 稀溶液使其完全反应,再用1.20 mol·L
稀溶液使其完全反应,再用1.20 mol·L
 标准溶液滴定生成的
标准溶液滴定生成的 ,当溶液紫红色褪去,且半分钟内不再恢复原色,即达到滴定终点,重复此操作2~3次,平均消耗
,当溶液紫红色褪去,且半分钟内不再恢复原色,即达到滴定终点,重复此操作2~3次,平均消耗 标准溶液的体积为28.00 mL,该产品的纯度为
标准溶液的体积为28.00 mL,该产品的纯度为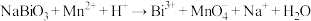 ,
,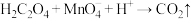
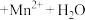 ,两离子反应方程式均未配平)
,两离子反应方程式均未配平)
您最近半年使用:0次



