Ⅰ.在工业上次磷酸(H3PO2)常用于化学镀银,发生的反应如下:Ag+ +H3PO2 +H2O →Ag↓ +H3PO4 +H+,请回答下列问题:
(1)H3PO2 中,P 元素的化合价为_____ ;该反应中,H3PO2 被_____ (填“氧化”或“还原”)。
(2)配平该离子方程:____ Ag+ +_____ H3PO2 +_____ H2O =_____ Ag↓ +_____ H3PO4 +_____ H+。
(3)H3PO2 是一元弱酸,写出其与足量NaOH 溶液反应的离子方程式:______ 。
Ⅱ. 现实验室用MnO2 和浓盐酸制氯气的反应为 MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑。回答下列问题:
MnCl2+2H2O+Cl2↑。回答下列问题:
(4)其中被还原的元素是_____ ,氧化剂是_____ ,还原剂是_____ ,还原产 物是_____ 。
(5)用双线桥标出该反应的电子转移的方向和数目:_____ 。
(1)H3PO2 中,P 元素的化合价为
(2)配平该离子方程:
(3)H3PO2 是一元弱酸,写出其与足量NaOH 溶液反应的离子方程式:
Ⅱ. 现实验室用MnO2 和浓盐酸制氯气的反应为 MnO2+4HCl(浓)
 MnCl2+2H2O+Cl2↑。回答下列问题:
MnCl2+2H2O+Cl2↑。回答下列问题:(4)其中被还原的元素是
(5)用双线桥标出该反应的电子转移的方向和数目:
更新时间:2020-12-04 01:30:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】写出下列反应的离子方程式:
(1)自然界中Cr主要以+3价和+6价形式存在。 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:_______ 。
(2)常温下,氰化钠(NaCN)能与过氧化氢溶液反应,生成一种酸式盐和一种能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。写出该反应的离子方程式:_______ 。
(3)连二亚硫酸钠(Na2S2O4)常作木浆造纸的漂白剂。向甲酸钠(HCOONa)与 的混合溶液中通入SO2气体,可得到连二亚硫酸钠及一种可用作灭火剂的气体,相应的化学反应的离子方程式为
的混合溶液中通入SO2气体,可得到连二亚硫酸钠及一种可用作灭火剂的气体,相应的化学反应的离子方程式为_______ ,碱性条件下连二亚硫酸钠溶液与 溶液反应可得到单质银,相应的离子方程式为
溶液反应可得到单质银,相应的离子方程式为_______ 。
(4)煤燃烧排放的烟气含有SO2和 ,形成酸雨,污染大气,采用
,形成酸雨,污染大气,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有 和NO的烟气,写出
和NO的烟气,写出 溶液脱硝(主要转化为
溶液脱硝(主要转化为 )过程中主要反应的离子方程式:
)过程中主要反应的离子方程式:_______ 。
(1)自然界中Cr主要以+3价和+6价形式存在。
 中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将
中的Cr能引起细胞的突变,可以用亚硫酸钠在酸性条件下将 还原。写出反应的离子方程式:
还原。写出反应的离子方程式:(2)常温下,氰化钠(NaCN)能与过氧化氢溶液反应,生成一种酸式盐和一种能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。写出该反应的离子方程式:
(3)连二亚硫酸钠(Na2S2O4)常作木浆造纸的漂白剂。向甲酸钠(HCOONa)与
 的混合溶液中通入SO2气体,可得到连二亚硫酸钠及一种可用作灭火剂的气体,相应的化学反应的离子方程式为
的混合溶液中通入SO2气体,可得到连二亚硫酸钠及一种可用作灭火剂的气体,相应的化学反应的离子方程式为 溶液反应可得到单质银,相应的离子方程式为
溶液反应可得到单质银,相应的离子方程式为(4)煤燃烧排放的烟气含有SO2和
 ,形成酸雨,污染大气,采用
,形成酸雨,污染大气,采用 溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有
溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有 和NO的烟气,写出
和NO的烟气,写出 溶液脱硝(主要转化为
溶液脱硝(主要转化为 )过程中主要反应的离子方程式:
)过程中主要反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】把一小块金属钠投入水中,观察到以下各种现象:钠浮在水面上,熔成闪亮的小球,四处游动,逐渐减少,直至消失.
(1)写出该反应的离子方程式_________________ ,其中钠熔成闪亮小球的原因是__________
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式_____________
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式_________ ;继续将沉淀过滤、洗涤、干燥、灼烧,此时得到的固体为_________ (填化学式)。
(1)写出该反应的离子方程式
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
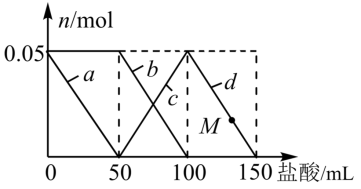
【推荐3】向100mL含Na2CO3、NaAlO2的混合溶液中逐滴加入HCl溶液,测得溶液中的某几种离子的物质的量的变化如图所示:
(1)已知 与
与 在溶液中反应而不能大量共存,写出两者反应的离子方程式:
在溶液中反应而不能大量共存,写出两者反应的离子方程式:___________ 。
(2)a和c曲线表示的离子分别是___________ 、___________ 。d曲线表示的离子方程式为___________ 。
(3)加入HCl溶液的物质的量浓度为___________ ,M点溶液中沉淀的质量为___________ 。
(4)原混合溶液中的Na+与 的物质的量之比为
的物质的量之比为___________ 。
(5)另取AlCl3溶液和NaOH溶液反应,当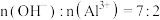 时,写出反应的离子方程式:
时,写出反应的离子方程式:___________ 。

(1)已知
 与
与 在溶液中反应而不能大量共存,写出两者反应的离子方程式:
在溶液中反应而不能大量共存,写出两者反应的离子方程式:(2)a和c曲线表示的离子分别是
(3)加入HCl溶液的物质的量浓度为
(4)原混合溶液中的Na+与
 的物质的量之比为
的物质的量之比为(5)另取AlCl3溶液和NaOH溶液反应,当
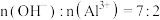 时,写出反应的离子方程式:
时,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3(不溶于水)、H2O、H2O2,已知该反应中H2O2只发生如下过程H2O2→O2.
(1)写出该反应的化学方程式:_____ 。
(2)该反应中氧化剂是_____ ,氧化产物是_____ 。
(3)产生1个O2,转移的电子的个数为_____ 个。
(4)用单线桥标出该反应中电子转移情况:_____ 。
(1)写出该反应的化学方程式:
(2)该反应中氧化剂是
(3)产生1个O2,转移的电子的个数为
(4)用单线桥标出该反应中电子转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳质量的90%以上。
(1)写出通信中硅的氧化物的一种用途:___________ 。
(2)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为 。
。
①该反应中Si元素的化合价为___________ 价。
②其中还原产物的化学式为___________ 。
③高温真空环境中,C与SiO2反应也可以生成SiC,同时生成一种有毒的气体,写出该反应的化学方程式:___________ 。
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3溶液可以用作___________ ;设计简单实验比较醋酸与H2SiO3酸性的强弱(用化学方程式回答:___________ 。
(1)写出通信中硅的氧化物的一种用途:
(2)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为
 。
。①该反应中Si元素的化合价为
②其中还原产物的化学式为
③高温真空环境中,C与SiO2反应也可以生成SiC,同时生成一种有毒的气体,写出该反应的化学方程式:
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3溶液可以用作
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下图为铁及其化合物的“价-类”二维图。
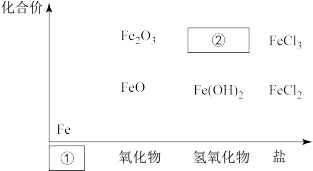
(1)填写二维图缺失的类别①___________ 和化学式②___________ 。
(2)某同学利用以下试剂研究 性质,进行了如下预测:
性质,进行了如下预测:
① ②Fe ③NaOH ④
②Fe ③NaOH ④ ⑤
⑤
从物质类别上看, 属于
属于___________ ,可能与___________ 发生反应(填序号)﹔
从化合价角度看, 具有
具有___________ 性,可能与___________ 发生反应(填序号)。
(3)某工厂用 溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
①用双线桥表示电子转移________ 。
②写出该反应的离子方程式___________
(4)工业废水中含有的重铬酸根离子( )有毒,必须处理达标后才能排放。工业上常用绿矾(
)有毒,必须处理达标后才能排放。工业上常用绿矾( )做处理剂,反应的离子方程式如下:
)做处理剂,反应的离子方程式如下: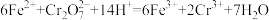 。并用单线桥法标出方程式中电子转移的方向和数目
。并用单线桥法标出方程式中电子转移的方向和数目___________ ;在该反应中,还原剂是___________ (填离子符号,下同),还原产物是___________ 。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂研究
 性质,进行了如下预测:
性质,进行了如下预测:①
 ②Fe ③NaOH ④
②Fe ③NaOH ④ ⑤
⑤
从物质类别上看,
 属于
属于从化合价角度看,
 具有
具有(3)某工厂用
 溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
①用双线桥表示电子转移
②写出该反应的离子方程式
(4)工业废水中含有的重铬酸根离子(
 )有毒,必须处理达标后才能排放。工业上常用绿矾(
)有毒,必须处理达标后才能排放。工业上常用绿矾( )做处理剂,反应的离子方程式如下:
)做处理剂,反应的离子方程式如下: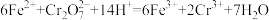 。并用单线桥法标出方程式中电子转移的方向和数目
。并用单线桥法标出方程式中电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I、现有下列物质:①铁②硫酸溶液③SO2④熔融的Na2O⑤ 固体⑥蔗糖⑦CuSO4·5H2O晶体⑧氧气⑨氨水⑩稀硝酸
固体⑥蔗糖⑦CuSO4·5H2O晶体⑧氧气⑨氨水⑩稀硝酸
(1)上述物质中属于电解质的有___________ (填编号,下同),属于非电解质的有___________ ,能导电的有___________ 。
(2)上述物质中有两种物质之间可发生离子反应: ,该离子反应对应的化学方程式
,该离子反应对应的化学方程式___________ 。
(3)上述物质中有两种物质配成的溶液混合后可得到两种不同颜色沉淀,该反应的离子方程式为___________ 。
Ⅱ.利用氧化还原反应原理可处理污水。
(4)高铁酸钠(Na2FeO4)是一种新型的净水剂,其中一种制备方法如下。用双线桥标出该反应电子转移的方向和数目。___________
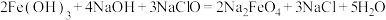
(5)电镀废水中含有剧毒的NaCN(C为+2价),加入NaClO溶液处理该碱性废水时生成Na2CO3、NaCl和N2.该反应的离子方程式为___________ 。
 固体⑥蔗糖⑦CuSO4·5H2O晶体⑧氧气⑨氨水⑩稀硝酸
固体⑥蔗糖⑦CuSO4·5H2O晶体⑧氧气⑨氨水⑩稀硝酸(1)上述物质中属于电解质的有
(2)上述物质中有两种物质之间可发生离子反应:
 ,该离子反应对应的化学方程式
,该离子反应对应的化学方程式(3)上述物质中有两种物质配成的溶液混合后可得到两种不同颜色沉淀,该反应的离子方程式为
Ⅱ.利用氧化还原反应原理可处理污水。
(4)高铁酸钠(Na2FeO4)是一种新型的净水剂,其中一种制备方法如下。用双线桥标出该反应电子转移的方向和数目。
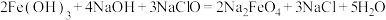
(5)电镀废水中含有剧毒的NaCN(C为+2价),加入NaClO溶液处理该碱性废水时生成Na2CO3、NaCl和N2.该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)按要求写出方程式:
①HClO3(电离方程式):____ 。
②Fe2(SO4)3(电离方程式):____ 。
③硫酸氢钠和氯化钡溶液反应(离子方程式):____ 。
④二氧化碳通入足量氢氧化钡溶液(离子方程式):____ 。
(2)以下为中学化学中常见的几种物质:①二氧化碳②熔融KCl③NaHSO4固体④铜⑤稀硫酸⑥澄清石灰水,其中属于导电的电解质的有____ (填序号,下同),属于非电解质的有____ 。
(3)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O。
①该反应中还原剂是____ (用化学式表示,下同),____ 元素被还原,氧化产物与还原产物质量比为____ 。
②用单线桥在方程式中标出电子转移的情况:____ 。
(1)按要求写出方程式:
①HClO3(电离方程式):
②Fe2(SO4)3(电离方程式):
③硫酸氢钠和氯化钡溶液反应(离子方程式):
④二氧化碳通入足量氢氧化钡溶液(离子方程式):
(2)以下为中学化学中常见的几种物质:①二氧化碳②熔融KCl③NaHSO4固体④铜⑤稀硫酸⑥澄清石灰水,其中属于导电的电解质的有
(3)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O。
①该反应中还原剂是
②用单线桥在方程式中标出电子转移的情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.某反应为:4CuI+Hg=Cu2HgI4+2Cu(反应前后的I均为-1价),试回答:
(1)上述反应产物Cu2HgI4中,Hg元素显_________ 价;
(2)CuI发生__________ 反应(填氧化或还原)。
Ⅱ.某反应为:3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O,用单线桥表示出该反应中电子转移的方向和数目。
_____________________________________________________________
Ⅲ.有下列三个反应:
a.2FeCl3+2KI=2FeCl2+2KCl+I2
b.2FeCl2+Cl2=2FeCl3
c.2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)上述三个反应中氧化剂氧化性强弱关系为____________ ;
(2)在反应c中,若被氧化的HCl为1.5mol,则转移的电子数是___________ 个。
(1)上述反应产物Cu2HgI4中,Hg元素显
(2)CuI发生
Ⅱ.某反应为:3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O,用单线桥表示出该反应中电子转移的方向和数目。
Ⅲ.有下列三个反应:
a.2FeCl3+2KI=2FeCl2+2KCl+I2
b.2FeCl2+Cl2=2FeCl3
c.2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)上述三个反应中氧化剂氧化性强弱关系为
(2)在反应c中,若被氧化的HCl为1.5mol,则转移的电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某课题组研究以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺,其设计的流程如下:

回答下列问题:
(1)已知在焙烧硫铁矿石过程中铁元素转化成了Fe3O4,则该反应的化学方程式是___ ;
(2)“酸溶”中反应的离子方程式是___ ;
(3)“过滤”后滤液中金属阳离子有___ ;
(4)“氧化”中使用的氧化剂最好是___ ;

回答下列问题:
(1)已知在焙烧硫铁矿石过程中铁元素转化成了Fe3O4,则该反应的化学方程式是
(2)“酸溶”中反应的离子方程式是
(3)“过滤”后滤液中金属阳离子有
(4)“氧化”中使用的氧化剂最好是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为“一些物质与水”的分类图,利用化合价和物质类别预测物质的性质是化学研究的重要手段。

已知:3NO2 + H2O = 2HNO3 + NO
(1)从化学反应类型的角度可以将物质分类。将上述物质分为A、B两组的依据是_______ ,C组物质与水反应时水既不是氧化剂又不是还原剂,则D组物质为__________ 。
(2)从化合价的角度可以预测Na2O2的性质。
①Na2O2的性质_____ (填序号)。
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
②Na2O2以氧化性为主,Na2O2加入含有 的溶液中反应结束后,硫元素存在形式合理的是
的溶液中反应结束后,硫元素存在形式合理的是____ (填序号)。
a.S2- b.S C. d.
d.
(3)从物质分类的角度可以推测物质的性质。化工生产中常常用到"三酸两碱”、“三酸“指硝酸、硫酸和盐酸,“两碱“指烧碱和纯碱。
①从物质分类角度看,不恰当的一种物质是________________ (填化学式)。
②“三酸”中一种酸的浓溶液与“84消毒液”混合会生成一种黄绿色气体,该反应的离子方程式为_________ (并用单线桥标出电子转移情况)。

已知:3NO2 + H2O = 2HNO3 + NO
(1)从化学反应类型的角度可以将物质分类。将上述物质分为A、B两组的依据是
(2)从化合价的角度可以预测Na2O2的性质。
①Na2O2的性质
a.只有氧化性 b.只有还原性 c.既有氧化性又有还原性
②Na2O2以氧化性为主,Na2O2加入含有
 的溶液中反应结束后,硫元素存在形式合理的是
的溶液中反应结束后,硫元素存在形式合理的是a.S2- b.S C.
 d.
d.
(3)从物质分类的角度可以推测物质的性质。化工生产中常常用到"三酸两碱”、“三酸“指硝酸、硫酸和盐酸,“两碱“指烧碱和纯碱。
①从物质分类角度看,不恰当的一种物质是
②“三酸”中一种酸的浓溶液与“84消毒液”混合会生成一种黄绿色气体,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是 _____________________________ ,又变为棕黄色的原因是用离子方程式解释 _____________________________ 。
您最近一年使用:0次



