高碘酸钾(KIO4)溶于热水,微溶于冷水和氢氧化钾溶液,可用作有机物的氧化剂。制备高碘酸钾的装置图如图I(夹持和加热装置省略)。回答下列问题:
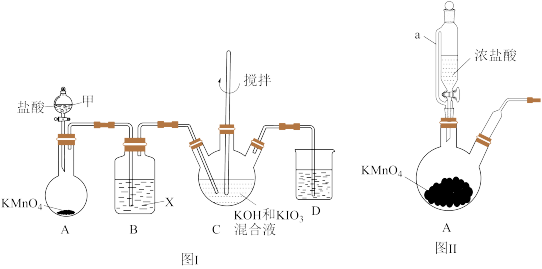
(1)装置A中仪器甲的名称是________ ,有同学提出将装置A改进为图II,这样改进的优点是________________ 。
(2)装置B的作用是______________ 。
(3)装置D中的试剂是____________ 。
(4)连接好后,将装置C水浴加热,通入氯气一段时间,冷却析出高碘酸钾晶体,装置C中反应的化学方程式为___________________
(5)反应后装置C中混合物经_______ (填操作名称),洗涤,干燥等步骤得到产品。洗涤时,应选用_______ (填“热水”或“冷水”)。
(6)在酸性条件下,向硫酸锰(MnSO4)溶液中滴加高碘酸钾(KIO4)溶液,溶液颜色会变为紫红色,生成高锰酸钾(KMnO4),则KIO4和KMnO4二者相比,______ 的氧化性强

(1)装置A中仪器甲的名称是
(2)装置B的作用是
(3)装置D中的试剂是
(4)连接好后,将装置C水浴加热,通入氯气一段时间,冷却析出高碘酸钾晶体,装置C中反应的化学方程式为
(5)反应后装置C中混合物经
(6)在酸性条件下,向硫酸锰(MnSO4)溶液中滴加高碘酸钾(KIO4)溶液,溶液颜色会变为紫红色,生成高锰酸钾(KMnO4),则KIO4和KMnO4二者相比,
更新时间:2020-11-25 15:43:00
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某小组同学欲探究H2O2的性质,经历如下探究过程:
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,又具有还原性。
(1)预测其具有氧化性的依据是______________ 。
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。

(2)实验①利用了酸性高锰酸钾的________ 性质,该实验中,证明KMnO4溶液与H2O2反应的现象除了溶液颜色变浅或褪色外,还有_____________ 。
(3)实验②是为了验证H2O2的________ 性质,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝。
解释和结论:
(4)以上实验可得出的结论是_________________ 。
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,又具有还原性。
(1)预测其具有氧化性的依据是
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。

(2)实验①利用了酸性高锰酸钾的
(3)实验②是为了验证H2O2的
解释和结论:
(4)以上实验可得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某化学小组按下图所示实验流程比较浓硝酸和稀硝酸的氧化性强弱,其中B为一种紫红色金属,C为红棕色气体。
(1)A与B反应的化学方程式是_________________________ ;A与B反应迅速,实验中需要采取措施控制气体放出的快慢及多少,则装置I可以选择的装置为_________________________ 。 气体,该操作的目的是
气体,该操作的目的是___________ 。
(3)装置Ⅱ中发生反应的化学方程式是_______________ 。
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸______________ (填“强”或“弱”),判断的依据是___________________ 。

(1)A与B反应的化学方程式是

 气体,该操作的目的是
气体,该操作的目的是(3)装置Ⅱ中发生反应的化学方程式是
(4)通过实验可得出:浓硝酸的氧化性比稀硝酸
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】瑞典化学家舍勒是最早发现氯气的人,他在研究软锰矿矿石(主要成分是二氧化锰)时,把浓盐酸和软锰矿矿石混合加热,意外地得到了氯气。至今,实验室中还用这种方法制取氯气,装置如图所示,化学反应方程式为: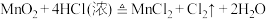
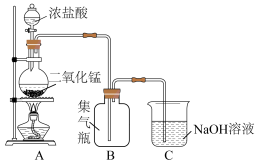
回答下列问题:
(1)实验室制取 的反应中,浓盐酸表现
的反应中,浓盐酸表现_________ (填“氧化性”、“还原性”或“酸性”)。
(2)请用单线桥表示该反应中电子转移的方向和数目_________ 。
(3)标况下,若生成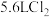 ,则转移电子的数目为
,则转移电子的数目为_________ 。
(4)装置C可吸收多余的 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式_________ 。所用 溶液一般为
溶液一般为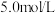 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、_________ 。
(5) 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是_________ 。
(6)装置C中也可能生成 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式_________ 。
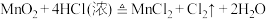

回答下列问题:
(1)实验室制取
 的反应中,浓盐酸表现
的反应中,浓盐酸表现(2)请用单线桥表示该反应中电子转移的方向和数目
(3)标况下,若生成
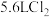 ,则转移电子的数目为
,则转移电子的数目为(4)装置C可吸收多余的
 ,生成
,生成 和
和 ,写出离子方程式
,写出离子方程式 溶液一般为
溶液一般为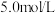 ,用
,用 固体配制
固体配制 该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、
该溶液,需要用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、(5)
 有强氧化性,某实验小组为探究
有强氧化性,某实验小组为探究 、
、 、
、 在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下
在酸性条件下的氧化性强弱,设计实验如下:实验①:在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;实验②:向实验①的溶液中加入少量亚硫酸钠溶液,蓝色又褪去。以上实验说明,在酸性条件下 、
、 、
、 的氧化性由弱到强的顺序是
的氧化性由弱到强的顺序是(6)装置C中也可能生成
 ,
, 和浓盐酸也可以制备
和浓盐酸也可以制备 ,试写出离子方程式
,试写出离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】科学、安全、有效和合理地开发自然资源,对生产、生活有重要价值。
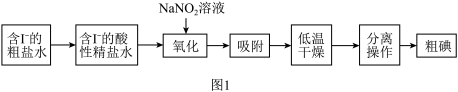
Ⅰ.活性炭纤维吸附法是工业提取碘单质的方法之一,其流程如图1所示:
已知:a. 溶液只能将
溶液只能将 氧化成
氧化成 ,同时生成NO气体。
,同时生成NO气体。
b.酸性条件下, 会与
会与 反应生成
反应生成 和
和 。
。
(1)粗盐水中还含有 、
、 、
、 ,制成精盐水时所加试剂的顺序是___________(填标号)。
,制成精盐水时所加试剂的顺序是___________(填标号)。
(2)“氧化”过程中发生反应的离子方程式是___________ 。
(3)酸性 溶液是常用的氧化剂,但此过程中选择价格更贵的
溶液是常用的氧化剂,但此过程中选择价格更贵的 的原因是
的原因是___________ 。
(4)根据碘单质的特性,分离操作是___________ ,冷凝得粗碘。
Ⅱ.以金红石(主要成分为TiO₂)为原料制取海绵钛的工艺流程如图2所示:
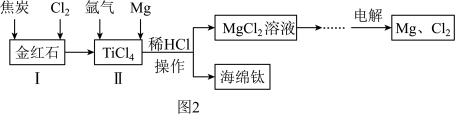
(5)高温条件下,反应1可生成一种可燃性气体,反应1的化学方程式是___________ 。
(6)上述流程中可循环利用的物质是___________ (填化学式),电解熔融 的化学方程式是
的化学方程式是___________ 。
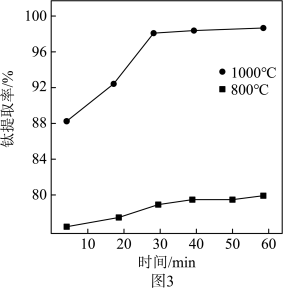
(7)反应2中钛的提取率在不同温度下随时间变化的曲线如图3,则反应最适宜的条件是___________ 。
Ⅰ.活性炭纤维吸附法是工业提取碘单质的方法之一,其流程如图1所示:

已知:a.
 溶液只能将
溶液只能将 氧化成
氧化成 ,同时生成NO气体。
,同时生成NO气体。b.酸性条件下,
 会与
会与 反应生成
反应生成 和
和 。
。(1)粗盐水中还含有
 、
、 、
、 ,制成精盐水时所加试剂的顺序是___________(填标号)。
,制成精盐水时所加试剂的顺序是___________(填标号)。A. 溶液、NaOH溶液、 溶液、NaOH溶液、 溶液、稀盐酸 溶液、稀盐酸 |
B.NaOH溶液、 溶液、 溶液、 溶液、稀盐酸 溶液、稀盐酸 |
C.NaOH溶液、 溶液、 溶液、 溶液、稀盐酸 溶液、稀盐酸 |
D. 溶液、 溶液、 溶液、NaOH溶液、稀盐酸 溶液、NaOH溶液、稀盐酸 |
(3)酸性
 溶液是常用的氧化剂,但此过程中选择价格更贵的
溶液是常用的氧化剂,但此过程中选择价格更贵的 的原因是
的原因是(4)根据碘单质的特性,分离操作是
Ⅱ.以金红石(主要成分为TiO₂)为原料制取海绵钛的工艺流程如图2所示:

(5)高温条件下,反应1可生成一种可燃性气体,反应1的化学方程式是
(6)上述流程中可循环利用的物质是
 的化学方程式是
的化学方程式是(7)反应2中钛的提取率在不同温度下随时间变化的曲线如图3,则反应最适宜的条件是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某实验小组对中学课本中可生成氢气的反应进行了研究,总结出三个可以生成H2的反应:①Zn+盐酸;②Na+水;③Al+NaOH溶液。为点燃上述三个反应生成的H2,他们设计了如右图所示的装置图:请回答下列问题:

(1)写出Al和NaOH溶液反应的离子方程式_______________________________ 。
(2)在点燃H2之前必须先进行____________________________________________ 。
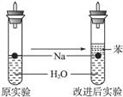
(3)实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量又太少。于是他们准备增加钠的用量,可教师说太危险,你认为产生危险的原因是___________________________ 。
(4)实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00 g·mL-1,并据此对实验进行了改进。在改进后的实验中H2的生成速率____________ 。(填“减慢”或“加快”)
(5)将4.6gNa和8.1gAl投入到足量的水中,所得溶液的体积为200mL,则生成标准状况下的H2的体积是___________ ?该溶液中溶质的物质的量浓度是__________________ ?

(1)写出Al和NaOH溶液反应的离子方程式
(2)在点燃H2之前必须先进行

(3)实验小组在点燃用上述装置制得的H2时,①③实验获得成功,②却失败了。他们分析认为失败的原因是Na与H2O的反应速率太快,Na的用量又太少。于是他们准备增加钠的用量,可教师说太危险,你认为产生危险的原因是
(4)实验小组查阅钠、苯(一种不溶于水的液态有机物)、水的密度分别为0.97 g·mL-1、0.88 g·mL-1、1.00 g·mL-1,并据此对实验进行了改进。在改进后的实验中H2的生成速率
(5)将4.6gNa和8.1gAl投入到足量的水中,所得溶液的体积为200mL,则生成标准状况下的H2的体积是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性,其中含氯消毒剂在生产生活中有着广泛的用途。
Ⅰ.某化学兴趣小组用如图装置制备家用消毒液。

(1)写出装置B中反应的离子方程式___________ 。
(2)装置A中的溶液是___________ ,长玻璃导管的作用是___________ 。图中装置的连接顺序是B、___________ 。
(3)用化学方程式表示装置D中“84”消毒液的生成过程:___________ 。
(4)居家消毒时,不能将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,原因是___________ 。
(5)某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和 的混合溶液,经测定
的混合溶液,经测定 与
与 的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为
的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为___________ 。
Ⅱ.世界卫生组织将定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。
(6)消毒效率是用单位质量的消毒剂得电子数来表示的, 作消毒剂时和
作消毒剂时和 一样,还原产物均为
一样,还原产物均为 。
。 的消毒效率是
的消毒效率是 的
的___________ 倍(保留两位小数)。
Ⅰ.某化学兴趣小组用如图装置制备家用消毒液。

(1)写出装置B中反应的离子方程式
(2)装置A中的溶液是
(3)用化学方程式表示装置D中“84”消毒液的生成过程:
(4)居家消毒时,不能将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,原因是
(5)某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和
 的混合溶液,经测定
的混合溶液,经测定 与
与 的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为
的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为Ⅱ.世界卫生组织将定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。
(6)消毒效率是用单位质量的消毒剂得电子数来表示的,
 作消毒剂时和
作消毒剂时和 一样,还原产物均为
一样,还原产物均为 。
。 的消毒效率是
的消毒效率是 的
的
您最近一年使用:0次
【推荐1】实验小组为验证 与水反应的产物,用下图所示装置进行实验(夹持装置已略去,气密性已检验)。
与水反应的产物,用下图所示装置进行实验(夹持装置已略去,气密性已检验)。
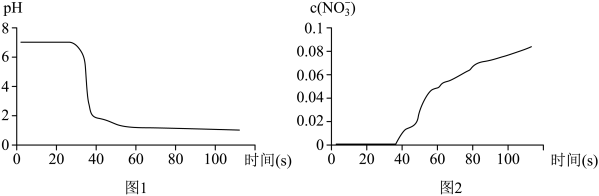
步㵵Ⅱ中,传感器记录数据如下图所示:
(1)步骤I中,通入 的目的是
的目的是_______ 。
(2)将步骤Ⅱ中圆底烧瓶内的实验现象补充完整:_______ 。
(3)该实验验证 与水反应产物的实验证据不包括_______(填序号)。
与水反应产物的实验证据不包括_______(填序号)。
 与水反应的产物,用下图所示装置进行实验(夹持装置已略去,气密性已检验)。
与水反应的产物,用下图所示装置进行实验(夹持装置已略去,气密性已检验)。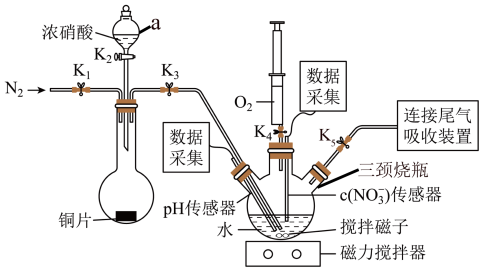
| 实验步骤 | 实验现象 |
Ⅰ.打开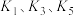 ,关闭 ,关闭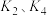 ,通入一段时间 ,通入一段时间 ,关闭 ,关闭 | —— |
Ⅱ.打开 ,放入足量浓 ,放入足量浓 ,同时打开 ,同时打开 传感器和 传感器和 传感器,记录数据 传感器,记录数据 | 圆底烧瓶中反应剧烈,铜片逐渐溶解,溶液变为蓝绿色,_______;片刻后,三颈瓶内的导管口有气泡冒出 |
Ⅲ. 后,打开 后,打开 ,用注射器将少量空气注入三颈瓶,关闭 ,用注射器将少量空气注入三颈瓶,关闭 | 三颈瓶内的气体从无色变为浅红棕色 |
(1)步骤I中,通入
 的目的是
的目的是(2)将步骤Ⅱ中圆底烧瓶内的实验现象补充完整:
(3)该实验验证
 与水反应产物的实验证据不包括_______(填序号)。
与水反应产物的实验证据不包括_______(填序号)。| A.圆底烧瓶中溶液变为蓝绿色 | B.三颈瓶内的气体从无色变为浅红棕色 |
C. 传感器记录所得数据 传感器记录所得数据 | D. 传感器记录所得数据 传感器记录所得数据 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】为了验证Cu和 浓H2SO4反应的产物中有SO2和H2O,选用下图所示仪器(内含物质)组装成实验装置 。 B中有无水硫酸铜、C中有品红、D中有氢氧化钠溶液
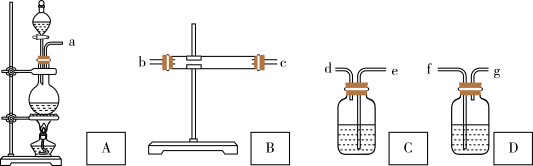
(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):a接______ ,______ 接______ ,______ 接______ ;
(2) 仪器B、C应有怎样的实验现象才表明已检验出SO2和H2O?B中______ ,C中______ ;
(3)D中氢氧化钠溶液的作用是______
(4)写出A中反应的化学方程式______ 。

(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):a接
(2) 仪器B、C应有怎样的实验现象才表明已检验出SO2和H2O?B中
(3)D中氢氧化钠溶液的作用是
(4)写出A中反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某学习小组探究氨的还原性及检验产物的性质,按下图装置进行实验(图中夹持装置已略去),并做喷泉实验。将B处的三氧化二铬加热至红热,再鼓入空气,已知:无水氯化钙可吸收氨气和水。回答下列问题:

(1)B中发生反应的化学方程式是___________ 。
(2)证明氨气发生了催化氧化的现象是___________ 。
(3)写出(2)中反应的化学方程式___________ 。
(4)装置E作用是___________ 。
(5)引发装置F的喷泉实验的操作是___________ 。
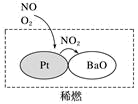
(6)大量行驶的机动车是污染源之一、汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式___________ 。

(1)B中发生反应的化学方程式是
(2)证明氨气发生了催化氧化的现象是
(3)写出(2)中反应的化学方程式
(4)装置E作用是
(5)引发装置F的喷泉实验的操作是
(6)大量行驶的机动车是污染源之一、汽车发动机废气稀燃控制系统主要工作原理如图所示;写出稀燃过程中NO发生的主要反应的方程式

您最近一年使用:0次



