目前国际空间站常采用还原法处理CO2,反应为CO2(g)+4H2(g) CH4(g)+2H2O(g)。在恒温恒压的密闭容器中进行的该反应,下列不能判断其达到平衡状态的是
CH4(g)+2H2O(g)。在恒温恒压的密闭容器中进行的该反应,下列不能判断其达到平衡状态的是
 CH4(g)+2H2O(g)。在恒温恒压的密闭容器中进行的该反应,下列不能判断其达到平衡状态的是
CH4(g)+2H2O(g)。在恒温恒压的密闭容器中进行的该反应,下列不能判断其达到平衡状态的是| A.混合气体密度不再变化 | B.2v(CO2)正=v(H2O)逆 |
C.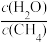 不再变化 不再变化 | D.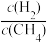 不再变化 不再变化 |
更新时间:2020-12-02 10:06:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在一定温度下,在密闭容器中投入 X(g) 和 Y(g) ,发生反应生成 Z(g) 。测得各物质浓度与时间关系如图所示(提示:净反应速率等于正、逆反应速率之差)。下列说法错误的是
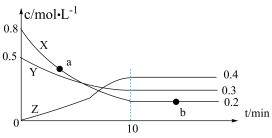

| A.上述可逆反应中 X、Y、Z 的化学计量数之比为3 :1: 2 |
| B.该条件下,Y 的最大限度(平衡转化率)为 60% |
| C.a 点:正反应速率大于逆反应速率 |
| D.b 点:净反应速率等于零 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将a mol N2和3a mol H2充入绝热的固定容积密闭容器中,发生合成氨反应N2(g)+3H2(g)⇌2NH3(g)。下列选项中说明反应已经达到平衡状态的是
①体系的温度不再改变;②体系的压强不再改变;③混合气体密度不再改变;④混合气体的平均摩尔质量不再改变;⑤N2和H2的浓度之比达到1:3;⑥v(N2)正=3v(H2)逆;⑦2v(H2)正=3v(NH3)逆;⑧每有1mol N≡N键断裂就有6 mol N-H键形成
①体系的温度不再改变;②体系的压强不再改变;③混合气体密度不再改变;④混合气体的平均摩尔质量不再改变;⑤N2和H2的浓度之比达到1:3;⑥v(N2)正=3v(H2)逆;⑦2v(H2)正=3v(NH3)逆;⑧每有1mol N≡N键断裂就有6 mol N-H键形成
| A.②④⑤⑥ | B.②④⑥⑧ | C.①②④⑥ | D.①②④⑦ |
您最近一年使用:0次
【推荐3】下列实验操作、现象与结论相匹配的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 铝箔插入稀硝酸中 | 无明显现象 | 铝箔表面形成了致密的氧化膜 |
| B | 碳和浓硫酸加热所得气体产物依次通过品红溶液和澄清石灰水 | 品红溶液褪色,澄清石灰水变浑浊 | 气体产物中含有CO2和SO2 |
| C | 向5mL0.1mol/LKI溶液中滴入0.1mol/LFeCl3溶液5~6滴,加2mLCCl4振荡,静置后取上层清液滴加KSCN溶液 | 溶液变红 |  与 与 的反应有一定限度 的反应有一定限度 |
| D | 足量的铜和浓硝酸反应,反应停止后,往溶液中加入稀硫酸 | 溶液褪色 | 铜和稀硫酸发生反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】向容积为1.00L的恒容密闭容器中通入一定量 和
和 的混合气体,发生反应:
的混合气体,发生反应: (g,无色)
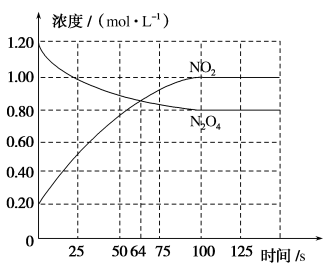
(g,无色)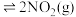 。体系中各物质浓度随时间的变化如图所示。下列说法正确的是
。体系中各物质浓度随时间的变化如图所示。下列说法正确的是
 和
和 的混合气体,发生反应:
的混合气体,发生反应: (g,无色)
(g,无色)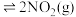 。体系中各物质浓度随时间的变化如图所示。下列说法正确的是
。体系中各物质浓度随时间的变化如图所示。下列说法正确的是
| A.64s时,反应达到化学平衡状态 |
| B.从反应开始至化学平衡,混合气体的颜色逐渐变浅 |
| C.0~100s内,该反应的正反应速率小于逆反应速率 |
D.0~100s内,用 浓度的变化表示该反应的平均速率为0.008 浓度的变化表示该反应的平均速率为0.008 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】可逆反应:2NO2 2NO+O2在恒温恒容密闭容器中反应,下列条件可判断该反应已经达到平衡状态的是( )
2NO+O2在恒温恒容密闭容器中反应,下列条件可判断该反应已经达到平衡状态的是( )
(1)单位时间内生成nmolO2的同时生成2nmolNO2
(2)单位时间内生成nmolO2的同时,生成2nmolNO
(3)用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的密度不再改变的状态
(6)混合气体的平均相对分子质量不再改变的状态
 2NO+O2在恒温恒容密闭容器中反应,下列条件可判断该反应已经达到平衡状态的是( )
2NO+O2在恒温恒容密闭容器中反应,下列条件可判断该反应已经达到平衡状态的是( )(1)单位时间内生成nmolO2的同时生成2nmolNO2
(2)单位时间内生成nmolO2的同时,生成2nmolNO
(3)用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的密度不再改变的状态
(6)混合气体的平均相对分子质量不再改变的状态
| A.(1)(4)(6) | B.(2)(3)(5) |
| C.(1)(3)(4) | D.(1)(2)(3)(4)(5)(6) |
您最近一年使用:0次



