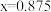已知:5C2O + 2MnO
+ 2MnO + 16H+=2Mn2+ +10CO2↑+ 8H2O)。某研究小组通过如下实验步骤测定晶体A (KxFey(C2O4)z·aH2O,其中的Fe元素为+3价)的化学式:
+ 16H+=2Mn2+ +10CO2↑+ 8H2O)。某研究小组通过如下实验步骤测定晶体A (KxFey(C2O4)z·aH2O,其中的Fe元素为+3价)的化学式:
步骤1:准确称取A样品9.82g,分为两等份;
步骤2:取其中一份,干燥脱水至恒重,残留物质量为4.37 g;
步骤3:取另一份置于锥形瓶中,加入足量的3.0mol·L-1 H2SO4溶液和适量蒸馏水,使用0.5 mol·L-1KMnO4溶液与其反应,反应结束时消耗KMnO4溶液的体积为24.0 mL;
步骤4:将步骤2所得固体溶于水,加入铁粉0.28g,恰好完全反应。
下列说法正确的是
 + 2MnO
+ 2MnO + 16H+=2Mn2+ +10CO2↑+ 8H2O)。某研究小组通过如下实验步骤测定晶体A (KxFey(C2O4)z·aH2O,其中的Fe元素为+3价)的化学式:
+ 16H+=2Mn2+ +10CO2↑+ 8H2O)。某研究小组通过如下实验步骤测定晶体A (KxFey(C2O4)z·aH2O,其中的Fe元素为+3价)的化学式:步骤1:准确称取A样品9.82g,分为两等份;
步骤2:取其中一份,干燥脱水至恒重,残留物质量为4.37 g;
步骤3:取另一份置于锥形瓶中,加入足量的3.0mol·L-1 H2SO4溶液和适量蒸馏水,使用0.5 mol·L-1KMnO4溶液与其反应,反应结束时消耗KMnO4溶液的体积为24.0 mL;
步骤4:将步骤2所得固体溶于水,加入铁粉0.28g,恰好完全反应。
下列说法正确的是
| A.据步骤2可以算出水的物质的量,得出a=0.03 |
B.据步骤3算得晶体A样品中含草酸根离子(C2O )的物质的量为0.03 mol )的物质的量为0.03 mol |
| C.据上述4步算得晶体A的化学式为K3Fe(C2O4)3·3H2O |
| D.将步骤4所得溶液中Fe2+全部氧化为Fe3+需要通入168 mL Cl2 |
20-21高一上·浙江·期中 查看更多[6]
(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)【浙江新东方】70.(已下线)【浙江新东方】【2020】【高一上】【期中】【HD-LP408】【化学】
更新时间:2020-12-10 13:56:46
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】工业上将Na2CO3和Na2S配成溶液,再通入SO2可制取Na2S2O3,同时放出CO2。已知:
S (s)+Na2SO3(aq)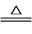 Na2S2O3(aq)。下列说法不正确的是
Na2S2O3(aq)。下列说法不正确的是
S (s)+Na2SO3(aq)
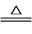 Na2S2O3(aq)。下列说法不正确的是
Na2S2O3(aq)。下列说法不正确的是| A.上述反应中氧化剂和还原剂的物质的量比是2:l |
| B.上述反应中的Na2CO3和Na2S的物质的量比最佳是1:2 |
| C.每生成lmol Na2S2O3转移4mol电子 |
| D.通入的SO2过量很多,将会产生浑浊现象 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】 g铜与足量浓H2SO4共热时完全反应,在标准状况下生成
g铜与足量浓H2SO4共热时完全反应,在标准状况下生成 L气体,则被还原的H2SO4的量是( )
L气体,则被还原的H2SO4的量是( )
 g铜与足量浓H2SO4共热时完全反应,在标准状况下生成
g铜与足量浓H2SO4共热时完全反应,在标准状况下生成 L气体,则被还原的H2SO4的量是( )
L气体,则被还原的H2SO4的量是( )A.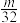 mol mol | B. mol mol | C.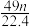 g g | D. g g |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某溶液可能含有 NH4+、K+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,现取 100mL 溶液先加入足量氯水,然后滴加足量 BaCl2 溶液,得到沉淀 4.66g,在滤液中加足量 NaOH 溶液并加热,生成的气体在标准状况下体积为 1.12L。根据上述实验,以下推测正确的是
| A.原溶液一定存在 NH4+、I- |
| B.原溶液一定不含 Ba2+、Fe3+、I- |
| C.原溶液可能存在 K+、Fe3+、SO42- |
| D.另取试液滴加足量盐酸、BaCl2溶液,即可确定溶液所有的离子组成 |
您最近一年使用:0次
单选题
|
较难
(0.4)
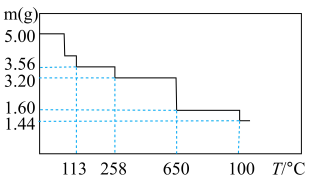
【推荐2】球墨铸铁中含有一种铁碳化合物X。实验小组为测定化合物X的组成设计实验如下:
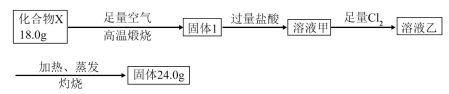
下列说法不正确的是

下列说法不正确的是
| A.X的化学式可以表示为Fe3C2 |
| B.24.0g固体的成分为是氧化铁 |
| C.将溶液甲加热、蒸发、灼烧也可得到24.0g固体 |
| D.X与足量的热浓硝酸反应有NO2和CO2生成 |
您最近一年使用:0次

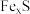 ,
, 为
为 )与100mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成2.4g硫单质、0.425mol
)与100mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成2.4g硫单质、0.425mol  和一定量
和一定量 气体,且溶液中无
气体,且溶液中无 (已知
(已知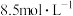
 与
与