g铜与足量浓H2SO4共热时完全反应,在标准状况下生成
g铜与足量浓H2SO4共热时完全反应,在标准状况下生成 L气体,则被还原的H2SO4的量是( )
L气体,则被还原的H2SO4的量是( )A.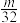 mol mol | B. mol mol | C.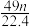 g g | D. g g |
更新时间:2019-04-22 09:46:00
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
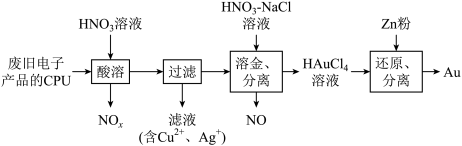
【推荐1】废旧电子产品的CPU元件可以回收利用,其中的Au、Ag和Cu回收的部分流程如下:
已知: 。下列说法正确的是
。下列说法正确的是

已知:
 。下列说法正确的是
。下列说法正确的是A.“酸溶”时使用浓硝酸, 的利用率更高 的利用率更高 |
B.滤液中的 和 和 可通过向滤液中加入过量浓氨水充分反应、过滤来分离 可通过向滤液中加入过量浓氨水充分反应、过滤来分离 |
C.“溶金”过程发生反应的离子方程式为 |
D.用过量Zn粉将 完全还原,理论上需消耗120gZn 完全还原,理论上需消耗120gZn |
您最近一年使用:0次
【推荐2】有一种铁的“氧化物”样品,用2.5mol/L盐酸280mL恰好完全溶解,所得溶液还能吸收标况下的0.56L氯气,如使其中的Fe2+全部转化为Fe3+,该样品可能的化学式是
| A.Fe2O3 | B. Fe3O4 | C. Fe4O5 | D. Fe5O7 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O;3Cl2+6NaOH=5NaCl+NaClO3+3H2O。某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液。经测定ClO-与ClO3-的物质的量之比为4:1,则溶液中NaCl与NaClO的物质的量之比为
| A.9:4 | B.11:2 | C.5:1 | D.l:l |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】将41.2g由Al、Fe、Cu组成的合金等分为两份,将其中一份合金溶于足量的NaOH溶液中,产生气体6.72L(标准状况);另一份合金溶于过量的稀硝酸中,得到VL(标准状况下)NO气体,向反应后的溶液中加入过量的NaOH溶液,过滤得到滤液X和25.4g的沉淀Y(HNO3的还原产物仅为NO),则下列说法正确的是
| A.41.2g的合金中含铁5.6g | B.滤液X中的溶质只有硝酸钠 |
| C.V为8.96 | D.沉淀Y中含氢氧化铜9.8g |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将浓硫酸滴到纸上 | 纸张变黑 | 浓硫酸具有吸水性 |
| B | 测定等浓度的Na2CO3和Na2SO3的溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 向2.0ml浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1AgNO3溶液,振荡 | 沉淀呈黄色 | Ksp(AgCl)>Ksp(AgI) |
| D | 将镁条点燃后迅速伸入集满CO2的集气瓶 | 集气瓶中有浓烟和黑色颗粒 | CO2具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某小组设计实验探究铜和浓硫酸反应产物的装置如图所示:
已知:浓硫酸的沸点约为338℃;实验中可能有 、
、 生成,都是难溶于水、难溶于稀硫酸的黑色固体。
生成,都是难溶于水、难溶于稀硫酸的黑色固体。
下列关于实验操作或实验结论的叙述正确的是
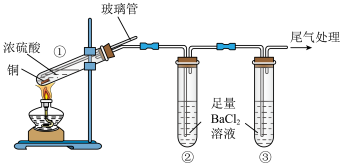
试管 | ① | ② | ③ |
实验现象 | 铜完全溶解后,溶液仍为无色,有白雾、灰白掺杂的黑色固体产生 | 有大量白色沉淀产生 | 有少量白色沉淀产生 |
 、
、 生成,都是难溶于水、难溶于稀硫酸的黑色固体。
生成,都是难溶于水、难溶于稀硫酸的黑色固体。下列关于实验操作或实验结论的叙述正确的是
| A.为防止实验时压强过大,可将玻璃管拉出液面以上 |
| B.为了检验试管①中的固体成分,实验结束后,取下试管①并向其中加入适量的水 |
C.试管②和③中白色沉淀的主要成分都是 |
| D.用浓氨水吸收尾气防污染 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】根据下列实验操作和现象,得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 表面变黑的银器浸泡到盛有食盐水的铝制容器中,银器与铝接触,一段时间后,银器变得光亮如新 | 构成原电池,硫化银得电子被还原成单质银 |
B | 足量的锌与一定量的浓硫酸加热放出气体 | 气体成分一定只有 |
C | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,试管里出现凝胶 | 非金属性:Cl>Si |
D | 将铁与水蒸气反应所得的固体用过量盐酸溶解,然后再加入少量 溶液,生成蓝色沉淀 溶液,生成蓝色沉淀 | 铁与水蒸气反应所得的固体中一定有铁粉剩余 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列说法正确的是
A.方程式2C+SiO2  2CO+Si表明非金属性:碳>硅 2CO+Si表明非金属性:碳>硅 |
| B.一定量的氯气与过量的铁粉在密闭容器中充分反应,有FeCl2生成 |
| C.将少量的浓硝酸滴入盛有过量的铜粉的试管中,气体产物只有NO2 |
| D.向新制备的饱和氯水中加入碳酸钙粉末可以增强氯水的漂白性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
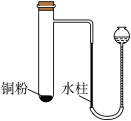
【推荐2】利用如图装置探究铜粉与下列试剂的反应,在试管中加入一定量铜粉,加入试剂后,立即塞上橡胶塞,实验现象如下表所示,下列推断不正确 的是
资料:Cu2++4NH3 [Cu(NH3)4]2+, [Cu(NH3)4]2+呈绛蓝色。
[Cu(NH3)4]2+, [Cu(NH3)4]2+呈绛蓝色。
资料:Cu2++4NH3
 [Cu(NH3)4]2+, [Cu(NH3)4]2+呈绛蓝色。
[Cu(NH3)4]2+, [Cu(NH3)4]2+呈绛蓝色。装置 | 序号 | 试剂 | 现象 |
| ① | 10 mL浓NH3·H2O,3 mLH2O | 溶液变为绛蓝色,左侧水柱上升 |
| ② | 10 mL浓NH3·H2O,3 mL H2O2 | 溶液变为绛蓝色,且比①深 | |
| ③ | 10 mL 20% HNO3溶液,3 mL H2O | 溶液快速变蓝,产生无色气体,左侧水柱下降 | |
| ④ | 10 mL 20% HNO3溶液,3 mL H2O2 | 溶液变蓝比③慢,产生无色气体,左侧水柱下降 |
| A.①中实验现象说明O2参与了反应 |
| B.②中溶液颜色比①深可能是由于H2O2氧化Cu生成Cu2+ |
| C.③中左侧水柱下降可能是反应产生NO气体导致的 |
| D.④比③变蓝慢是由于H2O2分解造成自身消耗 |
您最近一年使用:0次