“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义。请回答下列问题:
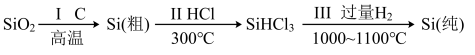
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
①写出步骤I的化学方程式:
②步骤II经过冷凝得到的SiHCl3(沸点为33.0℃)中含有少量的SiCl4(沸点为57.6℃)和HCl(沸点为-84.7℃),提纯SiHCl3的实验方法是
(2)磁性材料。这种黑色材料含有某种铁的氧化物,请写出该氧化物溶于稀硫酸溶液的化学方程式
(3)激光材料。我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料。请用离子方程式来证明它是一种两性氧化物:
(4)高分子材料。一种新型高效净水剂[Al Fe (OH)n Cl6-n]m属于无机高分子材料,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为
(5)合金材料。取等质量的两份某镁铝合金分别加入足量的稀盐酸和氢氧化钠溶液中,产生的H2体积分别为100mL、90mL则该合金中镁,铝的质量之比为
(6)消毒材料。棕黄色强刺激性气体Cl2O为国际公认高效安全灭菌消毒剂之一,实验室可用潮湿的Cl2与Na2CO3反应制取少量Cl2O,补充完整并配平下列反应方程式:
_______Cl2+_______Na2CO3+_______=_______NaHCO3+_______NaCl+_______Cl2O
相似题推荐
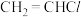 )是一种应用于高分子化工的重要单体,为无色、易液化气体,沸点为
)是一种应用于高分子化工的重要单体,为无色、易液化气体,沸点为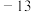 ℃。实验室可利用
℃。实验室可利用 、HCl、
、HCl、 的混合气体在催化剂作用下加热制备氯乙烯。回答下列问题:
的混合气体在催化剂作用下加热制备氯乙烯。回答下列问题:Ⅰ.HCl的制备
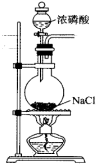
(1)盛装浓磷酸的仪器名称为
 的物质的量之比为2∶1,写出该反应的化学方程式:
的物质的量之比为2∶1,写出该反应的化学方程式:(2)磷酸浓度过低或过高均不利于HCl的逸出,写出磷酸浓度过低不利于HCl逸出的原因:
Ⅱ.氯乙烯的制备
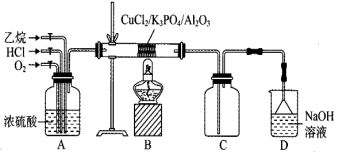
(3)①氯乙烯的电子式为
②A装置的作用为
③B中反应的化学方程式为
(4)该制备过程中会有副反应发生,生成副产物乙烯。
 为该反应的催化剂,其中
为该反应的催化剂,其中 为主催化剂,为了提高反应物的转化率和产物氯乙烯的选择性,常需加入助催化剂如KCl、
为主催化剂,为了提高反应物的转化率和产物氯乙烯的选择性,常需加入助催化剂如KCl、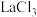 等,图1为K、Cu物质的量之比对催化剂活性的影响,图2为La的百分含量对催化剂活性的影响:
等,图1为K、Cu物质的量之比对催化剂活性的影响,图2为La的百分含量对催化剂活性的影响:
则实际生产过程中应选择的K、Cu的物质的量之比为
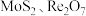 ,少量
,少量 )中回收铼的工艺流程如图所示:
)中回收铼的工艺流程如图所示: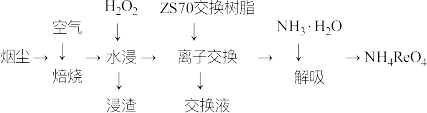
已知:①低价铼
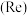 元素易被氧化。②
元素易被氧化。②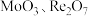 易溶于水生成
易溶于水生成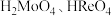 ,其它钼、铼的氧化物难溶于水。③钼元素与硫酸根可形成配离子。
,其它钼、铼的氧化物难溶于水。③钼元素与硫酸根可形成配离子。回答下列问题:
(1)
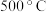 焙烧产物基本全部为
焙烧产物基本全部为 。焙烧时
。焙烧时 反应的化学方程式为:
反应的化学方程式为:①

②
(2)水浸时,加入
 的作用是
的作用是(3)已知
 在水中的溶解度:
在水中的溶解度:温度 | 18 | 30 | 45 | 60 | 70 | 80 |
溶解度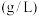 | 0.106 | 0.257 | 0.365 | 0.421 | 0.466 | 0.518 |
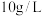 ,可能原因为
,可能原因为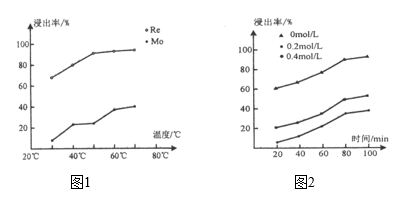
 )与树脂上的官能团发生交换反应达到平衡。浸取液中
)与树脂上的官能团发生交换反应达到平衡。浸取液中 浓度对铼的吸附率影响如图2所示,铼的浸出率随
浓度对铼的吸附率影响如图2所示,铼的浸出率随 浓度变化的原因为
浓度变化的原因为(5)
 的立方晶胞结构如下图所示,则
的立方晶胞结构如下图所示,则 配位数为
配位数为 ,则晶胞参数
,则晶胞参数
 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。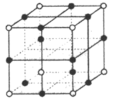
 及少量
及少量 、
、 等)来制取绿矾
等)来制取绿矾 。具体制备流程如下:
。具体制备流程如下: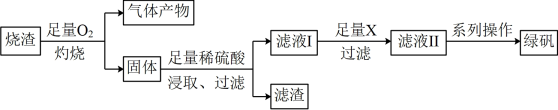
回答下列关于上述流程图中转化关系及操作的有关问题:
(1)在“灼烧”过程中发生的主要反应为:
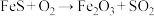 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为(2)所得气体产物
 属于
属于 ,请你写出用过量氨水吸收
,请你写出用过量氨水吸收 时发生反应的离子方程式
时发生反应的离子方程式(3)加入足量X时发生反应的离子方程式为:
(4)系列操作包括:
(5)绿矾保存不当容易被氧化变质,为了检验所得产品是否变质,技术人员进行了以下操作:取少量产品(绿矾)置于试管中加水溶解,向溶液中加入
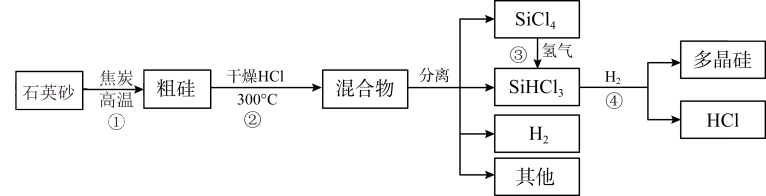
回答下列问题:
(1)反应①中氧化剂与还原剂的物质的量之比为
 的化学方程式为
的化学方程式为(2)反应③氢化过程中所需的高纯度
 可通过电解精制的饱和食盐水制得,粗盐水精制过程中,为有效除去
可通过电解精制的饱和食盐水制得,粗盐水精制过程中,为有效除去 等杂质,要按
等杂质,要按 、b.
、b. 、c.
、c. ,过滤后再向滤液中加盐酸调节
,过滤后再向滤液中加盐酸调节 。
。(3)反应④中
 还原
还原 过程中若混入
过程中若混入 ,除可能引起爆炸外,还可能引起
,除可能引起爆炸外,还可能引起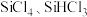 和
和 外,还有
外,还有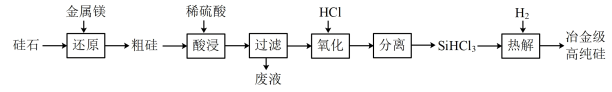
请回答下列问题:
(1)硅元素在周期的位置为
(2)“还原”过程需在高温下进行,该反应的生成物除硅和MgO外,还可能有
(3)加快“酸浸”速率的方法有
(4)“氧化”过程发生的主要反应为Si+3HCl=SiHCl3 +H2,该反应中还原产物为
(5)在还原炉中H2与SiHCl3加热到1100~1200℃发生“热解”反应即制取冶金级高纯硅,还原炉中发生反应的化学方程式为
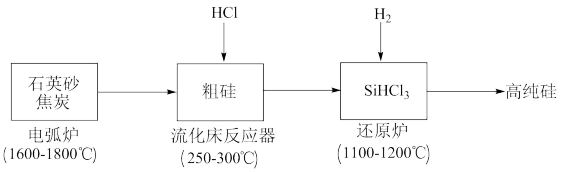
(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl 等,粗硅生成SiHCl3的化学反应方程式
(3)有关物质的熔沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和
| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 熔点/°C | 1410 | -70.4 | -126.5 | -122 | -118 | -114.2 | -185 |
| 沸点/°C | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
(4)还原炉中发生的化学反应为:
(5)上述工艺生产中循环使用的物质除Si、SiHCl3外,还有

(1)画出白色沉淀1中金属元素的原子结构示意图
(2)在惰性气流中加热X至完全分解的化学反应方程式为
(3)白色沉淀2在空气中变成红褐色沉淀的原因是
(4)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式
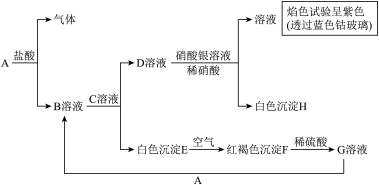
(1)写出C和H的化学式:C
(2)写出E转变成F的化学方程式:
(3)向G溶液中除加入A外,加入Cu也能生成B,写出G中加入Cu反应的离子方程式
(4)向G溶液中加入一定量A后,为检验所得溶液中金属阳离子,某兴趣小组提出了如下猜想:
猜想1:溶液中含Fe2+;
猜想2:溶液中含Fe3+;
猜想3:溶液中含
兴趣小组设计实验检验所得溶液中金属阳离子
| 实验方案 | 实验现象 | 结论 | |
| 步骤1 | 取待少量检测液于试管中,向其中滴加少量酸性高锰酸钾溶液 | 猜想三成立 | |
| 步骤2 | |||
②步骤2涉及的离子反应方程式是

(1)配制溶液所用的蒸馏水必须先除去溶解的氧气,具体方法是
(2)实验过程中,将生成的FeSO4溶液和NH4HCO3溶液混合的操作是
(3)装置B中的NH4HCO3需过量的原因
a.除去FeSO4溶液中残留的硫酸 b.Fe2+充分转化为FeCO3
c.NH4HCO3溶解度比较大 d.NH4HCO3受热分解损失
(4)碳酸亚铁在潮湿的空气中逐渐被氧化生成氢氧化铁和一种气体,反应的化学方程式为
(5)有同学提出该实验可用FeSO4,与Na2CO3反应制取FeCO3,经查阅:0.1mol/LNa2CO3溶液pH约为11.6;25℃时,Ksp[FeCO3]=3.1×10—11,Ksp[Fe(OH)2]=4.9×10—17,向10mL0.1mol/LNa2CO3溶液中滴加0.1mol/L FeSO4溶液,先析出的沉淀是
(6)NaHCO3与NH4HCO3均可作为Fe2+的沉淀剂,但更常用NH4HCO3,理由是
(7)设计实验检验制得的产品中是否含Fe3+



