题型:未知-未知
难度:0.65
引用次数:176
题号:12015241
可逆反应①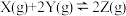 ,②
,② 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:

下列判断正确的是
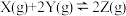 ,②
,② 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
分别在密闭容器的两个反应室中进行,反应室之间有无摩擦力、可自由滑动的密封隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
下列判断正确的是
| A.反应①的正反应是吸热反应 |
| B.达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为14:15 |
| C.达平衡(Ⅰ)时,X的转化率为5/11 |
| D.在平衡(Ⅰ)和平衡(Ⅱ)中,M在隔板右边气体中的体积分数不变 |
更新时间:2020-12-25 20:44:25
|
相似题推荐
未知-未知
|
适中
(0.65)
【推荐1】对于反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下下列说法正确的是
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下下列说法正确的是
 CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下下列说法正确的是
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下下列说法正确的是| A.加入催化剂,改变了反应的途径,反应的ΔH也随之改变 |
| B.改变压强,平衡不发生移动,反应放出的热量变大 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.增加反应物的浓度,反应速率加快,原因是单位体积内增加了活化分子的数目。 |
您最近一年使用:0次
未知-未知
|
适中
(0.65)
【推荐2】已知:xA(g)+yB(g)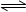 zC(g);△H=a。将xmolA和ymolB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)与反应时间(t)的关系如图所示。下列判断正确的是( )
zC(g);△H=a。将xmolA和ymolB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)与反应时间(t)的关系如图所示。下列判断正确的是( )

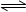 zC(g);△H=a。将xmolA和ymolB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)与反应时间(t)的关系如图所示。下列判断正确的是( )
zC(g);△H=a。将xmolA和ymolB混合在密闭容器中,在不同温度(T1>T2)及压强(P1>P2)下,C的物质的量n(C)与反应时间(t)的关系如图所示。下列判断正确的是( )
| A.x+y=z;a>0 | B.x+y>z;a<0 |
| C.x+y<z;a<0 | D.x+y<z;a>0 |
您最近一年使用:0次
未知-未知
|
适中
(0.65)
名校
【推荐1】采用CO与H2反应合成再生能源甲醇,反应如下:CO(g)+ 2H2(g)  CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、 压强(p)的关系如图所示。则下列符合题意的是
CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、 压强(p)的关系如图所示。则下列符合题意的是

 CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、 压强(p)的关系如图所示。则下列符合题意的是
CH3OH(g),在一容积可变的密闭容器中充有10molCO和20mol H2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、 压强(p)的关系如图所示。则下列符合题意的是
| A.B点的速率比C点的大 |
| B.A、B、C三点的平衡常数KA、KB、KC的大小关系为:KA=KB>KC |
| C.若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为5L |
| D.若增大H2的浓度,则CO 和H2的平衡转化率(α)均会增大 |
您最近一年使用:0次
未知-未知
|
适中
(0.65)
【推荐2】恒温、恒压下,1 mol A和1 mol B在一个容积可变的容器中发生如下反应:A(g)+2B(g)  2C(g)。一段时间后达到平衡,生成a mol C。下列说法不正确的是
2C(g)。一段时间后达到平衡,生成a mol C。下列说法不正确的是
 2C(g)。一段时间后达到平衡,生成a mol C。下列说法不正确的是
2C(g)。一段时间后达到平衡,生成a mol C。下列说法不正确的是| A.起始时刻和达到平衡后容器中的压强比为1:1 |
| B.物质A、B的转化率之比一定是1:2 |
| C.若起始放入3 mol A和3 mol B,则达到平衡时生成3a mol C |
| D.当v正(A)=v逆(B)时,可断定反应达到平衡 |
您最近一年使用:0次

 2HI(g)加压后,混合气体的颜色加深
2HI(g)加压后,混合气体的颜色加深 Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:
Cl2(g)+CO(g),向2.0 L恒容密闭容器中充入1.0 mol COCl2(g),反应过程中测得的有关数据见下表:

