向CH3COOH⇌CH3COO-+H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变小的是
| A.H2O | B.CH3COONa(s) | C.NaOH(s) | D.HCl(g) |
更新时间:2020-12-28 10:00:57
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列方程式书写正确的是( )
A.HCO 在水溶液中的电离方程式:HCO 在水溶液中的电离方程式:HCO +H2O +H2O H3O++CO H3O++CO |
B.H2SO3的电离方程式H2SO3 2H++SO 2H++SO |
C.CO 的水解方程式:CO 的水解方程式:CO +2H2O +2H2O H2CO3+2OH- H2CO3+2OH- |
D.CaCO3的电离方程式:CaCO3 Ca2++CO Ca2++CO |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】25°C时,向10mL0.10 mol·L−1的一元弱酸HA(Ka=1.0×10−3)中逐滴加入0.10mol·L−1NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示。下列说法正确的是
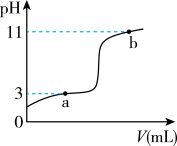
| A.a点时,c(HA)+c(OH-)=c(Na+)+c(H+) |
| B.溶液在a点和b点时水的电离程度相同 |
| C.b点时,c(Na+)=c(HA)+c(A-)+c(OH-) |
| D.V=10mL时,c(Na+)>c(A-)>c(H+)>c(HA) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】常温下,纯水中存在电离平衡:H2O H++OH-。欲使水的电离平衡向正方向移动,并使c(H+)增大,应加入的物质是( )
H++OH-。欲使水的电离平衡向正方向移动,并使c(H+)增大,应加入的物质是( )
 H++OH-。欲使水的电离平衡向正方向移动,并使c(H+)增大,应加入的物质是( )
H++OH-。欲使水的电离平衡向正方向移动,并使c(H+)增大,应加入的物质是( )| A.H2SO4 | B.AlCl3 |
| C.NaHCO3 | D.NaOH |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列事实中一定能证明 是弱电解质的是
是弱电解质的是
①用 溶液做导电实验,灯泡很暗
溶液做导电实验,灯泡很暗
②往 溶液中滴加
溶液中滴加 溶液,产生大量气泡
溶液,产生大量气泡
③0.1
 溶液中
溶液中
④1mL 的
的 溶液稀释至1L,
溶液稀释至1L,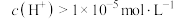
⑤20mL 0.2
 溶液恰好与20mL 0.2
溶液恰好与20mL 0.2 NaOH溶液完全反应
NaOH溶液完全反应
 是弱电解质的是
是弱电解质的是①用
 溶液做导电实验,灯泡很暗
溶液做导电实验,灯泡很暗②往
 溶液中滴加
溶液中滴加 溶液,产生大量气泡
溶液,产生大量气泡③0.1

 溶液中
溶液中
④1mL
 的
的 溶液稀释至1L,
溶液稀释至1L,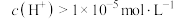
⑤20mL 0.2

 溶液恰好与20mL 0.2
溶液恰好与20mL 0.2 NaOH溶液完全反应
NaOH溶液完全反应| A.①② | B.②③ | C.②⑤ | D.③④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】在CH3COOH溶液中存在如下平衡:CH3COOH⇌H++CH3COO-。加入少量下列物质或采取下述方法,能使平衡逆向移动的是
| A.加水 | B.CH3COONa固体 | C.升温 | D.NaCl固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列方法中不能使0.10mol/L氨水中NH3·H2O电离程度增大的是
| A.加水稀释 | B.微热溶液 |
| C.滴加少量浓盐酸 | D.加入少量氯化铵晶体 |
您最近一年使用:0次





