下列关于O、Na、S、Cl、K元素及其化合物的说法正确的是
| A.第一电离能:I1(K)>I1(Na) |
| B.沸点:H2S>H2O |
| C.原子半径:r(K)>r(Cl)>r(S)>r(O) |
| D.热稳定性:HCl>H2S |
21-22高三上·江苏扬州·阶段练习 查看更多[6]
江苏扬州市2021届高三1月调研考试化学试题江苏省扬州市2021届高三上学期检测化学试题江苏省苏州市相城区陆慕高级中学2021-2022学年高三上学期第一次阶段性诊断测试化学试题(已下线)2022年江苏卷高考真题变式题1-13专题2 原子结构与元素性质 本专题达标检测(已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题1-5)
更新时间:2021-01-07 10:44:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列微粒性质递变正确的是( )
| A.原子半径:C、A1、Na、K依次增大 |
| B.离子半径:O2-、F-、A13+、Mg2+、Na+ 依次减小 |
| C.热稳定性:HF、NH3、PH3、SiH4 依次增强 |
| D.非金属性:Si、P、S依次减弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】巴蜀化学兴趣小组在研究元素周期表的形成历史史料时,查询到下列史料片段:1869年门捷列夫把当时已知的元素根据元素性质、相对原子质量等进行排列,预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如图所示。下列说法不正确的是

| A.甲的单质可以用作半导体材料 |
B.乙的氢化物稳定性比 弱 弱 |
| C.甲的最高价氧化物对应水化物是难溶于水的强酸 |
D.原子半径关系 甲 甲 乙 乙 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某种咪唑盐具有良好的导电性,其结构如下.X、Y、Z原子序数依次增大,均为短周期主族元素.下列说法正确的是


A.原子半径: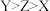 | B.分子的极性: |
C.简单氢化物的还原性: | D.该化合物具有良好的导电性,是因为它含有有机环状结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W四种短周期元素在元素周期表中的位置如图所示。已知Z元素原子内层电子数是最外层电子数的2倍,下列说法正确的是
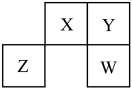

| A.简单离子半径:W>Y>X |
| B.简单气态氯化物的稳定性:X>Y>W |
| C.WX2是一种比较安全的漂白剂和消毒剂 |
| D.Z、W最高价氧化物的水化物均属于强电解质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知X、Y、Z是同一周期的主族金属元素,I为电离能,单位是 。根据下表所列数据判断错误的是
。根据下表所列数据判断错误的是
 。根据下表所列数据判断错误的是
。根据下表所列数据判断错误的是| 元素 |  |  |  |  | 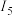 |
| X | 500 | 4600 | 6900 | 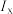 | 13350 |
| Y | 740 | 1450 | 7730 | 10540 | 13630 |
| Z | 580 | 1800 | 2700 | 11600 | 14830 |
| A.X、Y、Z三种元素的化合价依次为+1、+2、+3 |
B.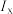 值可能在9200~11050之间 值可能在9200~11050之间 |
| C.若X、Y、Z是第三周期元素,则它们分别为Na、Al、Mg |
| D.Y、Z的第一、第二电离能数据大小关系恰好相反与ns能级上电子数目有关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据。
根据以上数据分析,下列说法正确的是
元素 | I1/eV | I2/eV | I3/eV |
甲 | 5.7 | 47.4 | 71.8 |
乙 | 7.7 | 15.1 | 80.3 |
丙 | 13.0 | 23.9 | 40.0 |
丁 | 15.7 | 27.6 | 40.7 |
| A.甲的金属性比乙弱 | B.乙的化合价为+1价 |
| C.丙一定为非金属元素 | D.丁一定为金属元素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】第IVA、VA、VIA、VIIA族元素的气态氢化物的沸点与周期数的关系如图。有关说法不正确 的是


| A.甲曲线中第二周期元素的气态氢化物的沸点显著高于第三周期元素气态氢化物的沸点,其原因是分子间存在氢键 |
| B.乙曲线中第三、四、五周期元素的气态氢化物的沸点依次升高,其原因是它们的范德华力依次增大 |
| C.丙曲线中第二、三、四、五周期元素的气态氢化物均极易溶于水,并且易液化 |
| D.丁曲线表示第IVA族元素气态氢化物的沸点随周期数递增而逐渐增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W 均为短周期主族元素,它们在周期表中的相对位置如图,下列说法正确的是
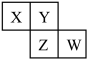

| A.Y 的价层电子排布式是ns2np5 |
| B.X、Z、W 的最高价氧化物所对应的水化物不可能均是强酸 |
| C.Y、Z 之间可形成离子型化合物 |
| D.四种元素所形成的最简单氢化物中,沸点最高的可能是Y 的氢化物 |
您最近一年使用:0次

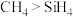

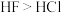
 >
>
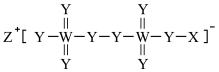
 ,X原子核外有3个未成对电子,Y原子的s和p轨道的电子数相同。下列说法一定正确的是
,X原子核外有3个未成对电子,Y原子的s和p轨道的电子数相同。下列说法一定正确的是 分子内含有N≡N,
分子内含有N≡N, 极易溶于水,液氨可用作制冷剂
极易溶于水,液氨可用作制冷剂 (g)的高
(g)的高 具有还原性,可用作喷气式发动机的燃料
具有还原性,可用作喷气式发动机的燃料

