X、Y、Z、W是元素周期表中前四周期的元素,其有关性质或结构信息如下表:
(1)X、Y、Z元素的第一电离能由小到大的顺序是____________ 用元素符号表示)。
(2)W元素基态原子的价层电子排布式是_____________ ,X元素基态原子中电子占据最高能级的电子云轮廓图为_______ 形。
(3)ZY2中Z原子的杂化类型为_______ ,ZY2易溶于水的原因可能是__________ (填序号)。
①ZY2与水极性相同 ②ZY2可以与水反应 ③ZY2可以与水形成氢键
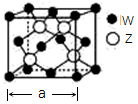
(4)W与Z所形成化合物晶体的晶胞如图所示。W离子的配位数是_____________ ,Z离子填充在W离子形成的正四面体空隙中,其空隙填充率是_________________ 。若该晶体的密度为dg·cm-3,阿伏加德罗常数的值为NA,则该晶胞参数a=______________ nm。
| 元素 | 有关性质或结构信息 |
| X | 基态原子2p轨道中有三个未成对电子 |
| Y | 基态原子最外层电子数是其内层电子数的3倍 |
| Z | 基态原子的3p轨道上有4个电子 |
| W | 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2 |
(1)X、Y、Z元素的第一电离能由小到大的顺序是
(2)W元素基态原子的价层电子排布式是
(3)ZY2中Z原子的杂化类型为
①ZY2与水极性相同 ②ZY2可以与水反应 ③ZY2可以与水形成氢键
(4)W与Z所形成化合物晶体的晶胞如图所示。W离子的配位数是

更新时间:2020-12-31 10:20:14
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】请按要求填空:
(1)C、N元素形成的新材料具有如图所示的结构该晶体的化学式为________________ 。

(2)氮化碳和氮化硅晶体结构相似,是新型的非金属高温陶瓷材料,它们的硬度大、熔点高、化学性质稳定。
①氮化硅的硬度________ (填“大于”或“小于”)氮化碳的硬度,原因是___________________________ 。
②已知氮化硅的晶体结构中,原子间都以单键相连,且氮原子与氮原子不直接相连、硅原子与硅原子不直接相连,同时每个原子都满足最外层8电子稳定结构,请写出氮化硅的化学式:______________ 。
(3)第ⅢA、VA元素组成的化合物GaN、GaP、CaAs等是人工合成的新型半导体材料,其晶体结构与晶体硅相似。在GaN晶体中,每个Ga原子与________ 个N原子相连,与同一个Ga原子相连的N原子构成的空间构型为________ 。在四大晶体类型中,GaN属于________ 晶体。
(1)C、N元素形成的新材料具有如图所示的结构该晶体的化学式为

(2)氮化碳和氮化硅晶体结构相似,是新型的非金属高温陶瓷材料,它们的硬度大、熔点高、化学性质稳定。
①氮化硅的硬度
②已知氮化硅的晶体结构中,原子间都以单键相连,且氮原子与氮原子不直接相连、硅原子与硅原子不直接相连,同时每个原子都满足最外层8电子稳定结构,请写出氮化硅的化学式:
(3)第ⅢA、VA元素组成的化合物GaN、GaP、CaAs等是人工合成的新型半导体材料,其晶体结构与晶体硅相似。在GaN晶体中,每个Ga原子与
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】钛及其化合物的研究与应用越来越受到人们的重视。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料,可由TiCl4和LiBH4反应制得。
①在基态Ti2+中,电子占据的最高能层符号为_____ ,该能层具有的原子轨道数为____
②LiBH4由Li+和BH4-构成,BH4-的立体结构是____ ,根据化合物LiBH4判断,Li、B、H的电负性由大到小的顺序为_____ 。
③TiCl4在常温下是无色液体,则TiCl4属于_______ (填“原子”“分子”或“离子”)晶体。
(2)高分子纳米活性钛无霸是借助紫外线或太阳光的照射,在其表面产生氧化性极强的活性离子,这种活性离子可以分解生活中的一些有害物质(如苯、甲醛、丙酮等)。
①丙酮(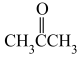 )分子中含有π键与σ键数目之比为
)分子中含有π键与σ键数目之比为______ 。
②甲醛( )分子中C原子轨道杂化类型为
)分子中C原子轨道杂化类型为_______ ;
甲醛易溶于水,原因是:a.甲醛和水都是极性分子,b._______ 。
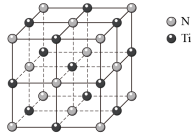
(3)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有__ 个,Ti原子的配位数为______ ;该晶胞中N、Ti原子之间的最近距离为a nm,则该氮化钛晶体的密度为_______ g·cm-3(NA为阿伏加 德罗常数的值,只列计算式)。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料,可由TiCl4和LiBH4反应制得。
①在基态Ti2+中,电子占据的最高能层符号为
②LiBH4由Li+和BH4-构成,BH4-的立体结构是
③TiCl4在常温下是无色液体,则TiCl4属于
(2)高分子纳米活性钛无霸是借助紫外线或太阳光的照射,在其表面产生氧化性极强的活性离子,这种活性离子可以分解生活中的一些有害物质(如苯、甲醛、丙酮等)。
①丙酮(
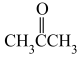 )分子中含有π键与σ键数目之比为
)分子中含有π键与σ键数目之比为②甲醛(
 )分子中C原子轨道杂化类型为
)分子中C原子轨道杂化类型为甲醛易溶于水,原因是:a.甲醛和水都是极性分子,b.
(3)某种氮化钛晶体的晶胞如图所示,该晶体中与N原子距离相等且最近的N原子有

您最近半年使用:0次
【推荐3】Ⅰ、下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
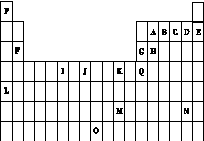
(1)写出基态时Q元素原子的电子排布式__________ ,J元素原子的外围电子排布图________________ 。
(2)下列对比正确的是__________ 。
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(3)关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是______ 。
a.L位于元素周期表第五周期ⅠA族,属于s区元素
b.O位于元素周期表第七周期Ⅷ族,属于ds区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
Ⅱ、已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(4)F、G元素对应的最高价含氧酸中酸性较强的化学式为__________ 。
(5)第一电离能:B__________ C,电负性:C__________ F。(填“<”、“>”或“=”)
(6)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为____________ ,试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式__________ 。
(7)写出E与D的最高价氧化物对应的水化物反应的化学方程式______________________ 。

(1)写出基态时Q元素原子的电子排布式
(2)下列对比正确的是
a.原子半径H>G>B>A b.第一电离能E>D>C>B
c.电负性A>H>G>Q d.最高价氧化物的水化物酸性B>A>H>G
(3)关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述不正确的是
a.L位于元素周期表第五周期ⅠA族,属于s区元素
b.O位于元素周期表第七周期Ⅷ族,属于ds区元素
c.M的外围电子排布式为6s1,属于ds区元素
d.H所在族的外围电子排布式为ns2np2,属于p区元素
Ⅱ、已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A是元素周期表中原子半径最小的元素,D3B中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C属同一周期,两者可以形成许多种共价化合物,C、F属同一主族,B原子最外电子层的p能级上的电子处于半满状态,C的最外层电子数是内层电子数的3倍,E最外层电子数比最内层多1。请用具体的元素回答下列问题:
(4)F、G元素对应的最高价含氧酸中酸性较强的化学式为
(5)第一电离能:B
(6)A、C形成的一种绿色氧化剂X有广泛应用,X分子中A、C原子个数比为1∶1,X的电子式为
(7)写出E与D的最高价氧化物对应的水化物反应的化学方程式
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】快离子导体是一类具有优良离子导电能力的固体电解质,研究得最多的是Ag、Cu、 Li、Na、F、O等的快离子导体。
(1)Cu-e-=Cu+的过程中,失去的电子是基态Cu中_______ 轨道上的电子。
(2)N、O、F的第一电离能从小到大的顺序为_______ (用元素符号表示);NH3、H2O、HF的沸点由低到高的顺序为_______ (用化学式表示)。
(3)“棕色环”现象是检验溶液中NO 的一种方法。向含有NO
的一种方法。向含有NO 溶液的试管中加入FeSO4,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[Fe(NO)(H2O)5 ]SO4。
溶液的试管中加入FeSO4,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[Fe(NO)(H2O)5 ]SO4。
①NO 中N元素采取
中N元素采取_______ 杂化,其立体构型为_______ (填名称)。
②[Fe(NO)(H2O)5]SO4中一种配体实际上是NO+,则其中Fe元素的化合价为_______ ;写出NO+的一种等电子体的化学式_______ 。
(4)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为_______ 。SiCl4可发生水解反应,机理如图:
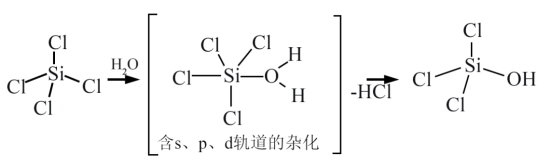
含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为_______ (填标号)。
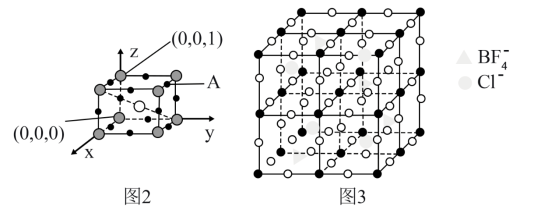
(5)Li3SBF4是潜在的快离子导体,其晶胞结构如图,A原子的坐标为_______ ;若在运算建立该晶体的模型过程中,晶胞中部分BF 被Cl- 取代后得到的晶胞结构如图3所示,则得到的晶体的化学式为
被Cl- 取代后得到的晶胞结构如图3所示,则得到的晶体的化学式为_______ 。
(1)Cu-e-=Cu+的过程中,失去的电子是基态Cu中
(2)N、O、F的第一电离能从小到大的顺序为
(3)“棕色环”现象是检验溶液中NO
 的一种方法。向含有NO
的一种方法。向含有NO 溶液的试管中加入FeSO4,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[Fe(NO)(H2O)5 ]SO4。
溶液的试管中加入FeSO4,随后沿管壁加入浓硫酸,在溶液界面上出现“棕色环”,研究发现棕色物质化学式为[Fe(NO)(H2O)5 ]SO4。①NO
 中N元素采取
中N元素采取②[Fe(NO)(H2O)5]SO4中一种配体实际上是NO+,则其中Fe元素的化合价为
(4)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为

含s、p、d轨道的杂化类型有:①dsp2、②sp3d、③sp3d2,中间体SiCl4(H2O)中Si采取的杂化类型为
(5)Li3SBF4是潜在的快离子导体,其晶胞结构如图,A原子的坐标为
 被Cl- 取代后得到的晶胞结构如图3所示,则得到的晶体的化学式为
被Cl- 取代后得到的晶胞结构如图3所示,则得到的晶体的化学式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
真题
解题方法
【推荐2】A.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为_________________ 。
(2)B的氢化物的分子空间构型是____________ 。其中心原子采取_________ 杂化。
(3)写出化合物AC2的电子式____________ ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为_____________ 。
(4)E的核外电子排布式是_____________ ,ECl3形成的配合物的化学式为_______ 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是________________________________________________ 。
B.醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4=HBr+NaHSO4①
R-OH+HBr R-Br+H2O ②
R-Br+H2O ②
可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br—被浓硫酸氧化为Br2等。有关数据列表如下;
请回答下列问题:
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是_______ 。(填字母)
a.圆底烧瓶 b.量筒 c.锥形瓶 d.布氏漏斗
(2)溴代烃的水溶性_______ (填“大于”、“等于”或“小于”);其原因是_______________________________________________________________________ 。
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在________ (填“上层”、“下层”或“不分层”)。
(4)制备操作中,加入的浓硫酸必需进行稀释,起目的是___________ 。(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(5)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是___________ 。(填字母)
a.NaI b.NaOH c.NaHSO3d.KCl
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于_____________ ;但在制备1-溴丁烷时却不能边反应边蒸出产物,其原因是___________________________ 。
(1)A、B、C的第一电离能由小到大的顺序为
(2)B的氢化物的分子空间构型是
(3)写出化合物AC2的电子式
(4)E的核外电子排布式是
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是
B.醇与氢卤酸反应是制备卤代烃的重要方法。实验室制备溴乙烷和1-溴丁烷的反应如下:
NaBr+H2SO4=HBr+NaHSO4①
R-OH+HBr
 R-Br+H2O ②
R-Br+H2O ②可能存在的副反应有:醇在浓硫酸的存在下脱水生成烯和醚,Br—被浓硫酸氧化为Br2等。有关数据列表如下;
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g·cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
请回答下列问题:
(1)溴乙烷和1-溴丁烷的制备实验中,下列仪器最不可能用到的是
a.圆底烧瓶 b.量筒 c.锥形瓶 d.布氏漏斗
(2)溴代烃的水溶性
(3)将1-溴丁烷粗产品置于分液漏斗中加水,振荡后静置,产物在
(4)制备操作中,加入的浓硫酸必需进行稀释,起目的是
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂
(5)欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是
a.NaI b.NaOH c.NaHSO3d.KCl
(6)在制备溴乙烷时,采用边反应边蒸出产物的方法,其有利于
您最近半年使用:0次
【推荐3】已知A、B、C、D、E、F、G为前四周期中的常见元素,且原子序数依次增大,A的原子半径最小;B的基态原子L层电子数是K层电子数的2倍;C与B同周期且基态原子最外层电子排布式为nsmnpm+2;D、E、F、G是位于同一周期的金属元素,元素D的焰色反应要透过蓝色钴玻璃才能观察到紫色;且D、G的原子序数相差10;E元素有多种化合价,它的一种氢氧化物在空气中易被氧化且最终变为红褐色,且E、F的电子数相差1。
请回答下列问题:
(1)基态E原子的价电子排布式为___ 。
(2)与BC分子互为等电子体的离子为___ (填化学式,任写一种)。
(3)在液态非极性分子B6A6中,B原子采取的杂化方式为___ 。
(4)元素C的简单氢化物的沸点比同主族的简单氢化物都高的原因是___ 。
(5)F可形成化学式均为F(NH3)5BrSO4的两种配合物,其中一种化学式为[F(NH3)5Br]SO4。向另一种配合物的溶液中加入BaCl2溶液时,无明显现象。若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为___ 。
(6)金属D、G晶体的晶胞结构如图所示。
①金属G的晶胞中,测得晶胞中G原子的半径为apm,则G晶体的密度为___ g/cm3(列出表达式即可,NA为阿伏加 德罗常数的值),D、G两种晶胞中金属的配位数之比为___ 。
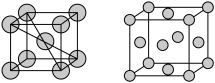
②金属G、锌两种元素的第一电离能、第二电离能如下表所示:
G的第二电离能(I2)大于锌的第二电离能(I2),其主要原因是___ 。
请回答下列问题:
(1)基态E原子的价电子排布式为
(2)与BC分子互为等电子体的离子为
(3)在液态非极性分子B6A6中,B原子采取的杂化方式为
(4)元素C的简单氢化物的沸点比同主族的简单氢化物都高的原因是
(5)F可形成化学式均为F(NH3)5BrSO4的两种配合物,其中一种化学式为[F(NH3)5Br]SO4。向另一种配合物的溶液中加入BaCl2溶液时,无明显现象。若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为
(6)金属D、G晶体的晶胞结构如图所示。
①金属G的晶胞中,测得晶胞中G原子的半径为apm,则G晶体的密度为

②金属G、锌两种元素的第一电离能、第二电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 |
| G | 746 | 1958 |
| 锌 | 906 | 1733 |
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】X、Y、Z、Q、R、W是原子序数依次增大的前四周期元素。X的原子核内无中子,Y与Z能形成两种无色无味的气体,Q与X同族,R在同周期主族元素中原子半径最小,基态原子W的3d能级有2个空轨道。请回答下列问题:
(1)W在元素周期表中的位置:_____ 。上述6种元素中电负性最大的是(填名称)_____ 。
(2)RZ-3的空间构型为_______ ,化合物YX4Z的沸点比YX3R高,其原因是____________ 。
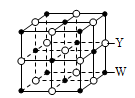
(3)Y和W能够形成强度极高的化合物G,其晶胞结构如图所示, G的化学式为________ 。如从该晶胞中抽出Y原子,所得晶胞即为单质W的晶胞,其配位数为________ 。
(4)强酸性溶液中,WZ 在加热条件下可以被X2Y2Z4还原为WZ,该反应的离子方程式是______________ 。
(1)W在元素周期表中的位置:
(2)RZ-3的空间构型为
(3)Y和W能够形成强度极高的化合物G,其晶胞结构如图所示, G的化学式为

(4)强酸性溶液中,WZ 在加热条件下可以被X2Y2Z4还原为WZ,该反应的离子方程式是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】二氯异氰尿酸钠(结构为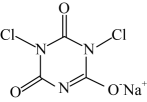 )是一种非常高效的强氧化性消毒剂。常温下是白色固体,难溶于冷水;合成二氯异氰尿酸钠的反应为
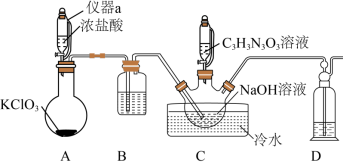
)是一种非常高效的强氧化性消毒剂。常温下是白色固体,难溶于冷水;合成二氯异氰尿酸钠的反应为 。某同学在实验室用如图装置制取二氯异氰尿酸钠(部分夹持装置已略)。
。某同学在实验室用如图装置制取二氯异氰尿酸钠(部分夹持装置已略)。
请回答下列问题:
(1)二氯异氰尿酸钠中N原子的杂化类型是___________ 。
(2)仪器a的名称是___________ ;仪器D中的试剂是___________ 。
(3)A中烧瓶内发生反应的化学方程式为___________ 。
(4)装置B的作用是___________ ;如果没有B装置,会产生的不良结果是___________ 。
(5)待装置C液面上方有黄绿色气体时,再滴加C3H3N3O3溶液,反应过程中需要不断通入Cl2的目的是___________ 。
(6)实验室测定二氯异氰尿酸钠样品中有效氯的原理如下:



准确称取mg样品,配成100mL溶液,取20.00mL所配溶液于碘量瓶中,加入稀H2SO4和过量KI溶液,充分反应后,加入淀粉溶液,用 标准溶液滴定,滴到终点时,消耗Na2S2O3标准溶液的体积为VmL,则样品有效氯含量为
标准溶液滴定,滴到终点时,消耗Na2S2O3标准溶液的体积为VmL,则样品有效氯含量为___________ %(有效氯含量 )。
)。
 )是一种非常高效的强氧化性消毒剂。常温下是白色固体,难溶于冷水;合成二氯异氰尿酸钠的反应为
)是一种非常高效的强氧化性消毒剂。常温下是白色固体,难溶于冷水;合成二氯异氰尿酸钠的反应为 。某同学在实验室用如图装置制取二氯异氰尿酸钠(部分夹持装置已略)。
。某同学在实验室用如图装置制取二氯异氰尿酸钠(部分夹持装置已略)。
请回答下列问题:
(1)二氯异氰尿酸钠中N原子的杂化类型是
(2)仪器a的名称是
(3)A中烧瓶内发生反应的化学方程式为
(4)装置B的作用是
(5)待装置C液面上方有黄绿色气体时,再滴加C3H3N3O3溶液,反应过程中需要不断通入Cl2的目的是
(6)实验室测定二氯异氰尿酸钠样品中有效氯的原理如下:



准确称取mg样品,配成100mL溶液,取20.00mL所配溶液于碘量瓶中,加入稀H2SO4和过量KI溶液,充分反应后,加入淀粉溶液,用
 标准溶液滴定,滴到终点时,消耗Na2S2O3标准溶液的体积为VmL,则样品有效氯含量为
标准溶液滴定,滴到终点时,消耗Na2S2O3标准溶液的体积为VmL,则样品有效氯含量为 )。
)。
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
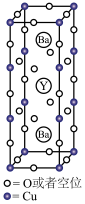
【推荐3】1911年,科学家发现汞在4.2K以下时电阻突然趋近于零——即低温超导性。1986年,科学家又发现了Nb3Ge在23K下具有超导性。1987年2月,赵忠贤及合作者独立发现了在液氮温区(沸点77 K)的高温超导体,其晶胞如图所示,元素组成为Ba-Y-Cu-O(临界温度93 K),推动了国际高温超导研究。赵忠贤院士获得2016年度国家最高科学技术奖。
回答下列问题:
(1)铌Nb位于第五周期,Nb的外围电子排布式为4d45s1,Nb位于_______ 族。
(2)下列关于Ge元素叙述正确的是______ (从下列选项中选择)。
A.Ge晶体属于准金属,且为原子晶体 B.Ge属于p区的过渡金属
C.Ge的第一电离能比As、Se均要小 D.Ge的电负性比C大
(3)Ge(CH3)2Cl2分子的中心原子Ge的杂化方式是______________ 。
(4)NH3也常作制冷剂,其键角_______ (填“大于”或“小于”)109°28′,主要原因是___________________________________________________________________________ 。
(5)图示材料的理想化学式(无空位时)为___________________ ,若Y(钇)元素的化合价为+3,则Cu的平均化合价为__________ 。

回答下列问题:
(1)铌Nb位于第五周期,Nb的外围电子排布式为4d45s1,Nb位于
(2)下列关于Ge元素叙述正确的是
A.Ge晶体属于准金属,且为原子晶体 B.Ge属于p区的过渡金属
C.Ge的第一电离能比As、Se均要小 D.Ge的电负性比C大
(3)Ge(CH3)2Cl2分子的中心原子Ge的杂化方式是
(4)NH3也常作制冷剂,其键角
(5)图示材料的理想化学式(无空位时)为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】根据已学物质结构与性质的有关知识,回答下列问题:
(1)请写出第三周期元素中p轨道上有3个未成对电子的元素符号:___________ ,某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是 ,该元素的名称是
,该元素的名称是___________ 。
(2)根据价层电子对互斥理论推测下列离子或分子的空间立体构型:
___________ ,
___________ 。
(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解,得到深蓝色的透明溶液,写出有关反应的离子方程式___________ 、___________ 。
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。则体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为___________ ;若两种晶体中最邻近的铁原子间距离相同,则体心立方晶胞和面心立方晶胞的密度之比为___________ 。
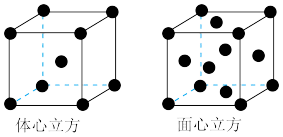
(1)请写出第三周期元素中p轨道上有3个未成对电子的元素符号:
 ,该元素的名称是
,该元素的名称是(2)根据价层电子对互斥理论推测下列离子或分子的空间立体构型:


(3)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解,得到深蓝色的透明溶液,写出有关反应的离子方程式
(4)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。则体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为

您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】氟化物在生产、生活和科研中应用广泛。
(1)基态F原子的价电子排布式为___________ 。
(2)HF、CH4、HCl的沸点由高到低的顺序为___________ 。
(3)OF2分子的空间构型为___________ 。
(4)CF2=CF2分子中C的杂化轨道类型为___________ ,聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因___________ 。
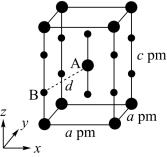
(5)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有___________ 个XeF2分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,
, ,
, )。已知Xe—F键长为r pm,则B点原子的分数坐标为
)。已知Xe—F键长为r pm,则B点原子的分数坐标为___________ ;晶胞中A、B间距离d=___________ pm。
(1)基态F原子的价电子排布式为
(2)HF、CH4、HCl的沸点由高到低的顺序为
(3)OF2分子的空间构型为
(4)CF2=CF2分子中C的杂化轨道类型为
(5)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
 ,
, ,
, )。已知Xe—F键长为r pm,则B点原子的分数坐标为
)。已知Xe—F键长为r pm,则B点原子的分数坐标为
您最近半年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】KI或KIO3可作为食盐的加碘剂,起到预防大脖子病的作用。
(1)基态I原子的价电子排布式为___________ 。
(2)食盐中往往还会加入一些Fe2+以供人体补铁。Fe2+可用K3[Fe(CN)6]检验,[Fe(CN)6]3-的配位数为___________ 。
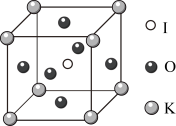
(3)KIO3晶体的晶胞结构如图所示,边长为a nm,晶胞中K、I、O分别处于顶角、体心、面心位置。
① 的空间构型为
的空间构型为___________ 。
②与K紧邻的O的个数为___________ ,在KIO3晶胞结构的另一种表示中,I处于各顶角的位置,则O处于___________ 位置。
③已知阿伏伽德罗常数的值为NA,则KIO3的密度为___________ (列式表示)g/cm3)。
(1)基态I原子的价电子排布式为
(2)食盐中往往还会加入一些Fe2+以供人体补铁。Fe2+可用K3[Fe(CN)6]检验,[Fe(CN)6]3-的配位数为
(3)KIO3晶体的晶胞结构如图所示,边长为a nm,晶胞中K、I、O分别处于顶角、体心、面心位置。

①
 的空间构型为
的空间构型为②与K紧邻的O的个数为
③已知阿伏伽德罗常数的值为NA,则KIO3的密度为
您最近半年使用:0次



