25°C时,水的电离达到平衡:H2O H++OH-,下列叙述不正确的是
H++OH-,下列叙述不正确的是
 H++OH-,下列叙述不正确的是
H++OH-,下列叙述不正确的是| A.将纯水加热到95℃时,Kw变大,pH减小,水仍呈中性 |
| B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw不变 |
| C.向水中加入少量固体硫酸氢钠,c(H+)增大,平衡逆向移动,KW不变 |
| D.向水中通入HCl气体,平衡逆向移动,溶液导电能力减弱 |
20-21高二上·河南驻马店·期末 查看更多[9]
广东省清远市名校2023-2024学年高二上学期期中调研联考化学试题吉林省长春市第二实验中学2023-2024学年高二上学期期中考试化学试题黑龙江省哈尔滨市第七十三中学校2022-2023学年高二上学期11月期中考试化学试题(已下线)考点27 水的电离与溶液的pH(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点27 水的电离和溶液的pH-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点23 弱电解质的电离-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点24 水的电离和溶液的酸碱性-备战2022年高考化学一轮复习考点帮(全国通用)河南省新蔡县2020-2021学年高二上学期期末调研考试化学试题
更新时间:2021-01-16 11:31:44
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】对于常温下pH为2的盐酸,下列叙述不正确的是
A.  |
| B.由H2O电离出的c(H+)=1.0×10-12mol•L-1 |
| C.与等体积pH=12的氨水混合后所得溶液显碱性 |
D.与等体积 乙酸钠溶液混合后所得溶液中: 乙酸钠溶液混合后所得溶液中: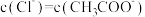 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据下列图示所得出的结论不正确的是
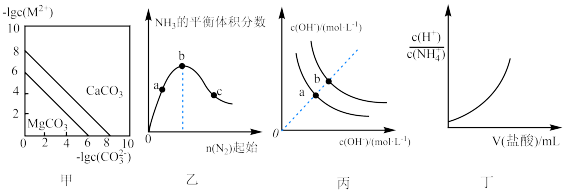
A.图甲表示一定温度下,MCO3(M:Mg2+、Ca2+)的沉淀溶解平衡曲线,则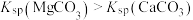 |
B.图乙是H2的起始量一定时恒温密闭容器中发生:N2(g)+3H2(g) 2NH3(g)反应,达到平衡时NH3的体积分数随N2的起始物质的量的变化曲线,则H2的转化率:b>c>a 2NH3(g)反应,达到平衡时NH3的体积分数随N2的起始物质的量的变化曲线,则H2的转化率:b>c>a |
| C.图丙表示不同温度下溶液中H+和OH-的浓度变化曲线,图中a点对应温度低于b点 |
D.图丁投示向0.lmol/L的NH4Cl溶液中滴加0.1mol/L的盐酸,溶液中 随盐酸的体积变化关系 随盐酸的体积变化关系 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】图为不同温度下水的电离平衡曲线,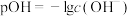 ,下列说法错误的是
,下列说法错误的是
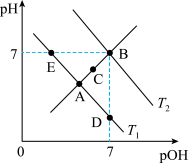
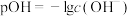 ,下列说法错误的是
,下列说法错误的是
A. 和 和 的关系是: 的关系是: |
| B.A点到D点:加入少量酸可实现 |
C. 的关系是: 的关系是: |
D. 时:pH=2的硫酸与pH=12的NaOH溶液等体积混合,溶液呈碱性 时:pH=2的硫酸与pH=12的NaOH溶液等体积混合,溶液呈碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列各组离子在相应条件下可能大量共存的是
A.能使pH试纸变橙色的溶液中:  、K+、Cl-、Na+ 、K+、Cl-、Na+ |
B.由水电离产生的c(H+)=1×10−10mol∙L−1的溶液中: 、Mg2+、Na+、 、Mg2+、Na+、 |
C.在 =1×1010的溶液中: =1×1010的溶液中: 、Fe2+、Cl-、 、Fe2+、Cl-、 |
D.加水稀释pH增大的溶液:Na+、K+、Cl-、 |
您最近一年使用:0次

 时,若溶液中由水电离产生的
时,若溶液中由水电离产生的 ,则下列说法正确的是
,则下列说法正确的是 一定为12
一定为12 溶液
溶液 、
、 、
、 、
、

