19. 习近平总书记近日对制止餐饮浪费作出重要指示。氨的合成对解决粮食危机有着重要意义。目前该研究领域已经催生了三位诺贝尔化学奖得主。
(1)德国化学家哈伯对研究“N
2(g)+3H
2(g)

2NH
3(g)”反应贡献巨大,1918年荣获诺贝尔化学奖,已知该反应在298 K时,
△H=-92.2 kJ/mol,
Kc=4.1×10
6(mol/L)
-2,若从平衡常数角度分析,反应限度已经较大,但为何化工生产中还需要使用催化剂:
_________。
(2)合成氨反应在催化剂作用下的反应历程为(*表示吸附态):
第一步 N
2(g)→2N
*;H
2(g)→2H
*(慢反应)
第二步 N
*+H
*
NH
*;NH
*+H
*
NH
2*;NH
2* +H
*
NH
3*;(快反应)
第三步 NH
3*
NH
3(g) (快反应)
比较第一步反应的活化能E
1与第二步反应的活化能E
2的大小:E
1__________E
2(填“>”、“<”或“=”),判断理由是
_______________________。
(3)2007年,德国科学家埃特尔发现了合成氨催化机理,开创了表面动力学的研究。研究发现,常温恒压密闭容器中,N
2在催化剂表面可以与水发生反应:2N
2(g)+6H
2O(l)

4NH
3(g)+3O
2(g)
①下列各项能够作为判断该反应一定达到平衡的依据是
___________(填标号)。
A.容器中N
2(g)、NH
3(g)、O
2(g)的浓度之比为2:4:3
B.N
2与NH
3浓度之比恒定不变
C.
v(N
2)
正=2
v(NH
3)
逆D.混合气体中氨气的质量分数不变
E.压强保持不变
②平衡后若分别改变下列一个条件,可以使N
2转化率增大的是
___________(填标号)
A.转移掉部分O
2 B.转移掉部分NH
3C.适当增加H
2O(l)的量
D.增加N
2的量
(4)向一个恒温恒压容器充入1 mol N
2和3 mol H
2模拟合成氨反应,下图为不同温度下平衡时混合物中氨气的体积分数与总压强(p)的关系图。
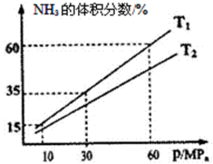
若体系在T
1、60MP
a下达到平衡。
①此时平衡常数
Kp_______(MP
a)
-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数;计算结果保留3位小数)。
②T
1_____________T
2(填“>”、“<”或“=”)。