NO氧化反应2NO(g)+O2(g) ⇌2NO2(g)分两步进行:I.2NO(g) ⇌N2O2(g) ∆H1;II.N2O2(g)+O2(g) ⇌2NO2(g) ∆H2,其反应过程能量变化示意图如图,下列说法不正确的是
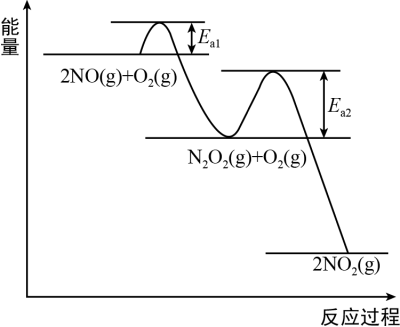

| A.由于 Ea1<Ea2,决定化学反应速率快慢的是反应Ⅱ |
| B.图示过程中,反应物断键吸收的能量小于生成物形成所释放的能量 |
| C.其它条件不变,升高温度,2NO(g)+O2(g) ⇌2NO2(g)反应速率一定加快 |
| D.其它条件不变,升高温度,2NO(g)+O2(g) ⇌2NO2(g)平衡一定逆向移动 |
2020·浙江绍兴·二模 查看更多[8]
(已下线)考点17 化学反应的热效应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点20 化学能与热能-备战2022年高考化学一轮复习考点帮(全国通用)河南省新蔡县2020-2021学年高二上学期期末调研考试化学试题浙江省瑞安市上海新纪元高级中学2019-2020学年高二下学期期末考试化学试题模拟卷05(必考+选考)——2020年秋高三化学开学摸底考试卷(全国通用)浙江省绍兴市上虞区2020届高三第二次教学质量调测化学试题
更新时间:2021-01-16 11:31:44
|
相似题推荐
【推荐1】下列说法正确的是
| A.等量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.任何放热反应在常温下一定能发生反应 |
| C.形成生成物化学键释放的能量大于破坏反应物化学键所吸收的能量时,反应为吸热反应 |
| D.对于吸热反应,反应物所具有的总能量低于生成物所具有的总能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列与化学反应能量变化相关的叙述正确的是
| A.生成物总能量一定低于反应物总能量 |
| B.应用盖斯定律,可计算某些难以直接测量的反应热 |
| C.放热反应的反应速率总是大于吸热反应的反应速率 |
| D.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列描述中,正确的是
| A.由 CH3CH2OH(l)+3O2(g) =2CO2 (g)+3H2O(g) ΔH=-1366.8 kJ·mol-1,可知乙醇的标准燃烧热为1366.8 kJ·mol-1 |
| B.已知:C(金刚石,s)=C(石墨,s) ΔH<0,则金刚石比石墨稳定 |
| C.已知:N2(g)+O2(g)=2NO(g) ΔH=+180 kJ·mol-12CO(g)+O2(g)=2CO2 (g) ΔH=-566 kJ·mol-1则2CO(g)+2NO(g)===N2 (g)+2CO2(g) ΔH=-746 kJ·mol-1 |
| D.OH-(aq)+H+(aq)===H2O(l)ΔH=-57.3 kJ·mol-1故1 molHNO3与1mol NH3•H2O 完全反应,放出的热量一定为57.3 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】2007年2月,中国首条“生态马路”在上海复兴路隧道建成,它运用了“光触媒”技术,在路面涂上一种光催化剂涂料,可将汽车尾气中45%的NO和CO转化成N2和CO2。下列对此反应的叙述中正确的
| A.使用光催化剂不改变反应速率 |
| B.使用光催化剂能增大NO的转化率 |
| C.升高温度能加快反应速率 |
| D.改变压强对反应速率无影响 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2。将-定比例的O2、NH3和NOx的混合气体,匀速通入装有催化剂M的反应器中反应,模拟NOx的去除。在不同温度下,反应相同时间,测得NOx的去除率如图所示,下列说法不合理的是( )
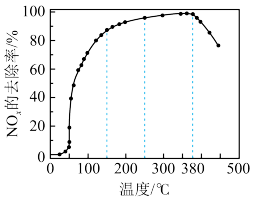

| A.低于50℃时,NOx去除率较低可能是因为反应速率较慢 |
| B.50~150℃时,NOx去除率迅速上升,只是因为温度升高导致反应速率加快引起的 |
| C.380℃以上,可能发生氨气的催化氧化反应,导致NOx的去除率降低 |
| D.无法由图象得出NH3与NOx反应生成N2的△H的正负 |
您最近一年使用:0次
单选题
|
适中
(0.65)
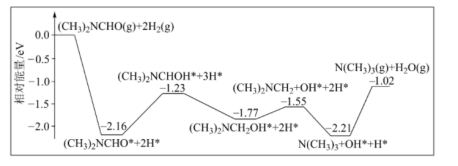
【推荐3】三甲胺(N (CH3)3)是重要的化工原料,最近我国科学家发明了使用铜催化剂将 二甲基甲酰胺 [N(CH3)2CHO,简称为
二甲基甲酰胺 [N(CH3)2CHO,简称为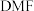 ]转化为三甲胺的合成路线,单一
]转化为三甲胺的合成路线,单一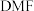 分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是
分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是
 二甲基甲酰胺 [N(CH3)2CHO,简称为
二甲基甲酰胺 [N(CH3)2CHO,简称为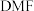 ]转化为三甲胺的合成路线,单一
]转化为三甲胺的合成路线,单一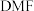 分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是
分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是 
| A.该历程中决速步骤为: (CH3)2NCH2OH*=(CH3)2NCH2+OH* |
B.该反应的原子利用率为 ,该历程中的最大能垒(活化能)为2.16eV ,该历程中的最大能垒(活化能)为2.16eV |
| C.升高温度可以加快反应速率,并提高DMF的平衡转化率 |
D.若 完全转化为三甲胺,则会释放出1.02eV·NA的能量 完全转化为三甲胺,则会释放出1.02eV·NA的能量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在催化剂作用下,以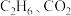 为原料合成
为原料合成 ,其主要反应有:
,其主要反应有:
反应1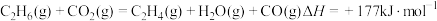
反应2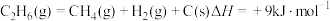
将体积比为 的
的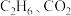 混合气体按一定流速通过催化反应管,测得
混合气体按一定流速通过催化反应管,测得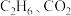 的转化率随温度变化的关系如图所示。
的转化率随温度变化的关系如图所示。
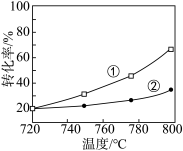
已知 的选择性
的选择性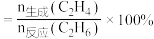
下列说法正确的是
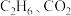 为原料合成
为原料合成 ,其主要反应有:
,其主要反应有:反应1
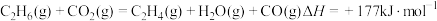
反应2
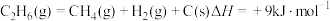
将体积比为
 的
的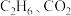 混合气体按一定流速通过催化反应管,测得
混合气体按一定流速通过催化反应管,测得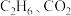 的转化率随温度变化的关系如图所示。
的转化率随温度变化的关系如图所示。
已知
 的选择性
的选择性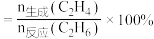
下列说法正确的是
A.图中曲线①表示 转化率随温度的变化 转化率随温度的变化 |
B.720~800℃范围内,随温度的升高,出口处 的量减少、 的量减少、 的量增大 的量增大 |
C.720~800℃范围内,随温度的升高, 的选择性不断增大 的选择性不断增大 |
D.其他条件不变,加入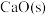 或选用高效催化剂,均能提高平衡时 或选用高效催化剂,均能提高平衡时 产率 产率 |
您最近一年使用:0次
【推荐2】化学实验在学科中有着非常重要的作用,结合图示实验装置,下列相关分析错误的是
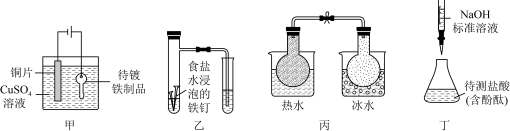

| A.用甲装置在铁制品表面镀铜 |
| B.用乙装置可验证铁的吸氧腐蚀 |
C.用丙装置可判断反应2NO2(g) N2O4(g)的△H<0 N2O4(g)的△H<0 |
| D.用丁装置可测定盐酸的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】三甲胺(N (CH3)3)是重要的化工原料,最近我国科学家发明了使用铜催化剂将 二甲基甲酰胺 [N(CH3)2CHO,简称为
二甲基甲酰胺 [N(CH3)2CHO,简称为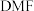 ]转化为三甲胺的合成路线,单一
]转化为三甲胺的合成路线,单一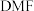 分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是
分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是

 二甲基甲酰胺 [N(CH3)2CHO,简称为
二甲基甲酰胺 [N(CH3)2CHO,简称为 ]转化为三甲胺的合成路线,单一
]转化为三甲胺的合成路线,单一 分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是
分子在铜催化剂表面的反应历程如图所示,(*表示物质吸附在铜催化剂上)下列说法正确的是 
| A.该历程中决速步骤为: (CH3)2NCH2OH*=(CH3)2NCH2+OH* |
B.该反应的原子利用率为 ,该历程中的最大能垒(活化能)为2.16eV ,该历程中的最大能垒(活化能)为2.16eV |
| C.升高温度可以加快反应速率,并提高DMF的平衡转化率 |
D.若 完全转化为三甲胺,则会释放出1.02eV·NA的能量 完全转化为三甲胺,则会释放出1.02eV·NA的能量 |
您最近一年使用:0次



