门捷列夫认为氮、碳、氧、氢是“四大天王”元素,它们与宇宙和生命的形成都有密切联系,可以相互结合成很多化合物。
(1)四种元素中,核外未成对电子数目相同的元素有_______ (填写元素符号,下同);四种元素的原子半径由大到小的顺序为_______ 。
(2)HCN是生命演化过程中的基础物质之一。已知HCN中C、N都满足8电子稳定结构,则HCN的电子式为_______ ;其中C、N之间的共用电子对偏向的元素是_______ ,从原子结构角度解释其原因_______ 。
(3)N2O是医学上的一种麻醉剂,可以通过反应_______NH3+_______O2→ _______N2O+_______H2O制得,配平该反应的化学方程式_______ ;若生成1.8 g水,转移的电子数目为_______ 个。已知N2O为直线型极性分子,则该分子中所含化学键的类型有_______ (填写编号)。
a.极性共价键 b.非极性共价键 c.离子键 d.金属键
(1)四种元素中,核外未成对电子数目相同的元素有
(2)HCN是生命演化过程中的基础物质之一。已知HCN中C、N都满足8电子稳定结构,则HCN的电子式为
(3)N2O是医学上的一种麻醉剂,可以通过反应_______NH3+_______O2→ _______N2O+_______H2O制得,配平该反应的化学方程式
a.极性共价键 b.非极性共价键 c.离子键 d.金属键
2021·上海浦东新·一模 查看更多[2]
更新时间:2021-01-20 10:12:26
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表是学习化学的重要工具,如图是元素周期表的一部分。
(1)很多科学家对元素周期表的发现和完善作出了重大贡献,其中,我国科学家___________ 主持测定了几种元素相对原子质量的新值;
(2)同种气态非金属元素的原子能够形成与粒子模型结构“ ”相似的分子,则图中形成该结构的一种分子的化学式为
”相似的分子,则图中形成该结构的一种分子的化学式为___________ ;
(3)图中与氟相邻的元素分别为氖、氯、氩,其中与氟元素的化学性质相似的是氯元素,原因是___________ 。

(1)很多科学家对元素周期表的发现和完善作出了重大贡献,其中,我国科学家
(2)同种气态非金属元素的原子能够形成与粒子模型结构“
 ”相似的分子,则图中形成该结构的一种分子的化学式为
”相似的分子,则图中形成该结构的一种分子的化学式为(3)图中与氟相邻的元素分别为氖、氯、氩,其中与氟元素的化学性质相似的是氯元素,原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据要求回答下列问题。
①CaBr2②H2O③NH4Cl④H2O2⑤Na2O2⑥ ⑦HClO⑧Al
⑦HClO⑧Al
(1)只含有离子键的是___________ (填序号,下同)。
(2)含有共价键的离子化合物是___________ 。
(3)属于共价化合物的是___________ 。
(4)熔融状态下和固态时都能导电的物质是___________ 。
(5)用电子式表示H2O的形成过程___________ 。
①CaBr2②H2O③NH4Cl④H2O2⑤Na2O2⑥
 ⑦HClO⑧Al
⑦HClO⑧Al(1)只含有离子键的是
(2)含有共价键的离子化合物是
(3)属于共价化合物的是
(4)熔融状态下和固态时都能导电的物质是
(5)用电子式表示H2O的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】二氧化碳的再利用是实现温室气体减排的重要途径之一。
(1)二氧化碳的电子式为__ 。
(2)下列二氧化碳所参与的反应中原子利用率达到100%的是__ (填字母)。
a.CO2+2NH3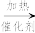 CO(NH2)2+H2O
CO(NH2)2+H2O
b.CO2+CH4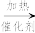 CH3COOH
CH3COOH
c.CO2+3H2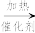 CH3OH+H2O
CH3OH+H2O
d.n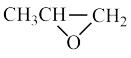 +nCO2
+nCO2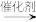

(3)在稀H2SO4中利用电催化可将CO2同时转化为多种燃料,其原理如图所示。

①一段时间后,Cu极区溶液质量__ (填“增加”“减少”或“不变”)。
②铜极上产生乙烯的电极反应式为__ 。
③若阴极只生成0.17molCO和0.33molHCOOH,则电路中转移电子的物质的量为__ mol。
(4)如图所示,某同学利用CO2生成的甲醚设计了一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

①写出甲中负极的电极反应式__ 。
②假设乙装置中氯化钠溶液足够多,若在标准状况下,有224mL氧气参加反应,则乙装置中阳离子交换膜左侧溶液质量将__ (填“增大”、“减小”或“不变”),且变化了__ 克;丙中阴极增重__ 克。
③若将乙装置中铁电极与石墨电极位置互换,其他装置不变,此时乙装置中发生的总反应式为__ 。
(1)二氧化碳的电子式为
(2)下列二氧化碳所参与的反应中原子利用率达到100%的是
a.CO2+2NH3
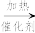 CO(NH2)2+H2O
CO(NH2)2+H2Ob.CO2+CH4
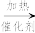 CH3COOH
CH3COOHc.CO2+3H2
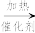 CH3OH+H2O
CH3OH+H2Od.n
 +nCO2
+nCO2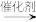

(3)在稀H2SO4中利用电催化可将CO2同时转化为多种燃料,其原理如图所示。

①一段时间后,Cu极区溶液质量
②铜极上产生乙烯的电极反应式为
③若阴极只生成0.17molCO和0.33molHCOOH,则电路中转移电子的物质的量为
(4)如图所示,某同学利用CO2生成的甲醚设计了一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。

①写出甲中负极的电极反应式
②假设乙装置中氯化钠溶液足够多,若在标准状况下,有224mL氧气参加反应,则乙装置中阳离子交换膜左侧溶液质量将
③若将乙装置中铁电极与石墨电极位置互换,其他装置不变,此时乙装置中发生的总反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)根据元素周期律,碳的非金属性强于硅,请用一个化学反应方程式表示___________________ 。
(2)若FeSO4和O2的系数比为2∶1,试配平下列方程式:
 FeSO4+
FeSO4+ K2O2→
K2O2→ K2FeO4+
K2FeO4+ K2O+
K2O+ K2SO4+
K2SO4+ O2↑
O2↑ __________________
(3)各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氮氧化物(NOx)废气的方法之一是用NaOH溶液进行吸收,现有NO与NO2的混合气体,将其通入50 mL 2 mol/L的NaOH溶液中,恰好完全吸收,测得溶液中含有NO3- 0.02 mol。
①所得溶液中NaNO2的物质的量为________ mol;
②混合气体中V(NO)∶V(NO2)=________ 。
(4)As2O3俗称砒霜,As2O3是两性偏酸性氧化物,是亚砷酸(H3AsO3)的酸酐,易溶于碱生成亚砷酸盐,写出As2O3与足量氢氧化钠溶液反应的离子方程式___________ 。
(2)若FeSO4和O2的系数比为2∶1,试配平下列方程式:
 FeSO4+
FeSO4+ K2O2→
K2O2→ K2FeO4+
K2FeO4+ K2O+
K2O+ K2SO4+
K2SO4+ O2↑
O2↑ (3)各种氮氧化物(NO、NO2)是主要的大气污染物之一,治理氮氧化物(NOx)废气的方法之一是用NaOH溶液进行吸收,现有NO与NO2的混合气体,将其通入50 mL 2 mol/L的NaOH溶液中,恰好完全吸收,测得溶液中含有NO3- 0.02 mol。
①所得溶液中NaNO2的物质的量为
②混合气体中V(NO)∶V(NO2)=
(4)As2O3俗称砒霜,As2O3是两性偏酸性氧化物,是亚砷酸(H3AsO3)的酸酐,易溶于碱生成亚砷酸盐,写出As2O3与足量氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁是人体中必需微量元素中含量最多,体内缺失会引起贫血。含FeO42-离子的盐具有强氧化性,能杀菌消毒,如高铁酸钾是一种新型、高效的消毒剂及绿色净水剂。铁及其化合物之间的相互转化可用下式表示: ,请回答下列有关问题:
,请回答下列有关问题:
(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液实现上述①的转化,要求产物纯净。可选用的试剂是___________ (选填序号);
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+→Cu2++5Fe2++2S,
则下列说法正确的是_________ (选填序号);
a.反应中,所有铁元素均被还原
b.从物质的组成来看,黄铜矿属于复盐
c.反应中,CuFeS2既作氧化剂又作还原剂
d.当转移1 mol 电子时,有46 g CuFeS2参加反应
(3)下列是工业制取高铁酸钾的一种方法,请在方框内填上合适的微粒符号并配平该离子方程式:
_______ Fe3+ +______ _________ +______ Cl2→_____ FeO42- + _____ Cl- +___ _____
 ,请回答下列有关问题:
,请回答下列有关问题:(1)Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液实现上述①的转化,要求产物纯净。可选用的试剂是
a.Cl2 b.Fe c.HNO3 d.H2O2
(2)上述转化得到的硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+→Cu2++5Fe2++2S,
则下列说法正确的是
a.反应中,所有铁元素均被还原
b.从物质的组成来看,黄铜矿属于复盐
c.反应中,CuFeS2既作氧化剂又作还原剂
d.当转移1 mol 电子时,有46 g CuFeS2参加反应
(3)下列是工业制取高铁酸钾的一种方法,请在方框内填上合适的微粒符号并配平该离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)储氢纳米碳管具有广泛的用途,电弧法合成的碳纳米管常伴有大量的杂质碳纳米颗粒,这种碳纳来颗粒可用氧化气化法提纯,反应的化学方程式如下(未配平):C+K2Cr2O7+H2SO4=CO2↑+K2SO4+Cr2(SO4)3+H2O。回答下列问题:
①配平上述反应方程式并用单线桥标出反应中电子转移方向和数目______ 。
②上述反应的离子方程式是_____ 。
③离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO 的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是
的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是______ 。
A.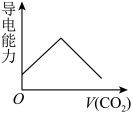 B.
B. C.
C.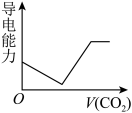 D.
D.
④若反应中电子转移了NA个,则产生的气体在标况下的体积为______ L;请写出Na2O2与该反应氧化产物反应的化学方式______ 。
(2)磷酸(H3PO4)、次磷酸(H3PO2)是精细磷化工产品,具有较强还原性,回答下列问题:
①H3PO2是一元中强酸,NaH2PO2为______ (填“正盐”或“酸式盐”)。
②H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于对器皿实现化学镀银,利用H3PO2进行化学镀银反应中,氧化产物为H3PO4,则氧化剂与还原剂的物质的量之比为______ 。
(1)储氢纳米碳管具有广泛的用途,电弧法合成的碳纳米管常伴有大量的杂质碳纳米颗粒,这种碳纳来颗粒可用氧化气化法提纯,反应的化学方程式如下(未配平):C+K2Cr2O7+H2SO4=CO2↑+K2SO4+Cr2(SO4)3+H2O。回答下列问题:
①配平上述反应方程式并用单线桥标出反应中电子转移方向和数目
②上述反应的离子方程式是
③离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO
 的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是
的摩尔电导率分别为0.60、1.98、0.45据此可判断,向饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是A.
 B.
B. C.
C. D.
D.
④若反应中电子转移了NA个,则产生的气体在标况下的体积为
(2)磷酸(H3PO4)、次磷酸(H3PO2)是精细磷化工产品,具有较强还原性,回答下列问题:
①H3PO2是一元中强酸,NaH2PO2为
②H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于对器皿实现化学镀银,利用H3PO2进行化学镀银反应中,氧化产物为H3PO4,则氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列物质:①H2②Na2O2③HCl④NaClO⑤CaCl2⑥NaHSO4⑦H2O2(填序号)
(1)只由离子键构成的物质是___ 。
(2)由极性键和非极性键构成的物质是___ 。
(3)由离子键和极性键构成的物质是___ 。
(4)属于共价化合物的物质是___ 。
(5)③溶于水时破坏键___ (填离子键、共价键,下同);⑥熔化时破坏___ 。
(1)只由离子键构成的物质是
(2)由极性键和非极性键构成的物质是
(3)由离子键和极性键构成的物质是
(4)属于共价化合物的物质是
(5)③溶于水时破坏键
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据要求回答下列问题:
(1)在 ①液氯 ②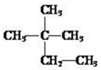 ③白磷 ④氯气
③白磷 ④氯气
⑤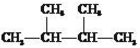 ⑥
⑥ ⑦
⑦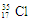 ⑧红磷
⑧红磷
这八种物质中,互为同分异构体的是____ ,互为同素异形体的是_____ 。(填序号)
(2)在下列固体中:①CaCl2 ②KOH ③He ④H2SO4 ⑤NH4Cl ⑥金刚石
①其中不含化学键的晶体是_________ ,
②既含有离子键又含有共价键的物质是______ ,
③固体熔化时只需破坏共价键的晶体是____ (填序号)
(1)在 ①液氯 ②
 ③白磷 ④氯气
③白磷 ④氯气⑤
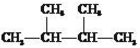 ⑥
⑥ ⑦
⑦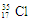 ⑧红磷
⑧红磷这八种物质中,互为同分异构体的是
(2)在下列固体中:①CaCl2 ②KOH ③He ④H2SO4 ⑤NH4Cl ⑥金刚石
①其中不含化学键的晶体是
②既含有离子键又含有共价键的物质是
③固体熔化时只需破坏共价键的晶体是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.现有下列物质:
1、Cl2 2、Na2O2 3、NaOH 4、HCl 5、H2O2 6、MgF2 7、Mg3N2
(1)只有离子键构成的物质是 (2)只有极性键构成的物质是
(3)只有非极性键构成的物质 (4)有极性键和非极性键构成的物质是
(5)有离子键和极性键构成的物质是(6)有离子键和非极性键构成的物质是
(7)属于离子化合物的是 (8)属于共价化合物的是
II.能够说明可逆反应2NO2 N2O4达到平衡状态的标志是_____________
N2O4达到平衡状态的标志是_____________
①单位时间消耗2mol NO2的同时,生成1 mol N2O4 ②恒温恒压下,混合气体的密度不变 ③NO2和N2O4的浓度之比为2∶1 ④混合气体的颜色不变 ⑤单位时间消耗4mol NO2的同时,消耗2mol N2O4
1、Cl2 2、Na2O2 3、NaOH 4、HCl 5、H2O2 6、MgF2 7、Mg3N2
(1)只有离子键构成的物质是 (2)只有极性键构成的物质是
(3)只有非极性键构成的物质 (4)有极性键和非极性键构成的物质是
(5)有离子键和极性键构成的物质是(6)有离子键和非极性键构成的物质是
(7)属于离子化合物的是 (8)属于共价化合物的是
II.能够说明可逆反应2NO2
 N2O4达到平衡状态的标志是_____________
N2O4达到平衡状态的标志是_____________ ①单位时间消耗2mol NO2的同时,生成1 mol N2O4 ②恒温恒压下,混合气体的密度不变 ③NO2和N2O4的浓度之比为2∶1 ④混合气体的颜色不变 ⑤单位时间消耗4mol NO2的同时,消耗2mol N2O4
您最近一年使用:0次
【推荐1】三元锂电池性能优异、能量密度高,正极材料包含了Ni、Co、Mn三种过渡金属的氧化物。
(1)基态Ni原子有___________ 个未成对电子,Ni2+核外电子排布式为___________ 。
(2)如表是Mn与Fe的部分电离能数据,解释I3(Mn)大于I3(Fe)的主要原因:___________ 。
(1)基态Ni原子有
(2)如表是Mn与Fe的部分电离能数据,解释I3(Mn)大于I3(Fe)的主要原因:
| 元素 | Fe | Mn |
| 第二电离能I2/(kJ·mol-1) | 1561 | 1509 |
| 第三电离能I3/(kJ·mol-1) | 2957 | 3248 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】黑火药是我国古代的四大发明之一,距今已有1000多年的历史,其成分是木炭(C)、硫粉(S)和硝酸钾(KNO3)。回答下列有关问题:
(1)黑火药爆炸生成无毒的气体和K2S,该反应的化学方程式为________________ 。
(2)Se与S同主族,则Se原子的核外电子排布式为〔Ar〕________ ,有____ 对成对电子。
(3)C、N、O、K的电负性由大到小的顺序是_________________ 。
(4)黑火药爆炸除生成K2S外,还生成少量K2S2,其结构类似于Na2O2。则K2S2中含有的化学键类型为_______________ 。
(5)K2S遇酸生成H2S,H2S分子中,S原子的杂化轨道类型是_________ ;KNO3可电离出NO3-,NO3-的空间构型是______________ 。
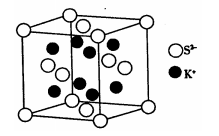
(6)K2S的晶胞结构如图所示。其中K+的配位数为_______ ,若K2S晶体的密度为ρg·cm-3,则晶胞中距离最近的两个S2-核间距为_________ cm(用NA表示阿伏伽德罗常数的值)
(1)黑火药爆炸生成无毒的气体和K2S,该反应的化学方程式为
(2)Se与S同主族,则Se原子的核外电子排布式为〔Ar〕
(3)C、N、O、K的电负性由大到小的顺序是
(4)黑火药爆炸除生成K2S外,还生成少量K2S2,其结构类似于Na2O2。则K2S2中含有的化学键类型为
(5)K2S遇酸生成H2S,H2S分子中,S原子的杂化轨道类型是
(6)K2S的晶胞结构如图所示。其中K+的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】早期发现的一种天然二十面体准晶颗粒由三种Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过_______________ 方法区分晶体、准晶体和非晶体。
(2)基态Fe原子有_________ 个未成对电子,Fe3+的电子排布式为_______________ 。可用硫氰化钾检验Fe3+,形成的配合物的颜色为_______________ 。
(3)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为____________ ,乙醛分子中各元素的电负性由大到小的顺序为_______________ 。乙酸的沸点明显高于乙醛,其主要原因是_____________________________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___________ 个铜原子。
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为__________ 。列式表示Al单质的密度_______________ g·cm-3。
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态Fe原子有
(3)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为
您最近一年使用:0次



