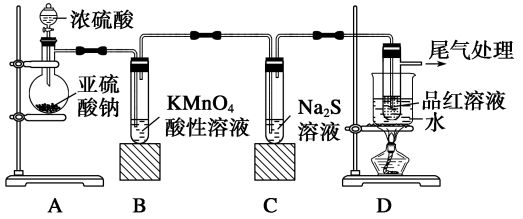
某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
(1)装置A中盛放亚硫酸钠(Na2SO3)的仪器名称是_______ ,若将亚硫酸钠改为铜片,与浓硫酸反应制取SO2,还缺少的仪器有_______ ,写出用铜片制取SO2的化学方程式_______ 。
(2)实验过程中,装置B中紫红色变为无色,说明SO2具有_______ (填“氧化性”或“还原性”),C中无色溶液中出现黄色浑浊,说明SO2具有_______ (填“氧化性”或“还原性”)。
(3)装置D的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象_______ 。
(1)装置A中盛放亚硫酸钠(Na2SO3)的仪器名称是
(2)实验过程中,装置B中紫红色变为无色,说明SO2具有
(3)装置D的目的是探究SO2与品红溶液作用的可逆性,请写出实验操作及现象
更新时间:2021-01-23 13:03:06
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E五种物质中含有同一种元素,A是淡黄色固体,其相互转化关系如图所示,回答下列问题:

(1)写出B、E的化学式:B_______ 、E_______ 。
(2)写出C→D的化学方程式:_______ 。
(3)将足量的物质C通入BaCl2溶液中,下列说法正确的是_______ (填序号)。
①溶液没有明显变化
②溶液中出现白色沉淀
③若继续通入Cl2,则溶液中出现白色沉淀

(1)写出B、E的化学式:B
(2)写出C→D的化学方程式:
(3)将足量的物质C通入BaCl2溶液中,下列说法正确的是
①溶液没有明显变化
②溶液中出现白色沉淀
③若继续通入Cl2,则溶液中出现白色沉淀
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】实验室中用下图装置(夹持装置已略去)研究不同价态硫元素之间的转化。
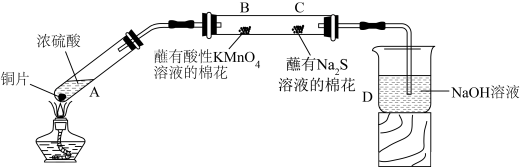
(1)A中产生的气体能使品红溶液褪色,A中反应的化学方程式为_______ 。
(2)由_______ (填现象)可推测出硫元素从+4价变为+6价。写出该反应对应的离子方程式_______ 。
(3)C处的现象为_______ 。
(4)D装置中发生反应的离子方程式为(NaOH溶液为足量)_______ 。

(1)A中产生的气体能使品红溶液褪色,A中反应的化学方程式为
(2)由
(3)C处的现象为
(4)D装置中发生反应的离子方程式为(NaOH溶液为足量)
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:

已知E是形成酸雨的主要气体,请回答:
(1)A的组成元素为______ (用化学符号表示);
(2)C溶液可溶解铜片,写出该反应的离子方程式______________________________ ;
(3)写出F→G反应的化学方程式_________________________________ ,设计实验证明溶液G中含有
____________________________________________________________________ 。

已知E是形成酸雨的主要气体,请回答:
(1)A的组成元素为
(2)C溶液可溶解铜片,写出该反应的离子方程式
(3)写出F→G反应的化学方程式

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】利用以下装置完成下列实验(图中a、b、c、d 为止水夹)。

(1)仪器乙的名称_________ 。
(2)装置 A、B、D 相连,可证明 SO2在水中的溶解度,相关操作依次是:制取 SO2,收集 SO2, 关闭止水夹 b、d,打开止水夹 c,_____________ ,
(3)若烧杯中有大量水倒吸入丙试管中,说明 SO2 易溶于水。 装置 A、C 相连,可用于证明C、Si 的非金属性强弱,则试剂甲是_____________ ,C 中 的 现 象 是____________ 。

(1)仪器乙的名称
(2)装置 A、B、D 相连,可证明 SO2在水中的溶解度,相关操作依次是:制取 SO2,收集 SO2, 关闭止水夹 b、d,打开止水夹 c,
(3)若烧杯中有大量水倒吸入丙试管中,说明 SO2 易溶于水。 装置 A、C 相连,可用于证明C、Si 的非金属性强弱,则试剂甲是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验。

(1)甲装置中发生的主要反应的化学方程式是_________________________________________ ,
该反应中若有6.4gCu参加反应,则被还原的H2SO4的物质的量为_______________ mol。
(2)在装置乙的试管口放有一团浸有碱液的棉花,若棉花中碱液为氢氧化钠溶液,请写出棉花中发生反应的离子方程式:_________________________________________ 。
已知甲中生成的还原产物具有较强还原性,试书写其与盐酸酸化的FeCl3溶液反应的离子方程式:____________________________________________________ 。
(3)欲观察甲装置中生成CuSO4溶液的蓝色,应进行的操作是_______________________________ 。

(1)甲装置中发生的主要反应的化学方程式是
该反应中若有6.4gCu参加反应,则被还原的H2SO4的物质的量为
(2)在装置乙的试管口放有一团浸有碱液的棉花,若棉花中碱液为氢氧化钠溶液,请写出棉花中发生反应的离子方程式:
已知甲中生成的还原产物具有较强还原性,试书写其与盐酸酸化的FeCl3溶液反应的离子方程式:
(3)欲观察甲装置中生成CuSO4溶液的蓝色,应进行的操作是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
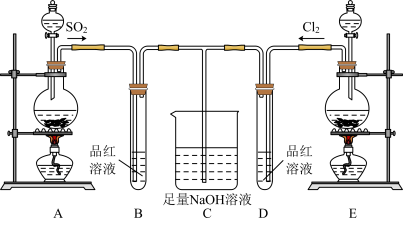
【推荐3】某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下实验装置:__ 。
(2)实验室可用装置E通过MnO2和浓盐酸反应制备Cl2,若有6molHCl参加反应,则转移电子的总数为___ 。
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象分别是:B__ ,D___ 。停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别是:B__ ,D__ 。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后漂白性肯定会更强。他们将制得的SO2和Cl2按物质的量之比为1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析产生该现象的原因:__ (用化学方程式表示)。
(2)实验室可用装置E通过MnO2和浓盐酸反应制备Cl2,若有6molHCl参加反应,则转移电子的总数为
(3)反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象分别是:B
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后漂白性肯定会更强。他们将制得的SO2和Cl2按物质的量之比为1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析产生该现象的原因:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】六种短周期元素在周期表中的相对位置如下所示,其中E元素原子核外电子总数是其最外层电子数的3倍。关于元素周期表及这六种元素性质,请回答:

(1)这六种元素的氢化物中,最稳定的是__________ .(写化学式);
(2)AC2的电子式为____________ .
(3)在一定条件下,由B单质与H2反应生成1 molG时,放出的热量为46.2 kJ,写出该反应的热化学方程式:____________________ .
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式_________________________ ,该反应中被氧化的G与参与反应的G的质量之比_________ .
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:_________ .

(1)这六种元素的氢化物中,最稳定的是
(2)AC2的电子式为
(3)在一定条件下,由B单质与H2反应生成1 molG时,放出的热量为46.2 kJ,写出该反应的热化学方程式:
(4)工业上用G检验输送氯气的管道是否漏气,可观察到大量白烟,同时有单质B生成,写出化学方程式
(5)F的单质可由其氧化物与氢化物反应生成,写出该反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】将过量的SO2分别通入下列溶液:①氢硫酸②溴水③品红溶液④澄清石灰水⑤酸性高锰酸钾⑥氯化钙溶液,根据要求填空。
(1)无明显现象的是_____________ ;
(2)溶液颜色褪去的是_____________ ;
(3)SO2作氧化剂的是________________ ;
(4)SO2作还原剂的是_______________ ;
(5)先生成沉淀然后沉淀溶解的是____________ ;
(6)有沉淀生成且沉淀不溶解的是______________ 。
(1)无明显现象的是
(2)溶液颜色褪去的是
(3)SO2作氧化剂的是
(4)SO2作还原剂的是
(5)先生成沉淀然后沉淀溶解的是
(6)有沉淀生成且沉淀不溶解的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】实验室可用如下图装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。
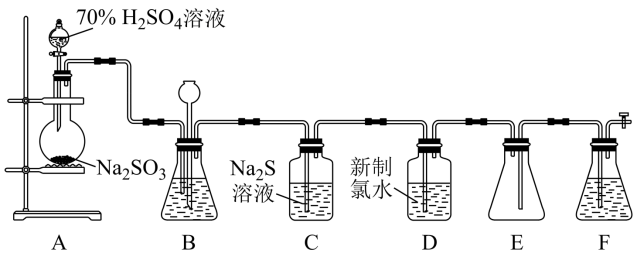
(1)盛装 仪器名称是
仪器名称是_______ 。
(2)装置B可以通过观察产生气泡的多少判断反应的快慢,最好盛装_______(填代号)。
(3)C装置可以验证 具有
具有_______ 性(选填“氧化性”、“还原性”),相关现象为_______ 。
(4)试管D中发生反应的离子方程式为_______ 。
(5)装置E的作用是_______ ,装置F中的试剂为_______ 溶液。
(6)煤燃烧会产生含 的废气,可以采用“钙基固硫法”解决。即将生石灰与含硫的煤混合后再燃烧,可以将生成的
的废气,可以采用“钙基固硫法”解决。即将生石灰与含硫的煤混合后再燃烧,可以将生成的 最终转化为
最终转化为 ,请写出该反应化学方程式
,请写出该反应化学方程式_______ 。
 并验证其性质。
并验证其性质。
(1)盛装
 仪器名称是
仪器名称是(2)装置B可以通过观察产生气泡的多少判断反应的快慢,最好盛装_______(填代号)。
| A.蒸馏水 | B.饱和NaCl溶液 | C.饱和NaOH溶液 | D.饱和 溶液 溶液 |
 具有
具有(4)试管D中发生反应的离子方程式为
(5)装置E的作用是
(6)煤燃烧会产生含
 的废气,可以采用“钙基固硫法”解决。即将生石灰与含硫的煤混合后再燃烧,可以将生成的
的废气,可以采用“钙基固硫法”解决。即将生石灰与含硫的煤混合后再燃烧,可以将生成的 最终转化为
最终转化为 ,请写出该反应化学方程式
,请写出该反应化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某同学设计了如下装置用于制取 和验证
和验证 的漂白性、酸性、还原性。
的漂白性、酸性、还原性。

回答下列问题:
(1)装置A中发生反应的化学方程式为___________ 。
(2)在框图内选择合适装置依次验证 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→___________ (填装置字母,还原性设计两个装置)。
(3)装置D中发生反应的离子方程式为___________ 。
(4)实验前必须鼓入 ,目的是
,目的是___________ 。
(5)装置F中产生了白色沉淀,其成分是___________ (化学式),分析F中产生白色沉淀原因___________ 。
 和验证
和验证 的漂白性、酸性、还原性。
的漂白性、酸性、还原性。
回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)在框图内选择合适装置依次验证
 的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→
的漂白性、酸性、还原性,上述各装置按气流从左到右方向连接顺序为A→(3)装置D中发生反应的离子方程式为
(4)实验前必须鼓入
 ,目的是
,目的是(5)装置F中产生了白色沉淀,其成分是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某同学为了测定某生铁(仅含C、 )中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.
)中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.

回答下列问题:
(1)仪器a的名称为________ ,仪器e的名称为________ ;
(2)B装置的作用为________ ,D装置的作用为________ ;
(3)点燃酒精灯,A装置中发生的反应化学方程式为_______________ 、_________________
(4)待 生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重
生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重 ,则生铁中铁的质量分数为
,则生铁中铁的质量分数为________ (用含m、b的表达式表示);
(5)利用该装置测得实验结果不够准确,改良的方法为____________________ 。
 )中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.
)中铁的质量分数,设计了如图所示的实验装置(夹持仪器已省略)和实验方案进行实验探究.
回答下列问题:
(1)仪器a的名称为
(2)B装置的作用为
(3)点燃酒精灯,A装置中发生的反应化学方程式为
(4)待
 生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重
生铁完全溶解后,停止加热,拆下装置E并称重.若装置E增重 ,则生铁中铁的质量分数为
,则生铁中铁的质量分数为(5)利用该装置测得实验结果不够准确,改良的方法为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
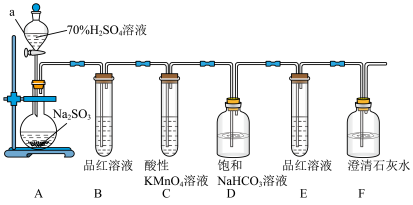
【推荐3】某化学兴趣小组对有关SO2性质进行如下探究活动。___________ ,装置A中发生反应的化学方程式为___________ 。
(2)①B中品红溶液褪色,是因为SO2具有___________ (填“氧化”“还原”或“漂白”,下同)性,C装置中酸性KMnO4溶液褪色,表明SO2具有___________ 性。
②证明亚硫酸酸性比碳酸酸性强的实验现象是___________ ;
③若将SO2气体直接通入澄清石灰水中,溶液变浑浊,则该反应的离子方程式为___________ 。
(2)①B中品红溶液褪色,是因为SO2具有
②证明亚硫酸酸性比碳酸酸性强的实验现象是
③若将SO2气体直接通入澄清石灰水中,溶液变浑浊,则该反应的离子方程式为
您最近一年使用:0次



