 、
、 、
、 都是重要的有机反应中间体,下列说法不正确的是
都是重要的有机反应中间体,下列说法不正确的是A.碳原子均采取 杂化 杂化 | B. 中所有原子共面 中所有原子共面 |
C. 的空间结构为三角锥形 的空间结构为三角锥形 | D. 和 和 结合可得到 结合可得到 |
更新时间:2021-02-19 08:28:08
|
【知识点】 利用杂化轨道理论判断分子的空间构型解读
相似题推荐
单选题
|
较易
(0.85)
【推荐1】制取H2O2的反应为Na2O2+H2SO4+10H2O=Na2SO4·10H2O+H2O2,下列说法正确的是
A.Na+的结构示意图为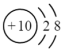 |
B. 的空间结构为正四面体形 的空间结构为正四面体形 |
C.H2O2的电子式为 |
| D.H2O2中O原子的杂化轨道类型为sp2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】氢氰酸(HCN)作为一种重要的精细化工原料,随着医药、染料和农药等相关行业的发展,其下游产品的研究和生产取得了较快的进展。HCN分子中所有原子都通过化学键而达到稳定结构,则下列有关HCN的说法中正确的是
A.结构式: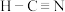 | B.电子式: |
C.中心原子是 杂化 杂化 | D.1个分子中含有4个σ键 |
您最近一年使用:0次

 BaS+ 4CO↑,BaS + 2HCl = BaCl2 + H2S↑。下列说法正确的是
BaS+ 4CO↑,BaS + 2HCl = BaCl2 + H2S↑。下列说法正确的是
 的空间构型是平面正方形
的空间构型是平面正方形

