一定温度下,金属硫化物的沉淀溶解平衡曲线如图所示。纵轴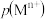 表示
表示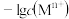 ,横轴
,横轴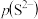 表示
表示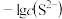 ,下列说法错误的是
,下列说法错误的是
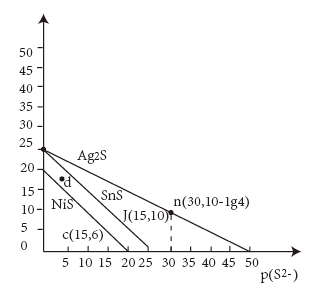
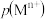 表示
表示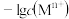 ,横轴
,横轴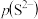 表示
表示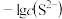 ,下列说法错误的是
,下列说法错误的是
A.该温度下, 的 的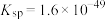 |
B. 点表示该温度下 点表示该温度下 的不饱和溶液 的不饱和溶液 |
C.该温度下, 和 和 的饱和溶液中 的饱和溶液中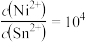 |
D.向含有等物质的量浓度的 、 、 、 、 溶液中加入饱和 溶液中加入饱和 溶液,析出沉淀的先后顺序为 溶液,析出沉淀的先后顺序为 、 、 、 、 |
更新时间:2021-03-09 11:37:40
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】t ℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是
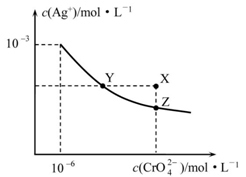

| A.在t ℃时,Ag2CrO4的Ksp=1×10-9 |
| B.X点有Ag2CrO4沉淀生成 |
| C.通过加热蒸发可以使溶液由Y点变到Z点 |
| D.在饱和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y点变到X点最终变到Z点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关难溶电解质的溶解平衡的说法中正确的是
| A.向AgCl悬浊液中加水,平衡右移,c(Ag+)和c(Cl-)均增大 |
B.Ca(OH)2悬浊液存在平衡: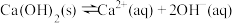 ,升温,溶液碱性增强 ,升温,溶液碱性增强 |
| C.向盛有2 mL0.1 mol/LAgNO3溶液的试管中滴加几滴0.1 mol/LNaCl溶液,再向其中滴加0.001 mol/LNaI溶液,先观察到白色沉淀,后又产生黄色沉淀,说明Ksp(AgCl)>Ksp(AgI) |
D.将0.001 mol/LAgNO3溶液滴入含有同浓度KCl和K2CrO4的混合溶液中,先产生AgCl沉淀[ , , ] ] |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化学与生产生活密切相关,下列叙述错误的是
| A.用K2FeO4处理自来水,既可以杀菌消毒又可净水 |
| B.泡沫灭火器内玻璃筒盛碳酸氢钠溶液,铁筒盛硫酸铝溶液 |
| C.使用含氟牙膏预防龋齿利用了沉淀转化的原理 |
| D.处理锅炉水垢时,先用饱和Na2CO3溶液浸泡,后加盐酸除去 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | Na2S有强还原性 | 用于除去废水中的Cu2+和Hg2+ |
| B | CaCO3是难溶物 | CaCl2溶液中通入CO2产生白色沉淀 |
| C | 浓H2SO4有强氧化性 | 浓H2SO4可用于干燥SO2 |
| D | Zn具有还原性和导电性 | 可用作锌锰干电池的负极材料 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小。已知p(Ag)=-lgc(Ag+),p(X)=-lgc(X-),利用p(X)、p(Ag)的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系。下列说法错误的是


| A.E线是AgCl的溶解平衡曲线 |
| B.坐标点p形成的溶液是AgCl的不饱和溶液 |
| C.m点是在水中加入足量的AgBr形成的饱和溶液 |
| D.n点表示由过量的KI与AgNO3反应产生AgI沉淀 |
您最近一年使用:0次

 的沉淀溶解平衡曲线如图所示.下列说法正确的是
的沉淀溶解平衡曲线如图所示.下列说法正确的是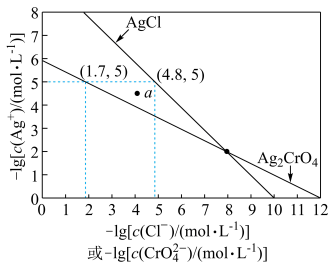
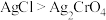
 沉淀,不能生成AgCl沉淀
沉淀,不能生成AgCl沉淀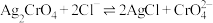 的平衡常数
的平衡常数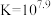
 均为
均为 的混合溶液中滴加
的混合溶液中滴加 溶液,先产生
溶液,先产生

