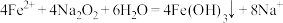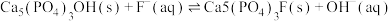某温度时,卤化银(AgX,X=Cl,Br,I)的3条溶解平衡曲线如图所示,AgCl、AgBr、AgI的Ksp依次减小。已知p(Ag)=-lgc(Ag+),p(X)=-lgc(X-),利用p(X)、p(Ag)的坐标系可表示出AgX的溶度积与溶液中的c(Ag+)和c(X-)的相互关系。下列说法错误的是


| A.E线是AgCl的溶解平衡曲线 |
| B.坐标点p形成的溶液是AgCl的不饱和溶液 |
| C.m点是在水中加入足量的AgBr形成的饱和溶液 |
| D.n点表示由过量的KI与AgNO3反应产生AgI沉淀 |
2022高三·全国·专题练习 查看更多[1]
(已下线)秘籍16 电解质溶液微粒变化及图象分析-备战2022年高考化学抢分秘籍(全国通用)
更新时间:2022-04-24 19:19:17
|
相似题推荐
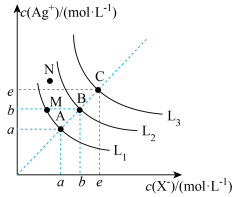
【推荐1】25℃时,卤化银(AgX,X=Cl、Br、I)在水中的沉淀溶解平衡曲线如图所示,AgCl、AgBr、AgI的 数据见下表(已知
数据见下表(已知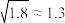 、
、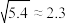 、
、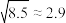 )。下列说法错误的是
)。下列说法错误的是
 数据见下表(已知
数据见下表(已知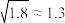 、
、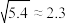 、
、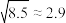 )。下列说法错误的是
)。下列说法错误的是| 化学式 |  |  |  |
| 溶度积 |  |  | 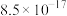 |

| A.N点为AgBr的饱和溶液 |
| B.L1、L2、L3分别为AgI、AgBr、AgCl的沉淀溶解平衡曲线 |
C.向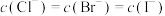 的混合溶液中滴入AgNO3溶液时,先生成AgI沉淀 的混合溶液中滴入AgNO3溶液时,先生成AgI沉淀 |
D.M点为AgX的饱和溶液,此时M点对应的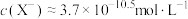 |
您最近一年使用:0次
【推荐2】已知pAg+=-lgc(Ag+),Px-=-lgc(X-)。某温度下,AgBr、AgCl在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是


| A.a和c两点的Kw不同 |
B. |
| C.向饱和AgCl溶液中加入NaCl固体,可使a点变到d点 |
D. 平衡常数 平衡常数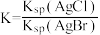 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】弱碱性条件下,利用含砷氧化铜矿(含CuO、As2O3及少量不溶性杂质)制备Cu2(OH)2SO4的工艺流程如图:

下列说法不正确 的是

下列说法
A.“氨浸”时As2O3发生的离子反应为:As2O3+6NH3+3H2O=6 + 2 + 2 |
| B.“氨浸”时CuO转化为[Cu(NH3)4]2+ |
C.“氧化除 ”时每生成1 mol FeAsO4,转移的电子数目为6.02×1023 ”时每生成1 mol FeAsO4,转移的电子数目为6.02×1023 |
D.“蒸氨”后滤液中主要存在的离子为: 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
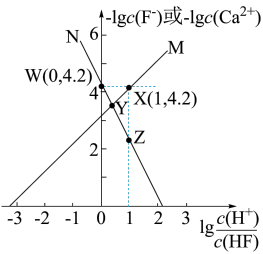
【推荐2】难溶盐 可溶于盐酸,常温下,用
可溶于盐酸,常温下,用 气体调节
气体调节 浊液的
浊液的 ,测得体系中
,测得体系中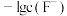 或
或 与
与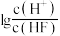 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
 可溶于盐酸,常温下,用
可溶于盐酸,常温下,用 气体调节
气体调节 浊液的
浊液的 ,测得体系中
,测得体系中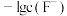 或
或 与
与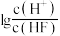 的关系如图所示。下列说法不正确的是
的关系如图所示。下列说法不正确的是
A.曲线 代表 代表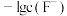 随 随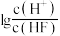 的变化趋势 的变化趋势 |
B. 点溶液中存在 点溶液中存在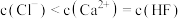 |
C.难溶盐 的溶度积常数 的溶度积常数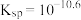 |
D.其他条件不变的情况下,无论增大 浓度或减小 浓度或减小 浓度, 浓度, 的 的 均不变 均不变 |
您最近一年使用:0次
【推荐1】下列实验装置或操作不正确的是
| A | B | C | D |
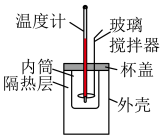 |  | 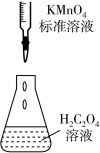 | 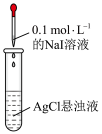 |
| 测定中和反应的反应热 | 验证铁的吸氧腐蚀 | 测定 溶液的浓度 溶液的浓度 | 比较 和 和 的大小 的大小 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列变化不可用沉淀溶解平衡原理解释是( )
| A.氢氧化亚铁浊液在空气中放置变红褐色 |
B.除去水垢中的 要加入 要加入 |
C.溶洞形成的过程中 与 与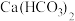 之间的转化 之间的转化 |
| D.含氟牙膏的使用降低了龋齿的发生率 |
您最近一年使用:0次

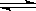 CuS(s)+Mn2+(aq),下列说法正确的是
CuS(s)+Mn2+(aq),下列说法正确的是 溶于铵盐溶液的原因,进行如下实验:
溶于铵盐溶液的原因,进行如下实验:
 溶液中滴加1
溶液中滴加1 溶液,另一份中逐滴加入4
溶液,另一份中逐滴加入4 溶液(pH≈7),边滴加边测定其中沉淀的量,沉淀的量与铵盐溶液的体积的关系如图。
溶液(pH≈7),边滴加边测定其中沉淀的量,沉淀的量与铵盐溶液的体积的关系如图。


 比
比 贡献更大
贡献更大 通入苯酚钠
通入苯酚钠 溶液:
溶液:
 溶液中加入
溶液中加入 :
: