现有五种元素,其中A、B、C为短周期主族元素,D、E为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题:
(1)已知BA5为离子化合物,写出其电子式:_______ 。
(2)B基态原子中能量最高的电子,其电子云在空间有_______ 个方向,原子轨道呈_______ 形。
(3)某同学根据上述信息,推断C的基态原子的核外电子排布图为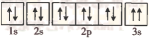 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了__ 。
(4)E位于_______ 族_______ 区,价电子排布式为_______ 。
(5)检验D元素的方法是_______ ,请用原子结构的知识解释产生此现象的原因是_______ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数s电子数少1 |
| C元素原子最外层有2个电子 |
| D是前四周期中电负性最小的元素 |
| E在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C的基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(4)E位于
(5)检验D元素的方法是
更新时间:2021-03-17 16:45:20
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】已知A、B、C、D、E为元素周期表中前四周期元素,且原子序数依次增大,A是短周期中原子半径最大的元素,B元素 能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E元素位于元素周期表的第11列。
能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E元素位于元素周期表的第11列。
试回答下列有关的问题:
(1)写出基态D原子的价层电子排布式:_______ ,E元素在元素周期表的位置:_______ 。
(2)画出A、B、C中第一电离能最大的元素的原子结构式意图,_______ ;这三种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时, 由大到小的顺序是
由大到小的顺序是_______ (写化学式)。
(3)D可形成化合物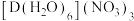 。
。
①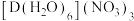 中配位体的
中配位体的 模型名称是
模型名称是_______ 。该化合物中阴离子的中心原子的轨道杂化类型为_______ 。
②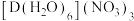 中
中 的键角
的键角_______ 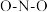 的键角(填“
的键角(填“ ”、
”、 ”、“
”、“ ”),原因是
”),原因是_______ 。
(4)已知B、C两种元素形成的化合物通常有两种。这两种化合物中_______ (填化学式)为非极性分子,另一种化合物的电子式为_______ 。
(5)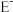 离子能与
离子能与 离子形成
离子形成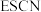 沉淀、
沉淀、 离子对应的酸有硫氰酸(
离子对应的酸有硫氰酸(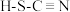 )和异硫氰酸(
)和异硫氰酸(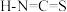 ),这两种酸沸点更高的是
),这两种酸沸点更高的是_______ (填名称),原因是_______ 。
 能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E元素位于元素周期表的第11列。
能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E元素位于元素周期表的第11列。试回答下列有关的问题:
(1)写出基态D原子的价层电子排布式:
(2)画出A、B、C中第一电离能最大的元素的原子结构式意图,
 由大到小的顺序是
由大到小的顺序是(3)D可形成化合物
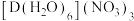 。
。①
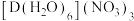 中配位体的
中配位体的 模型名称是
模型名称是②
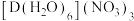 中
中 的键角
的键角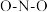 的键角(填“
的键角(填“ ”、
”、 ”、“
”、“ ”),原因是
”),原因是(4)已知B、C两种元素形成的化合物通常有两种。这两种化合物中
(5)
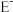 离子能与
离子能与 离子形成
离子形成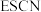 沉淀、
沉淀、 离子对应的酸有硫氰酸(
离子对应的酸有硫氰酸(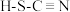 )和异硫氰酸(
)和异硫氰酸(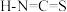 ),这两种酸沸点更高的是
),这两种酸沸点更高的是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】现有X、Y、Z、T四种短周期元素,原子序数依次增大。请根据下列相关信息,回答问题。
(1) Z2X4分子中Z原子采取________ 杂化,写出与之互为等电子体的有机物的结构简式_____________________
(2) Cl2T分子的空间构型___________ , Z2T的电子式_________________
(3) 请用价层电子对互斥理论解释ZX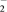 和ZX3的键角∠XZX的大小:
和ZX3的键角∠XZX的大小:_____________ 。
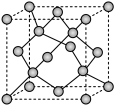
(4) Y晶体的晶胞如图所示,该晶胞含有______ 个Y原子,若晶胞的密度为d g·cm-3,阿伏加 德罗常数的值为NA(mol-1),则晶胞参数为a=_______ pm。(用含d 、NA的式子表示)
| 元素 | 相关信息 |
| X | 原子的1s轨道上只有1个电子 |
| Y | 原子的L层上s电子数等于p电子数 |
| Z | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的 |
| T | 负二价的元素T的氢化物在通常情况下是一种液体,且T的质量分数为88.9% |
(1) Z2X4分子中Z原子采取
(2) Cl2T分子的空间构型
(3) 请用价层电子对互斥理论解释ZX
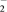 和ZX3的键角∠XZX的大小:
和ZX3的键角∠XZX的大小:(4) Y晶体的晶胞如图所示,该晶胞含有

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)元素F简单离子的价电子排布式为___________ ;写出元素G在周期表中的位置___________ 。
(2)B与氢元素形成的简单气态氢化物的空间构型为___________ ,C与氢元素形成的简单气态氢化物的VSEPR模型为___________ 。
(3)C、D、E三种元素的简单离子半径由大到小的顺序为___________ (用元素符号表示)。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为___________ 。
(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ 化合物(填“离子”或“共价”);M的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为___________ 。
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: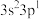 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)B与氢元素形成的简单气态氢化物的空间构型为
(3)C、D、E三种元素的简单离子半径由大到小的顺序为
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO
 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】钛被称为继铁、铝之后的第三金属。钙钛矿是一类氧化物陶瓷材料,典型代表是 晶体,是工业获取钛的重要原料。
晶体,是工业获取钛的重要原料。
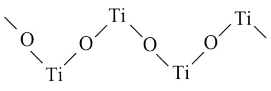
(1)基态钛原子的价层电子排布式为______ ,其原子核外共有______ 种运动状态不同的电子。
(2)六氟合钛酸钾(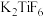 )中存在
)中存在 配离子,其中钛元素的化合价是
配离子,其中钛元素的化合价是______ ,配体是______ 。
(3)硫酸氧钛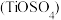 晶体中阳离子为链状聚合形式的离子,结构如图所示,则该阳离子的化学式为
晶体中阳离子为链状聚合形式的离子,结构如图所示,则该阳离子的化学式为______ ,阴离子中心原子的杂化轨道类型为______ 。
(4) 晶体结构如图,已知该晶体晶胞参数为anm,则与
晶体结构如图,已知该晶体晶胞参数为anm,则与 紧邻的O个数为
紧邻的O个数为______ ,O与O间的最短距离为______  。
。
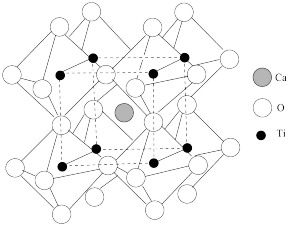
(5)钨青铜( )是一类色彩丰富的非整比化合物,其晶体结构与上述
)是一类色彩丰富的非整比化合物,其晶体结构与上述 晶体结构相同,若
晶体结构相同,若 无空缺,化学式为
无空缺,化学式为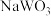 ,完全空缺则为
,完全空缺则为 ,每填入1个
,每填入1个 ,相应有1个
,相应有1个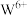 还原为
还原为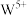 。
。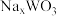 的颜色与x值的对应关系如图所示,已知某钨青铜晶体中
的颜色与x值的对应关系如图所示,已知某钨青铜晶体中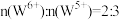 ,则其颜色为
,则其颜色为______ 色。
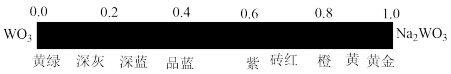
 晶体,是工业获取钛的重要原料。
晶体,是工业获取钛的重要原料。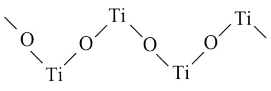
(1)基态钛原子的价层电子排布式为
(2)六氟合钛酸钾(
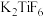 )中存在
)中存在 配离子,其中钛元素的化合价是
配离子,其中钛元素的化合价是(3)硫酸氧钛
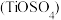 晶体中阳离子为链状聚合形式的离子,结构如图所示,则该阳离子的化学式为
晶体中阳离子为链状聚合形式的离子,结构如图所示,则该阳离子的化学式为(4)
 晶体结构如图,已知该晶体晶胞参数为anm,则与
晶体结构如图,已知该晶体晶胞参数为anm,则与 紧邻的O个数为
紧邻的O个数为 。
。
(5)钨青铜(
 )是一类色彩丰富的非整比化合物,其晶体结构与上述
)是一类色彩丰富的非整比化合物,其晶体结构与上述 晶体结构相同,若
晶体结构相同,若 无空缺,化学式为
无空缺,化学式为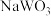 ,完全空缺则为
,完全空缺则为 ,每填入1个
,每填入1个 ,相应有1个
,相应有1个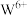 还原为
还原为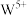 。
。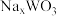 的颜色与x值的对应关系如图所示,已知某钨青铜晶体中
的颜色与x值的对应关系如图所示,已知某钨青铜晶体中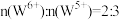 ,则其颜色为
,则其颜色为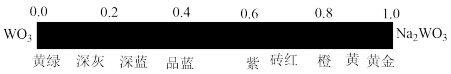
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】铬是人体必需的微量元素,对维持人体正常的生理功能有着重要的作用。铬是胰岛素不可缺少的辅助成分,它参与糖代谢过程,能够促进脂肪和蛋白质的合成,对于人体的生长发育起着积极的促进作用。虽然铬对维护人体健康有着十分重要的作用,但食用不当也会带来很大的危害。由于无机铬很不容易被人体所吸收,铬只有以有机化合物的形式进入人体内才能被吸收。而在铬的化合物中,六价铬具有很强的毒性,尤以铬酸盐和重铬酸盐的毒性最为突出。
(1)铬原子的基态电子排布式为_______ ,该元素在周期表中的位置是_______ 。
(2)氯化铬酰(CrO2Cl2)常温下为暗红色液体,熔点-96.5°C、 沸点117°C,能与丙酮(CH3COCH3)、CCl4、CS2等互溶。
①丙酮中碳原子采取的杂化方式为_______ ;
②CS2属于_______ (填“极性”或“非极性”)分子。
(3)CrCl3·6H2O(相对分子质量为266.5)有多种不同颜色的异构体(均是配合物,配位数为6)。为测定蒸发CrCl3溶液析出的暗绿色晶体是哪种异构体,取2.665g CrCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀1.435g。该异构体为_______ (填化学式)。 下列是暗绿色晶体配离子的空间结构(中心原子位于正八面体的中心,已省去),其中B与_______ 具有完全相同的结构。(填字母)
A.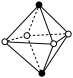 B.
B. C.
C. 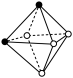 D.
D.  E.
E.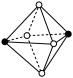
(4)六价铬的化合物有剧毒,所以要对Cr(VI)(罗马数字表示元素的化合价,下同)废水进行化学处理,使其转化为毒性较低的Cr(III)。最常见的是铁氧磁体法,即把FeSO4·7H2O(M=278g ·mol-1 )加入含CrO3的废水中,在pH<4时,Fe2+将Cr(VI)还原为Cr(III), 调节溶液pH达8~10,使溶液中的Fe(II)、 Fe(III)、Cr(III)析出组成相当于Fe(II)[Fex(III)·Cr2-x(III)]O4(磁性材料铁氧体的组成)沉淀。试回答:
①根据上述结果可确定铁氧磁体中x=_______ ;
②根据①的结果,在pH<4时,加入FeSO4·7H2O的质量至少是废水中CrO3质量的_______ 倍。
(1)铬原子的基态电子排布式为
(2)氯化铬酰(CrO2Cl2)常温下为暗红色液体,熔点-96.5°C、 沸点117°C,能与丙酮(CH3COCH3)、CCl4、CS2等互溶。
①丙酮中碳原子采取的杂化方式为
②CS2属于
(3)CrCl3·6H2O(相对分子质量为266.5)有多种不同颜色的异构体(均是配合物,配位数为6)。为测定蒸发CrCl3溶液析出的暗绿色晶体是哪种异构体,取2.665g CrCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀1.435g。该异构体为
A.
 B.
B. C.
C.  D.
D.  E.
E.
(4)六价铬的化合物有剧毒,所以要对Cr(VI)(罗马数字表示元素的化合价,下同)废水进行化学处理,使其转化为毒性较低的Cr(III)。最常见的是铁氧磁体法,即把FeSO4·7H2O(M=278g ·mol-1 )加入含CrO3的废水中,在pH<4时,Fe2+将Cr(VI)还原为Cr(III), 调节溶液pH达8~10,使溶液中的Fe(II)、 Fe(III)、Cr(III)析出组成相当于Fe(II)[Fex(III)·Cr2-x(III)]O4(磁性材料铁氧体的组成)沉淀。试回答:
①根据上述结果可确定铁氧磁体中x=
②根据①的结果,在pH<4时,加入FeSO4·7H2O的质量至少是废水中CrO3质量的
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】钴(Co)在合金工业、催化剂,颜料等方面有重要应用,某湿法炼锌工厂废弃钴渣的成分主要有: 、
、 、
、 ,一种富集钻的工艺流程如图所示:
,一种富集钻的工艺流程如图所示:

(1)Co的价层电子排布式为_______ , 的结构简式如图所示,则Co的配位数为
的结构简式如图所示,则Co的配位数为_______ 。
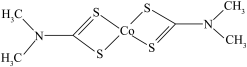
(2) 中Fe的化合价为
中Fe的化合价为_______ ,“酸浸”需要控制溶液的pH值不能过高,其原因是_______ 。
(3)煅烧时产生的气体成分为 、
、_______ 、_______ 。
(4)“烧渣”的主要成分为 ,写出“还原浸出”时的离子方程式:
,写出“还原浸出”时的离子方程式:_______ 。
(5)“氧化沉钴”时氧化剂和还原剂的物质的量之比为_______ 。
(6)一种掺钴催化剂的晶胞如图所示,则该晶体沿z轴的投影图为_______ (填序号),设阿伏加德罗常数的值为_______  ,晶胞参数为a nm,则该晶胞的密度为
,晶胞参数为a nm,则该晶胞的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。

A. B.
B. C.
C.
 、
、 、
、 ,一种富集钻的工艺流程如图所示:
,一种富集钻的工艺流程如图所示:
(1)Co的价层电子排布式为
 的结构简式如图所示,则Co的配位数为
的结构简式如图所示,则Co的配位数为
(2)
 中Fe的化合价为
中Fe的化合价为(3)煅烧时产生的气体成分为
 、
、(4)“烧渣”的主要成分为
 ,写出“还原浸出”时的离子方程式:
,写出“还原浸出”时的离子方程式:(5)“氧化沉钴”时氧化剂和还原剂的物质的量之比为
(6)一种掺钴催化剂的晶胞如图所示,则该晶体沿z轴的投影图为
 ,晶胞参数为a nm,则该晶胞的密度为
,晶胞参数为a nm,则该晶胞的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
A.
 B.
B. C.
C.
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】钒基笼目金属在超导电性方面有广阔的应用前最。某钒基笼目金属(M)的晶体结构如图所示。
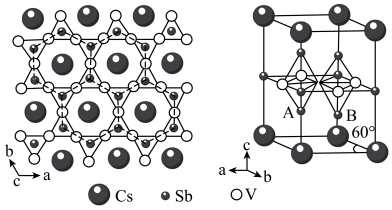
(1)Sb在元素周期表中的位置是___________ 。
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为___________ 。
(3)钒化合物在药物化学及催化化学等领域应用广泛。基态钒原子的价电子排布图为___________ ,钒有+2、+3、+4、+5等多种化合价,其中最稳定的化合价是_________ , 的空间结构为
的空间结构为________ 。
(4)SbH3的键角比NH3的键角小,原因是___________ 。
(5)该钒基笼目金属(M)的化学式为___________ ,与V原子距离最近且等距的V原子________ 个。
(6)已知,该晶胞中距离最近的两个V原子间的距离为2.75 Å,则晶胞体内A、B原子之间的距离为___________ Å ( ≈1.73, 保留两位小数)。
≈1.73, 保留两位小数)。

(1)Sb在元素周期表中的位置是
(2)基态V原子的价电子中,未成对电子数与成对电子数之比为
(3)钒化合物在药物化学及催化化学等领域应用广泛。基态钒原子的价电子排布图为
 的空间结构为
的空间结构为(4)SbH3的键角比NH3的键角小,原因是
(5)该钒基笼目金属(M)的化学式为
(6)已知,该晶胞中距离最近的两个V原子间的距离为2.75 Å,则晶胞体内A、B原子之间的距离为
 ≈1.73, 保留两位小数)。
≈1.73, 保留两位小数)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】铁及铁的化合物在生产、生活中有广泛应用。请回答下列问题:
(1) 结构示意图如图1。
结构示意图如图1。

① 的价层电子轨道表示式为
的价层电子轨道表示式为_______ ; 的配体是
的配体是_______ ,配位数是_______ 。
② 中H—O—H键角
中H—O—H键角_______  中O—S—O键角(填“大于”、“小于”或“等于”),原因是
中O—S—O键角(填“大于”、“小于”或“等于”),原因是_______ 。
③ 中
中 与
与 、
、 与
与 的作用力类型分别
的作用力类型分别_______ 。
(2) 晶体的晶胞形状为立方体,边长为a nm,结构如图2。
晶体的晶胞形状为立方体,边长为a nm,结构如图2。
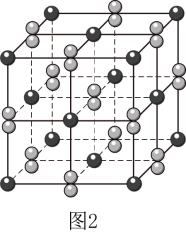
晶胞中 的个数为
的个数为_______ ;该晶体的密度为_______  。(阿伏伽德罗常数为
。(阿伏伽德罗常数为 )
)
(3)应用于合成氨反应的催化剂(铁)的表面上存在氮原子,图3为氮原子在铁的晶面上的单层附着局部示意图。则图中铁颗粒表面上氮原子与铁原子的个数比为_______ 。
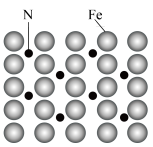
(1)
 结构示意图如图1。
结构示意图如图1。
①
 的价层电子轨道表示式为
的价层电子轨道表示式为 的配体是
的配体是②
 中H—O—H键角
中H—O—H键角 中O—S—O键角(填“大于”、“小于”或“等于”),原因是
中O—S—O键角(填“大于”、“小于”或“等于”),原因是③
 中
中 与
与 、
、 与
与 的作用力类型分别
的作用力类型分别(2)
 晶体的晶胞形状为立方体,边长为a nm,结构如图2。
晶体的晶胞形状为立方体,边长为a nm,结构如图2。
晶胞中
 的个数为
的个数为 。(阿伏伽德罗常数为
。(阿伏伽德罗常数为 )
)(3)应用于合成氨反应的催化剂(铁)的表面上存在氮原子,图3为氮原子在铁的晶面上的单层附着局部示意图。则图中铁颗粒表面上氮原子与铁原子的个数比为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】废锂离子电池正极材料中含有大量镍、钴,通过分选、硫酸浸出、除杂净化等工序,可以回收钴、镍。由镍钴渣料(主要成分为 、NiO(OH)、
、NiO(OH)、 、CoO(OH)、CuO、
、CoO(OH)、CuO、 )回收镍、钴流程如图:
)回收镍、钴流程如图:

已知:①二价镍、钴和二价杂质离子易溶于低浓度硫酸中,而三价镍、钴较难直接溶出。
② 开始沉淀pH为3.6沉淀完全pH为4.2,
开始沉淀pH为3.6沉淀完全pH为4.2, 开始沉淀pH为4.4沉淀完全pH为6.4
开始沉淀pH为4.4沉淀完全pH为6.4
(1)在一段浸出液中存在的金属阳离子为___________ 。
(2)氨水调pH时发生的离子方程式为___________ 。
(3)在二段酸浸中过氧化氢做___________ (氧化剂或还原剂),NiO(OH)发生的反应化学方程式为________ 。
NiO(OH)+___________+___________=___________ +___________+___________。
+___________+___________。
(4)在二段酸浸过程中需要加热,温度对钴镍浸出率的影响如图所示,该反应的最佳反应温度为___________ ,温度过高或过低会对该反应造成什么影响?___________ 。

(5)①一种钴的氧化物的晶胞结构如图所示,该氧化物中钴离子的价电子轨道表示式为___________ 。
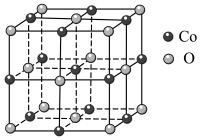
②该氧化物中氧离子的配位数是___________ 。
③设NA为阿佛伽德罗常数的值,晶胞密度为d ,该晶体中距离最近的两个钴原子之间的距离为
,该晶体中距离最近的两个钴原子之间的距离为___________ pm。
 、NiO(OH)、
、NiO(OH)、 、CoO(OH)、CuO、
、CoO(OH)、CuO、 )回收镍、钴流程如图:
)回收镍、钴流程如图:
已知:①二价镍、钴和二价杂质离子易溶于低浓度硫酸中,而三价镍、钴较难直接溶出。
②
 开始沉淀pH为3.6沉淀完全pH为4.2,
开始沉淀pH为3.6沉淀完全pH为4.2, 开始沉淀pH为4.4沉淀完全pH为6.4
开始沉淀pH为4.4沉淀完全pH为6.4(1)在一段浸出液中存在的金属阳离子为
(2)氨水调pH时发生的离子方程式为
(3)在二段酸浸中过氧化氢做
NiO(OH)+___________+___________=___________
 +___________+___________。
+___________+___________。(4)在二段酸浸过程中需要加热,温度对钴镍浸出率的影响如图所示,该反应的最佳反应温度为

(5)①一种钴的氧化物的晶胞结构如图所示,该氧化物中钴离子的价电子轨道表示式为

②该氧化物中氧离子的配位数是
③设NA为阿佛伽德罗常数的值,晶胞密度为d
 ,该晶体中距离最近的两个钴原子之间的距离为
,该晶体中距离最近的两个钴原子之间的距离为
您最近一年使用:0次



