硫酸高铈[Ce(SO4)2]可用作氧化还原反应的滴定剂。实验室要配制220mL0.1mol·L-1Ce(SO4)2溶液。回答下列问题:
(1)应该用托盘天平称取Ce(SO4)2·4H2O晶体质量为___ g。
(2)配制溶液所需仪器除烧杯、量筒、玻璃棒、胶头滴管外,还必须用到的一种玻璃仪器为___ ,在使用该仪器前必须进行的操作是___ 。
(3)试判断下列操作对配制溶液物质的量浓度的影响(填“偏高”“偏低”或“不变”)。
①定容时俯视刻度线___ 。
②转移前,容量瓶内有蒸馏水___ 。
③定容时水加多了用胶头滴管吸出___ 。
(4)取20mL一定浓度的FeSO4溶液于锥形瓶中,当滴入30.00mL0.1mol·L-1Ce(SO4)2溶液(铈被还原为Ce3+)时,FeSO4恰好完全反应,FeSO4溶液的物质的量浓度是___ mol·L-1。
(1)应该用托盘天平称取Ce(SO4)2·4H2O晶体质量为
(2)配制溶液所需仪器除烧杯、量筒、玻璃棒、胶头滴管外,还必须用到的一种玻璃仪器为
(3)试判断下列操作对配制溶液物质的量浓度的影响(填“偏高”“偏低”或“不变”)。
①定容时俯视刻度线
②转移前,容量瓶内有蒸馏水
③定容时水加多了用胶头滴管吸出
(4)取20mL一定浓度的FeSO4溶液于锥形瓶中,当滴入30.00mL0.1mol·L-1Ce(SO4)2溶液(铈被还原为Ce3+)时,FeSO4恰好完全反应,FeSO4溶液的物质的量浓度是
20-21高一下·安徽·开学考试 查看更多[4]
河南省名校联盟2020-2021学年高一上学期1月联考化学试题(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点03 物质的量的浓度及溶液配制-备战2022年高考化学一轮复习考点帮(全国通用)安徽省江淮名校2020-2021学年高一下学期开学联考化学试题
更新时间:2021-01-31 15:36:53
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】大气污染越来越成为人们关注的问题,烟气中的NOx必须脱除(即脱硝)后才能排放,脱硝的方法有多种。完成下列填空:

Ⅰ直接脱硝
(1)NO在催化剂作用下分解为氮气和氧气。在10 L密闭容器中,NO经直接脱硝反应时,其物质的量变化如图所示。则0~5min内氧气的平均反应速率为_______ mol/(L·min)。
Ⅱ臭氧脱硝
(2)O3氧化NO结合水洗可完全转化为HNO3,此时O3与NO的物质的量之比为_____ 。
Ⅲ氨气脱硝
(3)实验室制取纯净的氨气,除了氯化铵外,还需要_______ 、_______ (填写试剂名称)。不使用碳酸铵的原因是_______________________________ (用化学方程式表示)。吸收氨气时,常使用防倒吸装置,下列装置不能达到此目的的是________ 。

NH3脱除烟气中NO的原理如下图:

(4)该脱硝原理中,NO最终转化为________ (填化学式)和H2O。当消耗1mol NH3和0.25mol O2时,除去的NO在标准状况下的体积为______ L。

Ⅰ直接脱硝
(1)NO在催化剂作用下分解为氮气和氧气。在10 L密闭容器中,NO经直接脱硝反应时,其物质的量变化如图所示。则0~5min内氧气的平均反应速率为
Ⅱ臭氧脱硝
(2)O3氧化NO结合水洗可完全转化为HNO3,此时O3与NO的物质的量之比为
Ⅲ氨气脱硝
(3)实验室制取纯净的氨气,除了氯化铵外,还需要

NH3脱除烟气中NO的原理如下图:

(4)该脱硝原理中,NO最终转化为
您最近一年使用:0次
【推荐2】Mg在CO2中燃烧的反应可用于火星电站发电、人员取暖等,反应的化学方程式为2Mg+CO2 2MgO+C。
2MgO+C。
(1)做氧化剂的物质是________ ,碳元素的化合价_______ (填“升高”或“降低”)。
(2)反应中每生成1 mol MgO,消耗Mg的物质的量是______ mol,转移电子的物质的量是_____ mol。
 2MgO+C。
2MgO+C。(1)做氧化剂的物质是
(2)反应中每生成1 mol MgO,消耗Mg的物质的量是
您最近一年使用:0次
【推荐3】第ⅢA元素也称为硼族元素,除硼外其余均为金属元素。硼的应用非常广泛,可用于原子反应堆和高温技术,甚至可用来制作火箭中所用的某些结构材料。
(1)硼元素位于元素周期表第__________ 周期。铝与氢氧化钠溶液反应的离子方程式为_________________________ 。
(2)氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂(主要成分为Na2B4O7·10H2O)为起始物,经过一系列反应可以得到BN、B和BF3等。

①反应a的化学方程式为________ ,为了加快反应a的化学反应速率可采取的措施有_____________ (回答一条即可)。
②生成BN的化学反应_________ (填“是”或“不是”)氧化还原反应。
③由B2O3制硼时所得到的产品不纯,主要含有的杂质为____________ 。
(3)有一类硼烷形似鸟巢,故称为巢式硼烷,如下有三种巢式硼烷的结构:
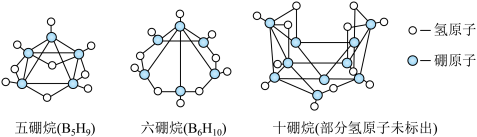
①根据五硼烷和六硼烷的化学式,推测十硼烷的化学式为_____________ 。
②已知:B6H10+O2→B2O3+H2O(未配平),每1 mol B6H10完全燃烧时转移__________ mol电子。
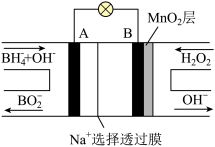
(4)NaBH4被称为“万能还原剂”,近年来常用NaBH4与过氧化氢构建一种新型碱性电池,如图所示;则该电池放电时的负极反应式为___________ ,正极附近溶液的pH会___________ 。(填“增大”、“减小”或“不变”)。
(1)硼元素位于元素周期表第
(2)氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂(主要成分为Na2B4O7·10H2O)为起始物,经过一系列反应可以得到BN、B和BF3等。

①反应a的化学方程式为
②生成BN的化学反应
③由B2O3制硼时所得到的产品不纯,主要含有的杂质为
(3)有一类硼烷形似鸟巢,故称为巢式硼烷,如下有三种巢式硼烷的结构:

①根据五硼烷和六硼烷的化学式,推测十硼烷的化学式为
②已知:B6H10+O2→B2O3+H2O(未配平),每1 mol B6H10完全燃烧时转移
(4)NaBH4被称为“万能还原剂”,近年来常用NaBH4与过氧化氢构建一种新型碱性电池,如图所示;则该电池放电时的负极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。现用该浓硫酸配制450mL 1mol/L的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。

请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有______ (选填序号),还缺少的仪器有______ (写仪器名称);
(2)经计算,配制上述稀硫酸时需要用量筒量取上述浓硫酸的体积为______ mL(保留一位小数)。
(3)接下来的操作是将上述所取浓硫酸进行稀释,稀释的操作是__________________ 。
(4)在溶液配制过程中,下列操作会引起所配置硫酸的浓度偏低的有_________ (填序号)
A.用量筒量取浓硫酸读数时仰视刻度线;
B.转移稀释的硫酸溶液后未洗涤烧杯和玻璃棒;
C.浓硫酸稀释后未经冷却即转移到容量瓶中;
D.容量瓶未干燥就用来配置溶液;
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平;
F.定容时仰视刻度线。

请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有
(2)经计算,配制上述稀硫酸时需要用量筒量取上述浓硫酸的体积为
(3)接下来的操作是将上述所取浓硫酸进行稀释,稀释的操作是
(4)在溶液配制过程中,下列操作会引起所配置硫酸的浓度偏低的有
A.用量筒量取浓硫酸读数时仰视刻度线;
B.转移稀释的硫酸溶液后未洗涤烧杯和玻璃棒;
C.浓硫酸稀释后未经冷却即转移到容量瓶中;
D.容量瓶未干燥就用来配置溶液;
E.定容后摇匀溶液,发现液面低于刻度线,再加入少量水使液面与刻度线相平;
F.定容时仰视刻度线。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 是一种重要的消毒剂,在日常生活中应用广泛。
是一种重要的消毒剂,在日常生活中应用广泛。
(1) 在水溶液中的电离方程式是
在水溶液中的电离方程式是_______ 。
(2)使用 溶液时经常滴加稀硫酸,目的是
溶液时经常滴加稀硫酸,目的是_______ 。
(3)实验室中要配制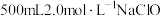 溶液。
溶液。
①实验中用到的玻璃仪器是烧杯、玻璃棒、_______ ;
②配制溶液的过程中一些操作如下图所示:
关于上述操作的说法正确的是_______ 。
A.溶解 固体的操作如图①所示
固体的操作如图①所示
B.定容时的操作如图②所示
C.定容时的操作可用图③表示
D.定容时向容量瓶内加蒸馏水至接近刻度线 时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
(4)下列操作能使所配制溶液浓度偏低的是_______。
(5)洁厕灵(主要成分是盐酸)与“84”消毒液混合使用发生下列反应: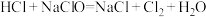 ,该反应的氧化剂是
,该反应的氧化剂是______ ,反应过程中生成标准状况下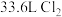 ,转移电子数是
,转移电子数是_____ 。
 是一种重要的消毒剂,在日常生活中应用广泛。
是一种重要的消毒剂,在日常生活中应用广泛。(1)
 在水溶液中的电离方程式是
在水溶液中的电离方程式是(2)使用
 溶液时经常滴加稀硫酸,目的是
溶液时经常滴加稀硫酸,目的是(3)实验室中要配制
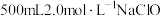 溶液。
溶液。①实验中用到的玻璃仪器是烧杯、玻璃棒、
②配制溶液的过程中一些操作如下图所示:
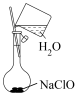 | 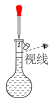 | 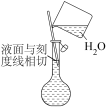 |
| ① | ② | ③ |
A.溶解
 固体的操作如图①所示
固体的操作如图①所示B.定容时的操作如图②所示
C.定容时的操作可用图③表示
D.定容时向容量瓶内加蒸馏水至接近刻度线
 时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切(4)下列操作能使所配制溶液浓度偏低的是_______。
| A.称量固体时物码反放 | B.使用的容量瓶不干燥 |
| C.称量时使用有油污的砝码 | D.定容摇匀后液面下降又加水 |
(5)洁厕灵(主要成分是盐酸)与“84”消毒液混合使用发生下列反应:
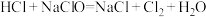 ,该反应的氧化剂是
,该反应的氧化剂是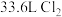 ,转移电子数是
,转移电子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】我国具有5000年文化,文物是活的历史,某博物馆修复出土铁器包括:检测锈蚀产物—分析腐蚀原理—脱氯—形成保护层等过程。
(1)锈蚀产物的主要成分为 、
、 、
、 、FeO(OH)、FeOCl,铁元素化合价全部为+3的物质有
、FeO(OH)、FeOCl,铁元素化合价全部为+3的物质有___________ 。检验FeOCl中存在铁元素的方法是:把FeOCl溶于___________ 、再向其中加入___________ ,观察到红色。
(2)研究发现,出土文物 保护层被
保护层被 氧化为FeO(OH)而引起腐蚀。该过程化学方程式为
氧化为FeO(OH)而引起腐蚀。该过程化学方程式为___________ 。
(3)利用在NaOH溶液中,溶解度FeOCl大于FeO(OH),对固体FeOCl进行脱氯,离子方程式为___________ 。若配制480ml 0.5mol/LNaOH溶液必须用到的仪器有天平、量筒、药匙、烧杯、玻璃棒,还有___________ 、___________ ,应用天平称出___________ g NaOH。
(4)用 把脱氯产物FeO(OH)还原为
把脱氯产物FeO(OH)还原为 ,生成
,生成 需要
需要___________  。
。
(1)锈蚀产物的主要成分为
 、
、 、
、 、FeO(OH)、FeOCl,铁元素化合价全部为+3的物质有
、FeO(OH)、FeOCl,铁元素化合价全部为+3的物质有(2)研究发现,出土文物
 保护层被
保护层被 氧化为FeO(OH)而引起腐蚀。该过程化学方程式为
氧化为FeO(OH)而引起腐蚀。该过程化学方程式为(3)利用在NaOH溶液中,溶解度FeOCl大于FeO(OH),对固体FeOCl进行脱氯,离子方程式为
(4)用
 把脱氯产物FeO(OH)还原为
把脱氯产物FeO(OH)还原为 ,生成
,生成 需要
需要 。
。
您最近一年使用:0次



