根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色 | 还原性:Br->Cl- |
| B | 室温下,将pH相等的HA和HB两种一元酸稀释相同倍数,测得HA的pH比HB的小 | 酸性:HA>HB |
| C | 向久置的FeSO4溶液中滴加KSCN,溶液变红 | FeSO4溶液全部被氧化 |
| D | 向Na2CO3溶液中滴加浓盐酸,反应产生的气体直接通入Na2SiO3溶液中,溶液变浑浊 | 非金属性: C>Si |
| A.A | B.B | C.C | D.D |
更新时间:2021-03-29 13:37:30
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列有关溶液的说法中,正确的是
| A.(NH4)2SO4溶液浓缩时温度过高可能导致生成NH4HSO4 |
| B.相同温度下,强酸溶液的导电能力一定大于弱酸溶液 |
| C.通电时,溶液中溶质粒子分别向两极移动 |
| D.蒸干Na2CO3溶液最终得到NaOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列是某同学学习相关知识后总结的规律,其中错误的是
A.Zn、Fe、Cu单质活泼性依次减弱, 、 、 、 、 氧化性依次增强 氧化性依次增强 |
B.一定温度下,一元弱酸HA的 越小,则NaA的 越小,则NaA的 越大 越大 |
C.电解时, 、 、 、 、 放电能力依次减弱, 放电能力依次减弱, 、 、 、 、 氧化性依次增强 氧化性依次增强 |
| D.元素的电负性越大,该原子的第一电离能越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】分析下表提供的数据,下列说法正确的是
化学式 | 电离常数 |
HClO |  |
H2CO3 |  |
 |
| A.84消毒液(有效成分为NaClO)能杀菌的原因:2ClO-+H2O+CO2→2HClO+CO32- |
| B.25℃时,0.1 mol/L NaClO的pH大于0.1 mol/LNaHCO3的pH |
| C.25℃时,0.1 mol/L NaClO的pH大于0.1 mol/L Na2CO3 的pH |
| D.0.1 mol/L NaClO和0.1 mol/L NaHCO3溶液中:c(ClO-)>c(HCO3-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】2023年4月《中华人民共和国黄河保护法》正式实施,保护黄河健康是生态保护事业的重要使命。下列有关说法错误的是
| A.冬春季节冰凌漂浮在黄河水面上与氢键的形成有关 |
B.使用FeS固体除去工业污水中 、 、 等重金属离子,减少对黄河水污染 等重金属离子,减少对黄河水污染 |
| C.水厂处理黄河水制取自来水,可用明矾消毒 |
D.黄河口大闸蟹配食醋味更美,1mol 含有4mol H 含有4mol H |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:25 ℃时,Mg(OH)2的Ksp=5.61×10−12,MgF2的Ksp=7.42×10−11。下列判断不正确的是
| A.25 ℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)较小。 |
| B.25 ℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大。 |
| C.25 ℃时,Mg(OH)2固体在20 mL 0.01 mol∙L−1的氨水中的Ksp与在20 mL 0.01 mol∙L−1 NH4Cl溶液中的Ksp相同,但前者的溶解度比后者小。 |
| D.25 ℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2。 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据下列实验操作和现象所得出的结论错误的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状炭,并放出有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| B | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe3+的水解平衡正向移动 |
| C | 铝片先用砂纸打磨,再加入到浓硝酸中 | 无明显现象 | 浓硝酸具有强氧化性,常温下,铝被浓硝酸钝化 |
| D | 向等浓度的KCl、KI混合液中逐滴滴加AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向含有MgCO3固体的溶液中滴加少许浓盐酸(忽略体积变化)。下列数值变小的是
| A.c(H+) | B.c(CO32-) | C.MgCO3溶解度 | D.Ksp(MgCO3) |
您最近一年使用:0次

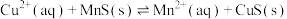 ,下列说法正确的是
,下列说法正确的是 比CuS的
比CuS的
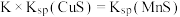
 固体后,
固体后, 减小,
减小, 增大
增大 Fe(SCN)3+3KCl的溶液中加入少量KCl固体
Fe(SCN)3+3KCl的溶液中加入少量KCl固体

