(1)在新疆与青海两省交界处有一狭长山谷,当地牧民经常遇到在风和日丽的晴天顷刻间电闪雷鸣,狂风大作,人畜皆遭雷击而倒毙。奇怪的是这里牧草茂盛,四季长青,被当地牧民称为“魔鬼谷”。请用化学方程式表示“魔鬼谷”牧草茂盛,四季长青的原因:
①___ ;②___ ;③___ 。
(2)治理汽车尾气含有CO、NO等多种污染物,已成为城市空气的主要污染源,现有一种治理方法是用使NO与CO在催化剂的表面发生反应,生成两种无污染的物质,请写出该反应的化学方程式:___ 。
①
(2)治理汽车尾气含有CO、NO等多种污染物,已成为城市空气的主要污染源,现有一种治理方法是用使NO与CO在催化剂的表面发生反应,生成两种无污染的物质,请写出该反应的化学方程式:
更新时间:2021-03-31 14:03:38
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
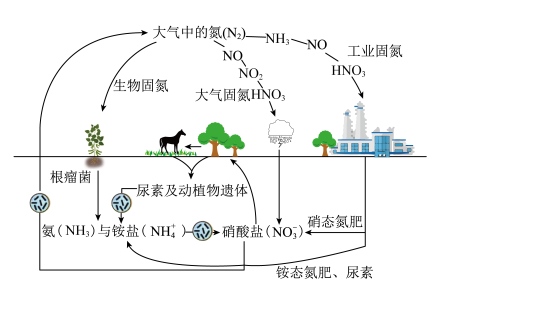
【推荐1】一定条件下,含氮元素的物质可发生如图所示的循环转化。

回答下列问题:
(1)写出铵根离子的电子式为_________ 。
(2)图中属于“氮的固定”的是_________ (填字母,下同);转化过程中发生非氧化还原反应的是_________ 。
(3)若“反应h”是在NO2与H2O的作用下实现,则该反应中氧化产物与还原产物的物质的量之比为_________
(4)若“反应i”是在酸性条件下由 与Zn的作用实现,则该反应的离子方程式为
与Zn的作用实现,则该反应的离子方程式为________

回答下列问题:
(1)写出铵根离子的电子式为
(2)图中属于“氮的固定”的是
(3)若“反应h”是在NO2与H2O的作用下实现,则该反应中氧化产物与还原产物的物质的量之比为
(4)若“反应i”是在酸性条件下由
 与Zn的作用实现,则该反应的离子方程式为
与Zn的作用实现,则该反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】自然界由于存在氮循环而使空气中的氮气含量保持相对稳定:
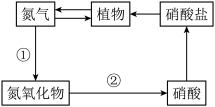
请回答下列问题:
(1)反应①的化学方程式为________ 。
(2)合成氨也叫人工固氮,化学方程式为_______ 。
(3)常见氮肥有NH4HCO3、NH4NO3、NH4Cl、CO(NH2)2,含氮量最高的是___ 。

请回答下列问题:
(1)反应①的化学方程式为
(2)合成氨也叫人工固氮,化学方程式为
(3)常见氮肥有NH4HCO3、NH4NO3、NH4Cl、CO(NH2)2,含氮量最高的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】NO是一种剧毒气体,但近年来发现许多生物体组织中存在少量NO,它有扩张血管、免疫、增强记忆的功能,因而成为当前生命科学的研究热点。
(1)写出自然界形成NO的化学方程式:_______ 。
(2)NO在大气层中可发生反应:①NO+O3→NO2+O,②NO2+O=NO+O2。上述反应①中,NO是_______ 剂,上述反应②中,NO是_______ 产物;整个过程中的总反应方程式为_______ ,整个过程中NO所起的作用是_______ 。
(3)为了消除NO对环境的污染,根据氧化还原反应原理,可选用NH3使NO转化为两种无毒气体(其中之一是水蒸气),该反应需要催化剂参加,其化学方程式为_______ 。
(1)写出自然界形成NO的化学方程式:
(2)NO在大气层中可发生反应:①NO+O3→NO2+O,②NO2+O=NO+O2。上述反应①中,NO是
(3)为了消除NO对环境的污染,根据氧化还原反应原理,可选用NH3使NO转化为两种无毒气体(其中之一是水蒸气),该反应需要催化剂参加,其化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】完成有关化学方程式:
(1)NO与O2 反应___________ 。
(2)NO2与水反应___________ 。
(3)Cu与稀硝酸反应___________ 。
(1)NO与O2 反应
(2)NO2与水反应
(3)Cu与稀硝酸反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此必须对含有氮氧化物的废气进行处理。
(1)用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
在反应①中,氧化剂是_________ ,还原剂是______________ 。
在反应②中,氧化剂和还原剂的物质的量之比为_________________ 。
(2)汽车尾气中含有CO和NO,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成N2和CO2,该反应的化学方程式为_____________ 。
(3)在一定条件下NH3亦可用来将氮氧化物转化为无污染的物质。写出NH3和NO2在一定条件下反应的化学方程式:_______________________ 。
(1)用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
在反应①中,氧化剂是
在反应②中,氧化剂和还原剂的物质的量之比为
(2)汽车尾气中含有CO和NO,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成N2和CO2,该反应的化学方程式为
(3)在一定条件下NH3亦可用来将氮氧化物转化为无污染的物质。写出NH3和NO2在一定条件下反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】目前地球环境污染问题越来越严重,如温室效应、臭氧层破坏、烟雾事件、酸雨的形成、有毒物质的污染等已成为目前世界各国人民普遍关心的问题。请回答下列问题:
(1)产生温室效应的原因主要是大气中含有_________
(2)臭氧层的破坏导致紫外线对地球表面辐射量增加,从而使全球皮肤癌的发病人数明显增加。造成这一现象的主要原因是______
(3)在20世纪60年代,一些工业发达国家的城市都发生过烟雾事件,并造成数以千计的人死亡。造成这一现象的主要原因是______
(1)产生温室效应的原因主要是大气中含有_________
| A.SO2 | B.NO2 | C.CO2 | D.CO |
| A.人们大量使用氟氯代烷 |
| B.人们在炼钢时向空气中排放了大量的高炉煤气 |
| C.石油炼制厂排放了大量的甲烷.氢气 |
| D.硫酸、硝酸工厂排放了大量的二氧化硫和一氧化氮 |
| A.汽油的不完全燃烧 | B.大量使用了农药化肥 |
| C.白色塑料垃圾的漂浮 | D.金属矿物的冶炼 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】氮氧化物会严重污染大气,所以实验室必须对含有氮氧化物的废气进行处理。用NaOH溶液可以吸收废气中的氮氧化物,反应方程式如下:
①NO+NO2+2NaOH=2NaNO2+H2O
②2NO2+2NaOH=NaNO2+NaNO3+H2O
(1)在反应①中,参加反应的氧化剂和还原剂的质量之比为___________ 。
(2)在反应②中,氧化产物是___________ ,还原产物是___________ (填化学式)。
(3)在反应①②中,参加反应的NaOH均为2mol时,两个反应转移电子数的关系是①___________ ②(填“ ”、“
”、“ ”或“
”或“ ”)
”)
(4)自来水中的NO 危害人类健康。为了降低自来水中NO
危害人类健康。为了降低自来水中NO 的浓度,某研究人员提出两种方案。
的浓度,某研究人员提出两种方案。
①方案a:微碱性条件下,用Fe(OH)2还原NO ,产物之一是NH3。生成3.4gNH3的同时会生成
,产物之一是NH3。生成3.4gNH3的同时会生成______ mol Fe(OH)3。
②方案b:碱性条件下,用Al粉还原NO ,产物之一是N2。发生的反应如下所示,配平离子方程式并用单线桥标出电子转移的方向和数目:
,产物之一是N2。发生的反应如下所示,配平离子方程式并用单线桥标出电子转移的方向和数目:___________ 。
Al+ NO +OH-—AlO
+OH-—AlO +N2↑+H2O
+N2↑+H2O
①NO+NO2+2NaOH=2NaNO2+H2O
②2NO2+2NaOH=NaNO2+NaNO3+H2O
(1)在反应①中,参加反应的氧化剂和还原剂的质量之比为
(2)在反应②中,氧化产物是
(3)在反应①②中,参加反应的NaOH均为2mol时,两个反应转移电子数的关系是①
 ”、“
”、“ ”或“
”或“ ”)
”)(4)自来水中的NO
 危害人类健康。为了降低自来水中NO
危害人类健康。为了降低自来水中NO 的浓度,某研究人员提出两种方案。
的浓度,某研究人员提出两种方案。①方案a:微碱性条件下,用Fe(OH)2还原NO
 ,产物之一是NH3。生成3.4gNH3的同时会生成
,产物之一是NH3。生成3.4gNH3的同时会生成②方案b:碱性条件下,用Al粉还原NO
 ,产物之一是N2。发生的反应如下所示,配平离子方程式并用单线桥标出电子转移的方向和数目:
,产物之一是N2。发生的反应如下所示,配平离子方程式并用单线桥标出电子转移的方向和数目:Al+ NO
 +OH-—AlO
+OH-—AlO +N2↑+H2O
+N2↑+H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】如图所示,将一瓶充满NO2气体的试管倒扣在水槽中,气体颜色由___________ 逐渐变为___________ 色,试管内的液面会逐渐________ ,当反应停止后向试管中缓慢通入氧气,气体颜色又由_______ 色逐渐变为______ 色,之后又变为_______ 色,试管内的液面会______ ,用化学方程式表示试管中发生的化学反应___________ 。
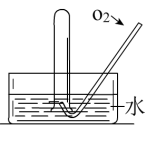

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】I.如图所示:在B水槽中装有500 mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B水槽的水中。充分反应后,试管A中余下气体的体积为0.5a mL。
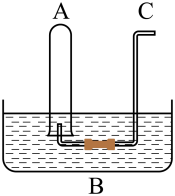
(1)通过导气管C向余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是___________ 。
(2)当试管A中充满气体时停止通入氧气,然后将试管取出水槽,水槽B中溶液的物质的量浓度为___________ mol/L(设溶液的体积仍为500 mL,答案用分数表示)。
Ⅱ.向 溶液中通入
溶液中通入 后,将溶液分置于两支试管中。向一份溶液中通入
后,将溶液分置于两支试管中。向一份溶液中通入 ,出现白色沉淀A;另一份通入少量
,出现白色沉淀A;另一份通入少量 ,产生白色沉淀B.试回答下列问题:
,产生白色沉淀B.试回答下列问题:
(3)沉淀A的化学式为___________ ,该沉淀能否溶于稀盐酸?___________ (填“能”或“不能”)。
(4)写出通入少量 ,生成沉淀B的离子方程式:
,生成沉淀B的离子方程式:___________ ,生成2.33 g沉淀B,理论上需要消耗标准状况下的
___________  。
。
(5)若将 溶液换成
溶液换成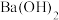 溶液,少量
溶液,少量 通入
通入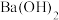 溶液中的离子方程式为
溶液中的离子方程式为___________ 。
Ⅲ.完成下列问题
(6)2.0 g铜镁合金完全溶解于100 mL密度为1.4 g/mL质量分数为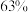 的浓硝酸溶液中,得到NO2和N2O4(NO2和
的浓硝酸溶液中,得到NO2和N2O4(NO2和 均为浓F溶液的还原产物
均为浓F溶液的还原产物 的混合气体1792 mL (标况
的混合气体1792 mL (标况 ,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为
,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为___________ ,加入NaOH溶液的体积为___________ mL。
(7)某分子筛类催化剂(H+交换沸石)催化NH3脱除NO、NO2的反应机理如图所示。
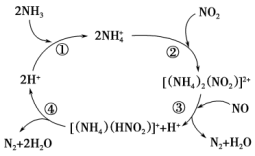
按如图反应机理,NH3脱除NO、NO2总反应的化学方程式是___________ 。
(8)室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不支持燃烧。则a、b、c的等量关系是___________ 。
(9)下列二组混合气体体积比为①NO2∶O2=1∶1;②NH3∶O2=2∶1,将分别盛满上述各种气体的试管倒置于盛有水的水槽中,最后两试管内溶液浓度之比为___________ (忽略溶质扩散)。
(10)将充满NO2和O2混合气体的量筒倒置于水中,充分反应后,保持气体压强不变,水进入至量筒体积的 处停止了,则原混合气体中NO2和O2的体积之比是
处停止了,则原混合气体中NO2和O2的体积之比是___________ 。

(1)通过导气管C向余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是
(2)当试管A中充满气体时停止通入氧气,然后将试管取出水槽,水槽B中溶液的物质的量浓度为
Ⅱ.向
 溶液中通入
溶液中通入 后,将溶液分置于两支试管中。向一份溶液中通入
后,将溶液分置于两支试管中。向一份溶液中通入 ,出现白色沉淀A;另一份通入少量
,出现白色沉淀A;另一份通入少量 ,产生白色沉淀B.试回答下列问题:
,产生白色沉淀B.试回答下列问题:(3)沉淀A的化学式为
(4)写出通入少量
 ,生成沉淀B的离子方程式:
,生成沉淀B的离子方程式:
 。
。(5)若将
 溶液换成
溶液换成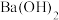 溶液,少量
溶液,少量 通入
通入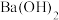 溶液中的离子方程式为
溶液中的离子方程式为Ⅲ.完成下列问题
(6)2.0 g铜镁合金完全溶解于100 mL密度为1.4 g/mL质量分数为
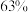 的浓硝酸溶液中,得到NO2和N2O4(NO2和
的浓硝酸溶液中,得到NO2和N2O4(NO2和 均为浓F溶液的还原产物
均为浓F溶液的还原产物 的混合气体1792 mL (标况
的混合气体1792 mL (标况 ,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为
,向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀,得到3.7g沉淀。则合金中铜与镁的物质的量之比为(7)某分子筛类催化剂(H+交换沸石)催化NH3脱除NO、NO2的反应机理如图所示。

按如图反应机理,NH3脱除NO、NO2总反应的化学方程式是
(8)室温时,在容积为a mL的试管中充满NO2气体,然后倒置在水中到管内水面不再上升时为止;再通入b mL O2,则管内液面又继续上升,测得试管内最后剩余气体为c mL,且该气体不支持燃烧。则a、b、c的等量关系是
(9)下列二组混合气体体积比为①NO2∶O2=1∶1;②NH3∶O2=2∶1,将分别盛满上述各种气体的试管倒置于盛有水的水槽中,最后两试管内溶液浓度之比为
(10)将充满NO2和O2混合气体的量筒倒置于水中,充分反应后,保持气体压强不变,水进入至量筒体积的
 处停止了,则原混合气体中NO2和O2的体积之比是
处停止了,则原混合气体中NO2和O2的体积之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
A B
B C
C D
D
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是_______ 。
②在工业生产中,B气体的大量排放被雨水吸收后形成了_______ 而污染环境。
(2)若A在常温下为气体,C是红棕色的气体。
①A、C的化学式分别是:A_______ ;C_______ 。
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式:_______ 。该反应_______ (填“属于”或“不属于”)氧化还原反应。
A
 B
B C
C D
D(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是
②在工业生产中,B气体的大量排放被雨水吸收后形成了
(2)若A在常温下为气体,C是红棕色的气体。
①A、C的化学式分别是:A
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式:
您最近一年使用:0次

 过程中还需要添加的物质是
过程中还需要添加的物质是 )可通过硝化细菌转化为硝酸盐(
)可通过硝化细菌转化为硝酸盐( ),生成
),生成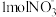 时转移
时转移 4NO+6H2O
4NO+6H2O

