将Mg、Cu组成的2.14g混合物投入适量稀硝酸中完全反应,并收集还原产物NO气体(还原产物只有一种)。然后向反应后的溶液中加入2mol·L-1NaOH溶液60mL时,金属恰好沉淀完全,形成沉淀质量为3.16g,则反应过程中收集到NO气体(标况下)体积为
| A.0.896L | B.0.448L | C.0.336L | D.0.224L |
更新时间:2021-04-21 20:34:12
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】x mol的铁铝合金完全溶于1L某稀硝酸后,生成了y mol的NO(无其他还原产物).则关于该反应的下列说法中,不正确的是( )
| A.在该反应中,硝酸既显氧化性,又显酸性 |
| B.根据题中所给条件,无法计算出硝酸的物质的量浓度 |
| C.参加反应的硝酸的物质的量为4y mol |
| D.若将生成的NO与O2混合溶于水被完全吸收,需标准状况下O2的体积是11.2y L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某浓度稀HNO3与金属M反应时,能得到+2价硝酸盐,反应时M与HNO3的物质的量之比为5 ∶12,则反应时HNO3的还原产物是 ( )
| A.NH4NO3 | B.N2 | C.N2O | D.NO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在通风橱中进行下列实验:
下列说法不正确的是
| 步骤 |
|
| |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| A.Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2=2NO2 |
| B.Ⅱ中的现象说明Fe表面形成致密的氧化膜,阻止Fe进一步反应 |
| C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 |
| D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.浓氨水中: 、 、 、 、 、 、 |
D.加入铝片能生成 的溶液: 的溶液: 、 、 、 、 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列由实验操作及现象得出的结论正确的是
A.向某溶液中加入硝酸酸化的 溶液,有白色沉淀生成,原溶液中一定含有 溶液,有白色沉淀生成,原溶液中一定含有 |
B.将碳与浓硝酸共热产生的气体通入少量澄清石灰水中,无明显现象,说明没有产生 |
C.向酸性 溶液中滴加足量 溶液中滴加足量 溶液, 溶液, 溶液褪色且有气泡产生,说明 溶液褪色且有气泡产生,说明 具有还原性 具有还原性 |
| D.过量铜与稀硝酸充分反应后,再滴加稀硫酸,铜逐渐溶解,说明铜可以和稀硫酸反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是
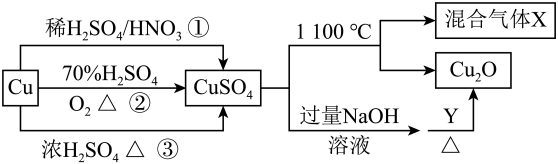

| A.途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 |
| B.相对于途径①、③,途径②更好地体现了绿色化学思想 |
| C.1mol CuSO4在1100℃所得混合气体X中O2可能为0.75mol |
| D.Y应该是一种还原剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】将100 mL稀硝酸和稀硫酸的混合酸溶液平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g铜粉(假设此时硝酸只被还原为NO,下同);向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示。则下列判断中错误的是


| A.OA段产生的气体是NO,BC段产生的气体是H2 |
| B.A点对应消耗NO3-物质的量为0.2 mol |
| C.B点对应消耗铁粉的质量为8.4 g |
| D.原混合酸溶液中H2SO4的浓度为4.0 mol·L-1 |
您最近一年使用:0次




 +H2O
+H2O

