在①HF、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 分子中:(填序号)
分子中:(填序号)
(1)以非极性键结合的非极性分子是___________ ;
(2)以极性键结合的具有直线形结构的非极性分子是___________ ;
(3)以极性键结合的具有正四面体形结构的非极性分子是___________ ;
(4)以极性键结合的具有三角锥形结构的极性分子是___________ ;
(5)以极性键结合的具有 杂化轨道和V形结构的分子是
杂化轨道和V形结构的分子是___________ ;
(6)以极性键结合的具有 杂化轨道结构的分子是
杂化轨道结构的分子是___________ 。
 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ 、⑦
、⑦ 分子中:(填序号)
分子中:(填序号)(1)以非极性键结合的非极性分子是
(2)以极性键结合的具有直线形结构的非极性分子是
(3)以极性键结合的具有正四面体形结构的非极性分子是
(4)以极性键结合的具有三角锥形结构的极性分子是
(5)以极性键结合的具有
 杂化轨道和V形结构的分子是
杂化轨道和V形结构的分子是(6)以极性键结合的具有
 杂化轨道结构的分子是
杂化轨道结构的分子是
更新时间:2021-04-26 08:36:55
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】Si(NH2)4分子的空间结构(以Si为中心)名称为________ ,分子中氮原子的杂化轨道类型是_______ 。Si(NH2)4受热分解生成Si3N4和NH3,其受热不稳定的原因是________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铬能形成多种配合物,许多铬的配合物都具有广泛用途。回答下列问题:
(1) 成为阳离子时首先失去的是
成为阳离子时首先失去的是_______ 轨道上的电子。
(2) 、
、 、C三种配合物的化学式和颜色如下:
、C三种配合物的化学式和颜色如下:
A.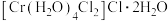 深绿色
深绿色
B.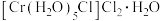 绿色
绿色
C.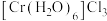 灰蓝色
灰蓝色
① 、
、 、
、 之间的关系是
之间的关系是_____ 。
②化合物 中与
中与 (Ⅲ)形成配位键的原子或离子是
(Ⅲ)形成配位键的原子或离子是_____ ,配位数为_____ 。
③相同物质的量的 、
、 、
、 分别与足量
分别与足量 溶液反应,生成
溶液反应,生成 的物质的量之比为
的物质的量之比为_____ 。
(3)Reineckesalt的结构如图所示。
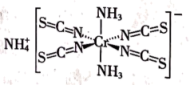
①阳离子的立体结构为_______ ; 的立体结构为
的立体结构为_____ 。
② 中碳原子的杂化方式为
中碳原子的杂化方式为_____ 。
(1)
 成为阳离子时首先失去的是
成为阳离子时首先失去的是(2)
 、
、 、C三种配合物的化学式和颜色如下:
、C三种配合物的化学式和颜色如下:A.
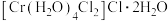 深绿色
深绿色B.
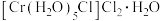 绿色
绿色C.
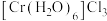 灰蓝色
灰蓝色①
 、
、 、
、 之间的关系是
之间的关系是②化合物
 中与
中与 (Ⅲ)形成配位键的原子或离子是
(Ⅲ)形成配位键的原子或离子是③相同物质的量的
 、
、 、
、 分别与足量
分别与足量 溶液反应,生成
溶液反应,生成 的物质的量之比为
的物质的量之比为(3)Reineckesalt的结构如图所示。

①阳离子的立体结构为
 的立体结构为
的立体结构为②
 中碳原子的杂化方式为
中碳原子的杂化方式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有下列微粒:①CH4;②CH2=CH2;③CH CH;④NH3;⑤NH
CH;④NH3;⑤NH ;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):
;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):
(1)呈正四面体的是_______ 。
(2)中心原子轨道为sp3杂化的是_______ ,为sp2杂化的是_______ ,为sp杂化的是_______ 。
(3)互为等电子体的一组是_______ 。
(4)为减少温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。若有1molCH4生成,则有_______ molσ键和_______ molπ键断裂。
 CH;④NH3;⑤NH
CH;④NH3;⑤NH ;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):
;⑥BF3;⑦P4;⑧H2O;⑨H2O2;填写下列空白(填序号):(1)呈正四面体的是
(2)中心原子轨道为sp3杂化的是
(3)互为等电子体的一组是
(4)为减少温室效应,科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中CO2。若有1molCH4生成,则有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)根据价层电子对互斥模型, 分子中心原子孤电子对数是
分子中心原子孤电子对数是_______ , 分子的空间构型是
分子的空间构型是_______ 。
(2)气态三氧化硫以单分子形式存在,属于_______ 分子(填“极性”、“非极性”),固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ 。
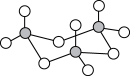
(3) 中心原子的价层电子对数为
中心原子的价层电子对数为_______ ,写出一个与 VEEPR模型相同的离子
VEEPR模型相同的离子_______ 。
(4)下列表述中,不能证明氯的非金属性比硫强的是_______ 。
A.气态氢化物的稳定性:
B.两元素的电负性: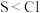
C.高价含氧酸的酸性: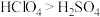
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应: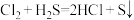
(1)根据价层电子对互斥模型,
 分子中心原子孤电子对数是
分子中心原子孤电子对数是 分子的空间构型是
分子的空间构型是(2)气态三氧化硫以单分子形式存在,属于

(3)
 中心原子的价层电子对数为
中心原子的价层电子对数为 VEEPR模型相同的离子
VEEPR模型相同的离子(4)下列表述中,不能证明氯的非金属性比硫强的是
A.气态氢化物的稳定性:

B.两元素的电负性:
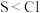
C.高价含氧酸的酸性:
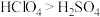
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:
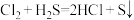
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题:
(1)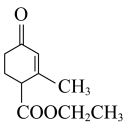 中含有的含氧官能团的名称为
中含有的含氧官能团的名称为___________ 。
(2)某有机物结构如图所示,下列说法正确的是___________ (填序号)。
③分子中C原子的杂化方式为 杂化 ④该分子是非极性分子
杂化 ④该分子是非极性分子
(3)TiO2是环境友好材料,能光催化降解有机物。纳米TiO2催化处理污水的一个实例如图所示。___________ ;化合物乙中有___________ 个手性碳原子。
(4)有A、B两种烃,已知:
( )B完全燃烧的产物
)B完全燃烧的产物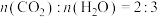 。
。
( )A是B分子中的氢原子全部被甲基取代后的产物;A遇
)A是B分子中的氢原子全部被甲基取代后的产物;A遇 的
的 溶液不褪色,其一氯代物只有一种。
溶液不褪色,其一氯代物只有一种。
①写出B与溴在光照下的反应方程式___________ (只写一取代)。
②A的结构简式为___________ ,系统命名为___________ 。
(1)
 中含有的含氧官能团的名称为
中含有的含氧官能团的名称为(2)某有机物结构如图所示,下列说法正确的是
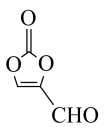
③分子中C原子的杂化方式为
 杂化 ④该分子是非极性分子
杂化 ④该分子是非极性分子(3)TiO2是环境友好材料,能光催化降解有机物。纳米TiO2催化处理污水的一个实例如图所示。

(4)有A、B两种烃,已知:
(
 )B完全燃烧的产物
)B完全燃烧的产物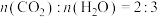 。
。(
 )A是B分子中的氢原子全部被甲基取代后的产物;A遇
)A是B分子中的氢原子全部被甲基取代后的产物;A遇 的
的 溶液不褪色,其一氯代物只有一种。
溶液不褪色,其一氯代物只有一种。①写出B与溴在光照下的反应方程式
②A的结构简式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】有下列粒子:①CH4 ②CH2 =CH2 ③CH≡CH ④NH3 ⑤NH4+ ⑥BF3 ⑦H2O。填写下列空白(填序号):
(1)呈正四面体的是__________
(2)中心原子轨道为 sp3 杂化的是__________ ,为 sp2 杂化的是__________ ,为 sp 杂化的是__________
(3)所有原子共平面的是__________
(4)粒子存在配位键的是__________
(5)含有极性键的极性分子的是__________
(1)呈正四面体的是
(2)中心原子轨道为 sp3 杂化的是
(3)所有原子共平面的是
(4)粒子存在配位键的是
(5)含有极性键的极性分子的是
您最近一年使用:0次



