有几种元素的粒子核外电子排布式均为1s22s22p63s23p6,其中:
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒的符号是___________ ;
(2)某微粒的盐溶液,能使溴水褪色,并出现浑浊,这种微粒的符号是___________ ;
(3)某微粒氧化性很弱,但得到电子后还原性很强,且这种原子有一个单电子,这种微粒的符号是___________ ;
(4)某微粒还原性虽弱,但失去电子后氧化性强,且这种元素的原子得到一个电子即达稳定结构,这种微粒的符号是___________ 。
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒的符号是
(2)某微粒的盐溶液,能使溴水褪色,并出现浑浊,这种微粒的符号是
(3)某微粒氧化性很弱,但得到电子后还原性很强,且这种原子有一个单电子,这种微粒的符号是
(4)某微粒还原性虽弱,但失去电子后氧化性强,且这种元素的原子得到一个电子即达稳定结构,这种微粒的符号是
更新时间:2021-05-20 19:03:10
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】储氢纳米碳管的研究成功体现了科技的进步,但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯其反应式为3C+2K2Cr2O7+8H2SO4=3CO2+2K2SO4+2Cr2(SO4)3+8H2O。
(1)氧化剂是____ ,氧化产物是____ 。
(2)H2SO4在上述发应中表现出来的性质是___ (填序号)。
a.氧化性 b.氧化性和酸性 c.酸性 d.还原性和酸性
(3)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为____ L。
(4)要使10mL0.5 mol∙L−1的K2Cr2O7溶液被还原,至少要加入___ mL2 mol∙L−1的H2SO4溶液。
(1)氧化剂是
(2)H2SO4在上述发应中表现出来的性质是
a.氧化性 b.氧化性和酸性 c.酸性 d.还原性和酸性
(3)若反应中电子转移了0.8mol,则产生的气体在标准状况下的体积为
(4)要使10mL0.5 mol∙L−1的K2Cr2O7溶液被还原,至少要加入
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C_______ 具有(填“氧化性”或“还原性”)。
(2)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中的还原产物是________ (写化学式),反应中每生成1个Cl2分子,转移电子的数目为________ 。
②用双线桥标出反应中电子转移的方向和数目_______ 。
③ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(ClO ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_______ 。
A.O2 B.FeCl2 C.KI D.KMnO4
(1)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C
(2)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中的还原产物是
②用双线桥标出反应中电子转移的方向和数目
③ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(ClO
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KI D.KMnO4
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】现有① ②
② ③
③ ④
④ ⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
(1)甲中有________ ;乙中有________ 。(填序号)
(2)由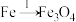 ,
,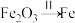 可知,欲实现I反应过程应从
可知,欲实现I反应过程应从________ (填“甲”或“乙”,下同)中找物质,欲实现Ⅱ反应过程应从________ 中找物质。
(3)请将下列6种物质: 、
、 、
、 、
、 、
、 、
、 (提示:能按
(提示:能按 ________+________→________+________+
________+________→________+________+ 形式反生化学反应)写出该反应对应的离子方式
形式反生化学反应)写出该反应对应的离子方式_______ ;并在离子方程式上标出电子转移的方向和数目______ 。
(4)一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为: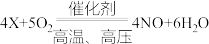 ,请推出X的化学式为
,请推出X的化学式为_____ 。
 ②
② ③
③ ④
④ ⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:(1)甲中有
(2)由
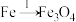 ,
,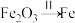 可知,欲实现I反应过程应从
可知,欲实现I反应过程应从(3)请将下列6种物质:
 、
、 、
、 、
、 、
、 、
、 (提示:能按
(提示:能按 ________+________→________+________+
________+________→________+________+ 形式反生化学反应)写出该反应对应的离子方式
形式反生化学反应)写出该反应对应的离子方式(4)一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为:
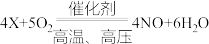 ,请推出X的化学式为
,请推出X的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)铁在元素周期表中的位置为_____ ,基态铁原子有个未成对电子_____ ,三价铁离子的电子排布式为_____ 。
(2)基态Si原子中,电子占据的最高能层符号_____ ,该能层具有的原子轨道数为_____ ;铝元素的原子核外共有_____ 种不同运动状态的电子、_____ 种不同能级的电子。
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____ 形象化描述。在基态14C原子中,核外存在_____ 对自旋相反的电子。
(4)中国古代四大发明之一——黑火药,它的爆炸反应为:2KNO3+3C+S K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为
K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为_____ ,第一电离能从大到小依次为_____ 。
(5)有以下物质:①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥CH4,⑦H2,⑧H2O2,⑨HCN(H—C≡N),⑩Ar,既有σ键又有π键的是______ ;含有由两个原子的s轨道重叠形成的σ键的是______ ;不存在化学键的是______ 。
(6)在BF3分子中,F—B—F的键角是______ ,硼原子的杂化轨道类型为______ ,BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为______ 。
(2)基态Si原子中,电子占据的最高能层符号
(3)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(4)中国古代四大发明之一——黑火药,它的爆炸反应为:2KNO3+3C+S
 K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为
K2S+N2↑+3CO2↑,除S外,上述元素的电负性从大到小依次为(5)有以下物质:①HF,②Cl2,③H2O,④N2,⑤C2H4,⑥CH4,⑦H2,⑧H2O2,⑨HCN(H—C≡N),⑩Ar,既有σ键又有π键的是
(6)在BF3分子中,F—B—F的键角是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】书写金属钠和氧的电子排布式___________ ,________________ 。
您最近一年使用:0次

 )可看作是SO
)可看作是SO 中的一个O原子被S原子取代的产物。
中的一个O原子被S原子取代的产物。

