磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金,主要用作耐磨零件和弹性原件。
(1)基态磷原子中,电子占据的最高能层符号为___ ,在该能层中磷原子的电子占据的能量最高的电子云在空间有___ 个伸展方向,原子轨道呈__ 形。
(2)磷在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态原子的核外电子排布式:___ 。
(3)锡存在两种同素异形体,α—Sn采纳六方最密堆积,β—Sn采纳体心立方堆积,由α—Sn转变为β—Sn晶体体积___ (填“膨胀”或“收缩”)。
(4)[Cu(CH3CN)4]+是非常稳定的络合离子,该络合离子中 键和
键和 键个数之比为
键个数之比为____ 。
(5)某磷青铜晶胞结构如图所示。
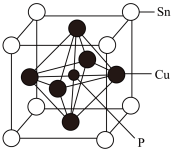
①则其化学式为__ 。
②该晶体中距离Cu原子最近的Sn原子有___ 个,这些Sn原子所呈现的构型为__ 。
③若晶体密度为8.82g•cm-3,最近的Cu原子核间距为___ pm(用含NA的代数式表示,列式即可,不用计算)。
(1)基态磷原子中,电子占据的最高能层符号为
(2)磷在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态原子的核外电子排布式:
(3)锡存在两种同素异形体,α—Sn采纳六方最密堆积,β—Sn采纳体心立方堆积,由α—Sn转变为β—Sn晶体体积
(4)[Cu(CH3CN)4]+是非常稳定的络合离子,该络合离子中
 键和
键和 键个数之比为
键个数之比为(5)某磷青铜晶胞结构如图所示。

①则其化学式为
②该晶体中距离Cu原子最近的Sn原子有
③若晶体密度为8.82g•cm-3,最近的Cu原子核间距为
更新时间:2021-06-01 09:55:59
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钛被称为继铁、铝之后的第三金属,在工业上有着广泛而重要的用途。
(1)基态钛原子的价电子排布图为__________________ ;基态铝原子核外电子分布在____ 个能级上。
(2)许多金属及其化合物灼烧时会产生特征焰色,产生焰色的原因是______________________ 。
(3)FeCl3熔点306℃、沸点315℃,CaCl2熔点782℃、沸点1600℃,同是金属氯化物,熔沸点差别很大的原因是________________________________ 。
(4)煅烧铁矿石常会生成SO2,SO2 为_______ 分子(填“极性”或“非极性”);分子中的大π键可用符号Пnm表示,其中m代表参与形成大π键的原子数,n 代表参与形成大π 键的电子数(如苯分子中的大π键可表示为П66)。推测SO2分子中的大π键可表示为_______________ 。
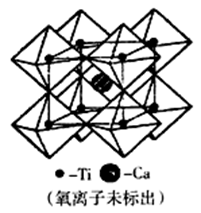
(5)钙钛矿可用来冶炼钛,它的晶胞结构如图所示。钛离子位于立方晶胞的角顶,被____ 个氧离子包围成配位八面体;钙离子离子位于立方晶胞的体心,被_____ 个氧离子包围。钙钛矿晶体的化学式为________________________ 。若该晶胞的边长为a pm,则钙钛矿晶体的密度为_____________ g·cm-3(用NA 表示阿保加德罗常数的值,只要求列算式,不必计算出数值)
(1)基态钛原子的价电子排布图为
(2)许多金属及其化合物灼烧时会产生特征焰色,产生焰色的原因是
(3)FeCl3熔点306℃、沸点315℃,CaCl2熔点782℃、沸点1600℃,同是金属氯化物,熔沸点差别很大的原因是
(4)煅烧铁矿石常会生成SO2,SO2 为
(5)钙钛矿可用来冶炼钛,它的晶胞结构如图所示。钛离子位于立方晶胞的角顶,被

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮、镁和铝元素及其化合物用途极为广泛。回答下列问题:
(1)基态N原子的最高能级原子轨道的形状是_______ ,价层电子排布图是_______ 。
(2)镁和铝的前5级电离能数值如下表:
一般来说,相对应的各级电离能是Al的比Mg的大,但也有反常,如I1(Mg)>I1(Al),该反常的原因是_____ 。
(3)镁的卟啉配合物的结构如图所示。

①上述粒子中包含元素的电负性从大到小的顺序是_______ (用元素符号表示),从电子给予的角度分析, Mg2+和N之间存在的化学键类型是 _______ 。
②该物质中的C原子的杂化轨道类型是_______ 。
(4)AlN是良好的耐热耐冲击材料,其晶胞结构如图所示。

①AlN熔点为2200 °C ,该晶体类型为_______ 。
②若AlN的晶胞的高为a nm,底边长为b nm,NA表示阿伏加德罗常数的值,则其晶体的密度为______ g·cm-3(用含a、b、NA的代数式表示)。
(1)基态N原子的最高能级原子轨道的形状是
(2)镁和铝的前5级电离能数值如下表:
| 电离能/(kJ ·mol -1) 元素 | I1 | I2 | I3 | I4 | I5 |
| Mg | 738 | 1451 | 7 733 | 10 540 | 13 630 |
| Al | 578 | 1 817 | 2 745 | 11575 | 14 830 |
(3)镁的卟啉配合物的结构如图所示。

①上述粒子中包含元素的电负性从大到小的顺序是
②该物质中的C原子的杂化轨道类型是
(4)AlN是良好的耐热耐冲击材料,其晶胞结构如图所示。

①AlN熔点为2200 °C ,该晶体类型为
②若AlN的晶胞的高为a nm,底边长为b nm,NA表示阿伏加德罗常数的值,则其晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】氧元素与多种元素具有亲和力,所形成化合物的种类很多。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为______ 。氧元素与氟元素能形成OF2分子,该分子的空间构型为______
(2)根据等电子体原理,在NO2+中氮原子轨道杂化类型是______ ;1molO22+中含有的π键数目为______ 个
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。Cr基态核外电子排布式为______
(4)下列物质的分子与O3分子的结构最相似的是______
A.H2O B.CO2 C.SO2 D.BeCl2
(5)O3分子是否为极性分子______
(1)氮、氧、氟元素的第一电离能从大到小的顺序为
(2)根据等电子体原理,在NO2+中氮原子轨道杂化类型是
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。Cr基态核外电子排布式为
(4)下列物质的分子与O3分子的结构最相似的是
A.H2O B.CO2 C.SO2 D.BeCl2
(5)O3分子是否为极性分子
您最近一年使用:0次
【推荐1】Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种_______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_______ ,能量最低的是_______ (填序号)。
a.1s22s22p43s13px13py13pz1 b.1s22s22p33s23px13py13pz1
c.1s22s22p63s13px1 d.1s22s22p63s2
(3)Ti原子位于元素周期表中的_______ 区,最高能层电子的电子云轮廓形状为_______ ,其价电子排布式为_______ 。与Ti同周期的过渡元素中,未成对电子数最多的的基态原子的外围电子排布图_______ 。
(4)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是_______ 。
(5)Fe3+与Fe2+的离子半径大小关系为Fe3+_______ Fe2+(填“大于”或“小于”)
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.1s22s22p43s13px13py13pz1 b.1s22s22p33s23px13py13pz1
c.1s22s22p63s13px1 d.1s22s22p63s2
(3)Ti原子位于元素周期表中的
(4)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是
(5)Fe3+与Fe2+的离子半径大小关系为Fe3+
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最高为_______(填标号)。
(2)三价铬离子能形成多种配位化合物。 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是_______ ,中心离子的配位数为_______ 。
(3) 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。

PH3中P的杂化类型是_______ 。NH3的沸点比PH3的高,原因是_______ ,H2O的键角小于NH3的,分析原因_______ 。
(4)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为NA,则Li2O的密度为_______ g·cm-3(列出计算式)。

(1)下列Li原子电子排布图表示的状态中,能量最高为_______(填标号)。
A. | B. |
C. | D. |
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(3)
 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。
PH3中P的杂化类型是
(4)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为NA,则Li2O的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为___________ 、___________ 。(填标号)
A.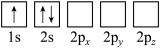 B.
B.
C. D.
D.
(2)Li+与H-具有相同的电子层结构,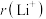 小于
小于 ,原因是
,原因是___________ 。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是___________ 、中心原子的杂化形式为___________ 。LiAlH4中,存在___________ (填标号)。
A. 离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其形成过程能量转化如图(a)所示。

可知,Li原子的第一电离能为___________ kJ∙mol-1,O=O键的键能为___________ kJ∙mol-1。
(5)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为NA,则Li2O的密度为___________ g∙cm-3 (列出计算式)。
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(2)Li+与H-具有相同的电子层结构,
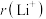 小于
小于 ,原因是
,原因是(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是
A. 离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其形成过程能量转化如图(a)所示。

可知,Li原子的第一电离能为
(5)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为NA,则Li2O的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】金属元素Fe、Ni、Pt均为周期表中同族元素,该族元素的化合物在研究和生产中有许多重要用途。
(1)Fe是常见的金属,生活中用途广泛。请回答下列问题:
①Fe在元素周期表中的位置为________________________ 。
②Fe的一种晶胞结构如图所示,测得晶胞边长为 a pm,则Fe原子半径为__________ 。
③已知:FeO晶体晶胞结构为NaCl型,与O2-距离最近且等距离的亚铁离子围成的空间构型为________ 。
(2)铂可与不同的配体形成多种配合物,分子式为[Pt(NH3)2Cl4]的配合物的配体是_________ ;该配合物有两种不同的颜色,其中橙黄色比较不稳定,在水中的溶解度大;呈亮黄色的物质在水中的溶解度小,如下图所示的结构示意图中呈亮黄色的是_____ (填“A”或“B”),理由是___________ 。
A B
B
(3)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图。

①测知镧镍合金晶胞体积为9.0×10-23cm3,则镧镍合金的晶体密度为____________ (不必计算结果) 。
②储氢原理为:镧镍合金吸附H2,H2解离为原子,H原子储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱和面心,则形成的储氢化合物的化学式为____________ 。
(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”(或大π键)。大π键可用 表示,其中m、n分别代表参与形成大π键的电子数和原子个数,如苯分子中大π键表示为
表示,其中m、n分别代表参与形成大π键的电子数和原子个数,如苯分子中大π键表示为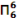 。 下列微粒中存在“离域Π键”的是
。 下列微粒中存在“离域Π键”的是__________ 。
a.O3 b.SO42- c.H2S d.NO3-
(1)Fe是常见的金属,生活中用途广泛。请回答下列问题:
①Fe在元素周期表中的位置为
②Fe的一种晶胞结构如图所示,测得晶胞边长为 a pm,则Fe原子半径为

③已知:FeO晶体晶胞结构为NaCl型,与O2-距离最近且等距离的亚铁离子围成的空间构型为
(2)铂可与不同的配体形成多种配合物,分子式为[Pt(NH3)2Cl4]的配合物的配体是
A
 B
B
(3)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如图。

①测知镧镍合金晶胞体积为9.0×10-23cm3,则镧镍合金的晶体密度为
②储氢原理为:镧镍合金吸附H2,H2解离为原子,H原子储存在其中形成化合物。若储氢后,氢原子占据晶胞中上下底面的棱和面心,则形成的储氢化合物的化学式为
(4)已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”(或大π键)。大π键可用
 表示,其中m、n分别代表参与形成大π键的电子数和原子个数,如苯分子中大π键表示为
表示,其中m、n分别代表参与形成大π键的电子数和原子个数,如苯分子中大π键表示为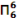 。 下列微粒中存在“离域Π键”的是
。 下列微粒中存在“离域Π键”的是a.O3 b.SO42- c.H2S d.NO3-
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】利用绿矾 和硫铁矿
和硫铁矿 可联合制备铁精粉
可联合制备铁精粉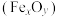 和硫酸。
和硫酸。
(1) 的结构示意图如图所示。
的结构示意图如图所示。___________ 。
② 中O原子和
中O原子和 中S原子均为
中S原子均为 杂化。
杂化。 分子中的
分子中的 键角
键角___________ (填“大于”、“等于”或“小于”)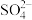 离子中
离子中 键角,其原因是
键角,其原因是___________ 。
③ 属于配位化合物。由结构示意图可知,
属于配位化合物。由结构示意图可知, 中
中 的配位数为
的配位数为___________ 。
(2) 晶体的晶胞形状为立方体,边长为
晶体的晶胞形状为立方体,边长为 ,结构如图所示。
,结构如图所示。 的电子式为
的电子式为___________ 。
② 晶体中
晶体中 位于
位于 形成的
形成的___________ (填“正四面体”或“正八面体”)空隙中。
③ 的摩尔质量为
的摩尔质量为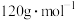 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。该晶体的密度为
。该晶体的密度为___________  。(列出算式即可,无需化简。
。(列出算式即可,无需化简。 )
)
 和硫铁矿
和硫铁矿 可联合制备铁精粉
可联合制备铁精粉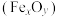 和硫酸。
和硫酸。(1)
 的结构示意图如图所示。
的结构示意图如图所示。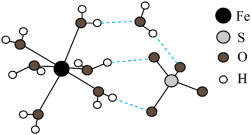
②
 中O原子和
中O原子和 中S原子均为
中S原子均为 杂化。
杂化。 分子中的
分子中的 键角
键角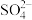 离子中
离子中 键角,其原因是
键角,其原因是③
 属于配位化合物。由结构示意图可知,
属于配位化合物。由结构示意图可知, 中
中 的配位数为
的配位数为(2)
 晶体的晶胞形状为立方体,边长为
晶体的晶胞形状为立方体,边长为 ,结构如图所示。
,结构如图所示。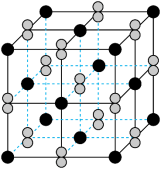
 的电子式为
的电子式为②
 晶体中
晶体中 位于
位于 形成的
形成的③
 的摩尔质量为
的摩尔质量为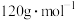 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。该晶体的密度为
。该晶体的密度为 。(列出算式即可,无需化简。
。(列出算式即可,无需化简。 )
)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】I.碳元素广泛存在于自然界中,对人类生命和生活具有重要意义。含碳化合物在工业生产和国防建设中有广泛的应用。
(1)写出基态碳原子的电子排布式________________ , CO2是_______ 分子(填“极性”或“非极性”),中心碳原子采取的杂化类型是_____________ 。
(2)碳和硅是同主族元素,下列能说明二者非金属性相对强弱的是_________ (填编号)。
a.CH4的稳定性比SiH4强 b.SiH4的沸点比CH4高
c.碳酸的酸性大于硅酸 d.SiO2+Na2CO3 =Na2SiO3+CO2↑
II.氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在800℃氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)该反应的平衡常数表达式K=__________________ 。已知平衡常数:K(800℃)>K(850℃),则正反应是__________ 反应(填“放热”或“吸热”)
(2)任写两种能提高二氧化硅转化率的措施______________ 、______________ 。
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2)。Mg3N2溶于足量的稀硫酸可得到两种正盐,写出该反应的化学方程式__________________________________________________ 。
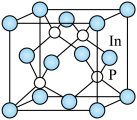
(4)磷化铟是一种半导体材料,其晶胞如下图所示。写出磷化铟的化学式______________ ;In的配位数(与之距离最近的原子数目)为_______________ 。
(1)写出基态碳原子的电子排布式
(2)碳和硅是同主族元素,下列能说明二者非金属性相对强弱的是
a.CH4的稳定性比SiH4强 b.SiH4的沸点比CH4高
c.碳酸的酸性大于硅酸 d.SiO2+Na2CO3 =Na2SiO3+CO2↑
II.氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在800℃氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g)
 Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)(1)该反应的平衡常数表达式K=
(2)任写两种能提高二氧化硅转化率的措施
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2)。Mg3N2溶于足量的稀硫酸可得到两种正盐,写出该反应的化学方程式
(4)磷化铟是一种半导体材料,其晶胞如下图所示。写出磷化铟的化学式

您最近一年使用:0次



