9. 硫酸铅广泛应用于制造铅蓄电池、白色颜料以及精细化工产品3PbO·PbSO
4·H
2O(三盐)等。工业生产中利用方铅矿(主要成分为PbS,含有FeS
2等杂质)制备PbSO
4的工艺流程如图:
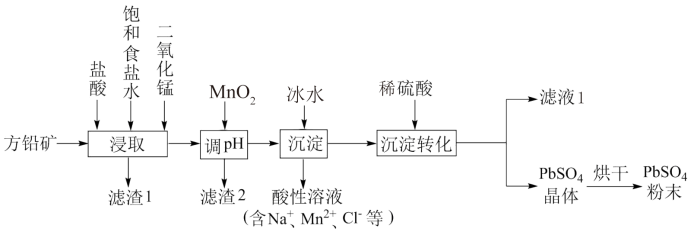
已知:①PbCl
2难溶于冷水,易溶于热水。
②PbCl
2(s)+2Cl
-(aq)

PbCl

(aq)
③
Ksp(PbSO
4)=1.0×10
-8,
Ksp(PbCl
2)=1.6×10
-6(1)“浸取”时需要适当加热控制反应温度约为80℃,选择该温度的原因为
___。
(2)若滤渣1的主要成分为S,“浸取”时Pb元素以Na
2PbCl
4的形式存在于溶液中,则PbS发生反应的离子方程式为
___。
(3)“浸取”步骤中FeS
2和MnO
2颗粒可以组成两个原电池,如图所示:
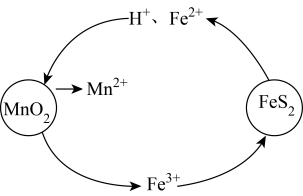
其中,MnO
2原电池反应迅速,而FeS
2原电池由于生成的S覆盖在FeS
2颗粒表面,溶解速率变慢。
①MnO
2原电池中,每消耗2molMnO
2,生成
___molFe
3+。
②FeS
2原电池负极上的电极反应式为
____。
(4)“滤渣2”的主要成分是
___。
(5)“沉淀”操作时加入冰水的目的是
___。
(6)“滤液1”经处理后可返回
___工序循环使用。
(7)PbCl
2经“沉淀转化”后得到PbSO
4,从溶液中获得PbSO
4晶体的操作为过滤、洗涤,干燥。检验沉淀是否洗净的操作为
___,若用1L硫酸溶液转化5mol的PbCl
2,则硫酸溶液的最初浓度不得低于
___(精确到小数点后3位)。